
【题目】如图是从NaCl和CsCl晶体结构中分割出来的部分结构图,其中属于从NaCl晶体中分割出来的结构图是( )
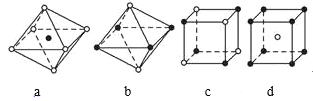
A.只有cB.b和cC.a和cD.a和d
科目:高中化学 来源: 题型:
【题目】如图为元素周期表中短周期的一部分,下列说法正确的是
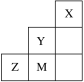
A.电负性:Y>Z>M
B.离子半径:M->Z2->Y-
C.Z和M的最高价含氧酸中非羟基氧原子数分别为2和3
D.Z元素基态原子的轨道表示式为:![]()
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为减轻大气污染,必须要加强对工业废气和汽车尾气的治理,根据所学知识回答下列问题:
(1)化石燃料包括煤、石油和________。
(2)酸雨是指pH____(填“>”“<”或“=”)5.6的降水,煤的燃烧是导致酸雨形成的主要原因,而正常雨水的pH约为5.6,原因是__________________ (用化学方程式表示)。
(3)煤的气化是高效、清洁利用煤的重要途径,可将煤炼成焦炭,再将焦炭在高温下与水蒸气反应生成一氧化碳和氢气的化学方程式为_________,该反应的基本类型是_________。
(4)在汽车尾气排放口加装“三效催化净化器”,在不消耗其他物质的情况下,可将尾气中的一氧化碳、一氧化氮转化为参与大气循环的气体和无毒的气体,该反应的化学方程式为__________________。
(5)在新能源汽车未普及时,如图所示为一种“节能减排”的有效措施,以下对乙醇作汽车燃料的描述错误的是__________(填字母)。
![]()
A.原料来源丰富 B.是可再生能源 C.燃烧完全没有污染
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于合成氨N2(g)+3H2(g) ![]() 2NH3(g)ΔH=-92.4 kJ·mol-1反应,达到平衡后,以下分析正确的是
2NH3(g)ΔH=-92.4 kJ·mol-1反应,达到平衡后,以下分析正确的是
A. 升高温度,对正反应的反应速率影响更大
B. 增大压强,对正反应的反应速率影响更大
C. 减小反应物浓度,对逆反应的反应速率影响更大
D. 加入催化剂,对逆反应的反应速率影响更大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4 mol A(g)和2 mol B(g)在2 L的恒容密闭容器中混合并在一定条件下发生反应:2A(g)+B(g) 2C(g) ΔH<0,反应2 s后测得C的浓度为0.6 mol·L-1。下列说法正确的是
A.2 s后物质A的转化率为70%
B.当各物质浓度满足c(A)=2c(B)=c(C)时,该反应达到了平衡状态
C.达到平衡状态时,增加A的物质的量,A和B的转化率都提高
D.达到平衡状态时,升高温度,平衡逆向移动,同时化学平衡常数K减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学学习小组设计了相关实验来探究元素周期律。该组同学为验证卤素单质氧化性的相对强弱,用如图所示装置进行实验(夹持仪器已略去,气密性已检验)。
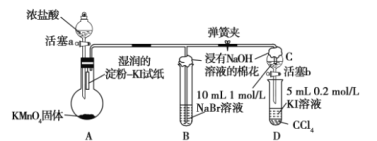
实验过程及现象:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸;
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹;
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a;
Ⅳ.打开活塞b,将少量C中溶液滴入D中,关闭活塞b,取下D振荡,静置后![]() 层溶液变为紫红色。
层溶液变为紫红色。
请回答下列有关问题。
(1)B中溶液由黄色变为棕红色时发生反应的离子方程式为______。
(2)验证氯气的氧化性强于碘的实验现象是______。
(3)B和C仪器口放置浸有![]() 溶液的棉花的作用是______。
溶液的棉花的作用是______。
(4)由此实验得出的结论:同主族元素从上到下,原子的得电子能力逐渐______(填“减弱”或“增强”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为元素周期表前四周期的一部分,下列有关B、W、X、Y、Z五种元素的叙述正确的是

A.常温常压下,W、Y、Z元素的单质中,Z的单质的沸点最高
B.W的最简单氢化物比X的最简单氢化物稳定性强
C.Y、Z的简单阴离子的电子层结构都与B元素原子的相同
D.Y元素比W元素的非金属性强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是元素周期表的一部分,表中所列字母分别代表一种元素。根据表中所列元素回答下列问题:
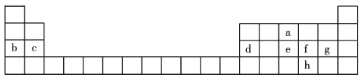
(1)元素d在元素周期表中的位置是________,元素h与f的原子序数相差_____。
(2)元素b、c、f形成的简单离子中半径最小的是______(填离子符号),原子半径最小的是______(填元素符号)。
(3)表中第三周期所列元素的非金属性最强的是______(填元素符号),e、f、g三种元素的简单氢化物中最不稳定的是______(填化学式)。
(4)元素![]() 与元素
与元素![]() 的最高价氧化物对应水化物反应的化学方程式为______。
的最高价氧化物对应水化物反应的化学方程式为______。
(5)铅(Pb)、锡(Sn)、锗(Ge)与碳(C)、硅(Si)属于同主族元素,常温下,在空气中,单质锡、锗均不反应而单质铅表面生成一层氧化铅;单质锗与盐酸不反应,而单质锡与盐酸反应。由此可得出以下结论:
①锗的原子序数为______;
②铅(Pb)、锡(Sn)、锗(Ge)的+4价氢氧化物的碱性由强到弱的顺序为___________(用化学式表示)。
(6)最近,德国科学家实现了铷原子气体的超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷(Rb)是37号元素,相对原子质量是85.5,与钠同主族。回答下列问题:
①铷在元素周期表中的位置为__________________。
②同主族元素的同类化合物的性质相似,请写出AlCl3与RbOH过量反应的离子方程式:_____________________。
③现有铷和另一种碱金属形成的混合金属50 g,当它与足量水反应时,放出标准状况下的氢气22.4 L,另一种碱金属可能是__________。(填序号)
A.Li B.Na C.K D.Cs
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃料电池的优点有能量转化效率高、无污染等。下图是乙醇燃料电池(BFC)的示意图,a、b为置于多孔陶瓷管中的纳米碳纤维电极。下列有关该电池的说法不正确的是
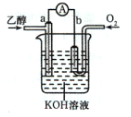
A.电子由a极经外电路导线流向b极
B.b极的电极反应式为:O2+4H++4e-=2H2O
C.该电池的总反应式为:C2H5OH+3O2+4KOH=2K2CO3+5H2O
D.用该电池电镀铜时,若待镀金属增重12.8 g,至少消耗标准状况下的氧气2.24 L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com