
【题目】氮及其化合物对环境具有显著影响。
(1)已知汽车气缸中氮及其化合物发生如下反应:
①N2(g)+O2(g) 2NO(g) △H=+180 kJ/mol
②N2(g)+2O2(g) 2NO2(g) △H=+68 kJ/mol
则2NO(g)+O2(g) 2NO2(g) △H=_____kJ/mol
(2)对于反应2NO(g)+O2(g) 2NO2(g)的反应历程如下:
第一步:2NO(g)![]() N2O2(g)(快速平衡)
N2O2(g)(快速平衡)
第二步:N2O2(g)+O2(g)![]() 2NO(g)(慢反应)
2NO(g)(慢反应)
其中可近似认为第二步反应不影响第一步的平衡,第一步反应中:υ正=k1 正·c2(NO),υ 逆=k1 逆·c(N2O2),k1正、k1 逆为速率常数,仅受温度影响。下列叙述正确的是_____
a.整个反应的速率由第一步反应速率决定
b.同一温度下,平衡时第一步反应的![]() 越大,反应正向程度越大
越大,反应正向程度越大
c.第二步反应速率慢,因而平衡转化率也低
d.第二步反应的活化能比第一步反应的活化能高
(3)将氨气与二氧化碳在有催化剂的反应器中反应![]() △H=-87.0 kJ/mol,体系中尿素的产率和催化剂的活性与温度的关系如图1所示:
△H=-87.0 kJ/mol,体系中尿素的产率和催化剂的活性与温度的关系如图1所示:
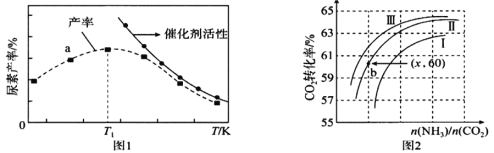
①a点_____(填是或不是)处于平衡状态,T1之后尿素产率下降的原因可能是 _____________。
②实际生产中,原料气带有水蒸气,图2表示CO2的转化率与氨碳比![]() 、水碳比
、水碳比![]() 的变化关系。曲线Ⅰ、Ⅱ、Ⅲ对应的水碳比最大的是_____,测得b点氨的转化率为30%,则x=______________。
的变化关系。曲线Ⅰ、Ⅱ、Ⅲ对应的水碳比最大的是_____,测得b点氨的转化率为30%,则x=______________。
(4)N2H4可作火箭推进剂。已知25℃时N2H4水溶液呈弱碱性:N2H4+H2ON2H5++OH- K1=![]() ;N2H5++H2ON2H62++OH - K2=
;N2H5++H2ON2H62++OH - K2=![]() ;
;
①25℃时,向N2H4水溶液中加入H2SO4,欲使c(N2H5+ )>c(N2H4 ),同时c(N2H5+)>c(N2H62+),应控制溶液pH范围__________(用含a、b式子表示)。
②水合肼(N2H4·H2O)的性质类似一水合氨,与硫酸反应可以生成酸式盐,该盐的化学式为__________。
【答案】-112 bd 不是 升高温度,平衡逆向移动,产率下降,且催化剂的活性降低 Ⅰ 4 14-b<pH<14-a (N2H6)(HSO4)2
【解析】
(1)根据盖斯定律分析解答;
(2)a.整个反应的速率由慢反应决定;
b.υ正=k1 正·c2(NO),υ 逆=k1 逆·c(N2O2),反应达平衡时,υ正=υ逆,所以![]() =K(该化学平衡常数),据此进行分析;
=K(该化学平衡常数),据此进行分析;
c.反应速率与转化率无关;
d.相同温度下,第一步反应快速达到平衡,第二步是慢反应;据此分析判断;
(3)①产率最高之前,反应未达到平衡状态;结合温度对平衡移动及催化剂的影响回答;
②氨碳比相同时,增大水蒸气的含量,平衡逆向移动,二氧化碳的转化率减小,结合图象分析判断水碳比最大的曲线;根据图象,b点时,![]() =x,α(CO2)=60%,α(NH3)=30%,结合2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g)计算解答;
=x,α(CO2)=60%,α(NH3)=30%,结合2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g)计算解答;
(4)①N2H4+H2ON2H5++OH- K1=1×10-a;N2H5++H2ON2H62++OH- K2=1×10-b,根据平衡常数表达式结合c(N2H5+)>c(N2H4),同时c(N2H5+)>c(N2H62+),计算c(OH-)的范围,从而计算pH的范围;
②水合肼的性质类似一水合氨,在水中应该能电离产生N2H62+和OH-,据此分析判断与硫酸反应生成的酸式盐的化学式。
(1)已知①N2(g)+O2(g)2NO(g)△H=+180 kJmol-1,②N2(g)+2O2(g)2NO2(g)△H=+68 kJmol-1,根据盖斯定律,反应②-①得:2NO(g)+O2(g)=2NO2(g) △H=(-180+68)kJmol-1 =-112kJ/mol,故答案为:-112;
(2)a.整个反应的速率由慢反应决定,即由第二步反应速率决定,故a错误;
b.根据①同一温度下,平衡时第一步反应的![]() 越大,化学平衡常数越大,则反应正向进行程度越大,故b正确;
越大,化学平衡常数越大,则反应正向进行程度越大,故b正确;
c.反应速率的快慢与转化率无关,转化率与反应的限度有关,故c错误;
d.相同温度下,第一步反应快速达到平衡,第二步是慢反应,则第二步的活化能比第一步的活化能高,故d正确;
故答案为:bd;
(3)①产率最高之前,未达到平衡状态,故a点不是平衡点;反应为放热反应,达到平衡之后,升高温度,平衡逆向移动,产率下降,且催化剂的活性降低;
故答案为:不是;升高温度,平衡逆向移动,产率下降,且催化剂的活性降低;
②氨碳比相同时,增大水蒸气的含量,平衡逆向移动,二氧化碳的转化率减小,根据图象,氨碳比相同时,曲线Ⅲ的二氧化碳的转化率大,所以曲线Ⅰ、Ⅱ、Ⅲ对应的水碳比最大的是为Ⅰ;根据图象,b点时,![]() =x,α(CO2)=60%,α(NH3)=30%,假设二氧化碳为1mol,则氨气为xmol,转化的二氧化碳为0.6mol,根据2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g),转化的氨气为1.2mol,则α(NH3)=
=x,α(CO2)=60%,α(NH3)=30%,假设二氧化碳为1mol,则氨气为xmol,转化的二氧化碳为0.6mol,根据2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g),转化的氨气为1.2mol,则α(NH3)=![]() ×100%=0.3,解得:x=4,故答案为:Ⅰ;4;
×100%=0.3,解得:x=4,故答案为:Ⅰ;4;
(4)①N2H4+H2ON2H5++OH- K1=1×10-a;N2H5++H2ON2H62++OH- K2=1×10-b,可知K1=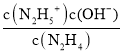 =1×10-a,K2=
=1×10-a,K2=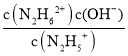 =1×10-b,欲使c(N2H5+)>c(N2H4),同时c(N2H5+)>c(N2H62+),则1×10-b<c(OH-)<1×10-a,即应控制溶液pH范围为14-b<pH<14-a,故答案为:14-b<pH<14-a;
=1×10-b,欲使c(N2H5+)>c(N2H4),同时c(N2H5+)>c(N2H62+),则1×10-b<c(OH-)<1×10-a,即应控制溶液pH范围为14-b<pH<14-a,故答案为:14-b<pH<14-a;
②水合肼的性质类似一水合氨,在水中应该能电离产生N2H62+和OH-,因此它与硫酸反应生成的酸式盐的化学式为(N2H6)(HSO4)2,故答案为:(N2H6)(HSO4)2。


 名题金卷系列答案
名题金卷系列答案 优加精卷系列答案
优加精卷系列答案科目:高中化学 来源: 题型:
【题目】氯毗格雷(clopidogrel)是一种用于抑制血小板聚集的药物,以2-氯苯甲醛为原料的合成路线如下:

(1)分子C中能团名称为__________,氯吡格雷的分子式为____________。
(2)X的结构简式为_____________。
(3)两分子C可在一定条件下反应,生成的有机产物中含有3个六元环,写出该反应的化学方程式:_____________________。
(4)物质D的某种同分异构体G满足以下条件:
① 苯环上有两个取代基,且其中一个取代基不含碳原子;② 与D中的官能团相同;③G能发生银镜反应;则符合条件的G有_______种。
(5)已知:![]()
在下列方框内写出由乙烯-甲醇为有机原料制备化合物![]() 的合成路线流程图(无机试剂任选),并标出每步对应的反应类型。_____________________示例如下:
的合成路线流程图(无机试剂任选),并标出每步对应的反应类型。_____________________示例如下:
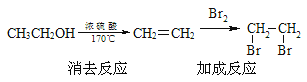
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在容积为V L的密闭容器里进行反应,M、N的物质的量随时间的变化曲线如图所示,且两者都为气体:
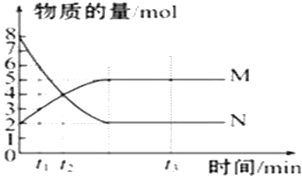
(1)此反应的化学方程式为__________________。
(2)t1到t2时刻,以M的浓度变化表示的平均反应速率为:__________________。
(3)达平衡时N的转化率为:_______________ ;
(4)反应前与达平衡时容器内压强之比为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化妆品的组分Z具有美白功效,原从杨树中提取,现可用如下反应制备:

下列叙述错误的是
A. X、Y和Z均能使溴水褪色
B. X和Z均能与NaHCO3溶液反应放出CO2
C. Y既能发生取代反应,也能发生加成反应
D. Y可作加聚反应单体,X可作缩聚反应单体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种芳纶纤维的拉伸强度比钢丝还高,广泛用作防护材料。其结构片段如下图
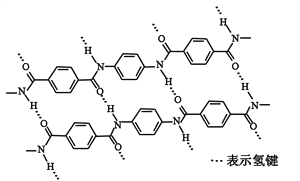
下列关于该高分子的说法正确的是
A. 完全水解产物的单个分子中,苯环上的氢原子具有不同的化学环境
B. 完全水解产物的单个分子中,含有官能团―COOH或―NH2
C. 氢键对该高分子的性能没有影响
D. 结构简式为:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为环境修复研究的热点之一。

(1)Fe还原水体中NO3-的反应原理如图1所示。
①作负极的物质化学式为___________。
②正极的电极反应式是_________________________________________。
(2)将足量铁粉投入水体中,经24小时测定NO3-的去除率和pH,结果如下:
初始pH | pH=2.5 | pH=4.5 |
NO3-的去除率 | 接近100% | <50% |
24小时pH | 接近中性 | 接近中性 |
铁的最终物质形态 |
|
|
pH=4.5时,NO3-的去除率低。其原因是_____________________________________。
(3)实验发现:在初始pH=4.5的水体中投入足量铁粉的同时,补充一定量的Fe2+可以明显提高NO3-的去除率。对Fe2+的作用提出两种假设:
Ⅰ.Fe2+直接还原NO3-;
Ⅱ.Fe2+破坏FeO(OH)氧化层。
①做对比实验,结果如图2所示,可得到的结论是____________________。
②同位素示踪法证实Fe2+能与FeO(OH)反应生成Fe3O4,该反应的离子方程式为_________,解释加入Fe2+提高NO3-去除率的原因:_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以葡萄糖为原料制得的山梨酸醇(A)和异山梨酸醇(B)都是重要的生物质转化平台化合物。E是一种治疗心绞痛的药物。由葡萄糖为原料合成E的路线如下:

回答下列问题:
(1)葡萄糖的分子式为______;A中含有的官能团的名称为_______。
(2)C的结构简式为_______;由B到C的反应类型为____。
(3)由D到E的反应方程式为:_________。
(4)F是B的同分异构体。7.30g的F与足量饱和碳酸氢钠反应可释放出2.24LCO2(标准状况),F的可能结构有_____种(不考虑立体异构);其中核磁共振氢谱为三组峰,峰面积比为3:1:1的结构为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水合肼(N2H4·H2O)是一种强还原性的碱性液体,是一种用途广泛的化工原料,实验室用如图装置制备(部分装置省略)。
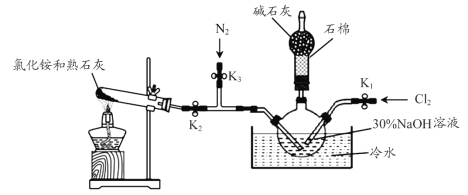
步骤1关闭K2、K3,打开K1,制备NaClO。
步骤2关闭K1、K2,打开K3,通入N2一段时间;关闭K3,打开K2,通入NH3,制备N2H4·H2O。
回答下列问题:
(1)盛放碱石灰的仪器的名称为___________。
(2)配制30%NaOH溶液时,所需玻璃仪器除量筒外还有__________(填标号)。
A.容量瓶 B.烧杯 C.烧瓶 D.玻璃棒
(3)步骤2中通入N2一段时间的原因是____________________。
(4)本装置中制备氨气的化学方程式是______________________________。
(5)NH3与NaClO反应生成N2H4·H2O的化学方程式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸是一种重要的化工产品.实验室用硝酸氧化淀粉水解液制备草酸的装置如图所示(加热、搅拌和仪器固定装置均已略去)。

实验过程如下:
①将一定量的淀粉水解液加入三颈瓶中;
②控制反应液温度在55~60℃条件下,边搅拌边缓慢滴加一定量含有适量催化剂的混酸(65%HNO3与98%H2SO4的质量比为2∶1.5)溶液;
③反应3h左右,冷却,抽滤后再重结晶得草酸晶体;
硝酸氧化淀粉水解液过程中可发生下列反应:
C6H12O6+12HNO3→3H2C2O4+9NO2↑+3NO↑+9H2O
C6H12O6+8HNO3→6CO2+8NO↑+10H2O
3H2C2O4+2HNO3→6CO2+2NO↑+4H2O
(1)检验淀粉是否水解完全所需用的试剂为________;
(2)实验中若混酸滴加过快,将导致草酸产率下降,其原因是_________;
(3)装置C用于尾气吸收,当尾气中n(NO2)∶n(NO)=1∶1时,过量的NaOH溶液能将NO,全部吸收,原因是_________(用化学方程式表示);
(4)与用NaOH溶液吸收尾气相比较,若用淀粉水解液吸收尾气,其优、缺点是________;
(5)草酸重结晶的减压过滤操作中,除烧杯、玻璃棒外,还必须使用属于硅酸盐材料的仪器有_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com