
����Ŀ���㶹�أ�3������![]() ��һ����Ҫ������,�������ճ���Ʒ��ʳƷ�ļ������
��һ����Ҫ������,�������ճ���Ʒ��ʳƷ�ļ������
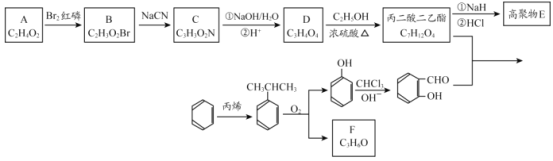
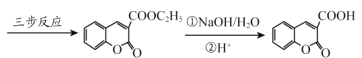
��֪:
RCOOR��+ R��OH ![]() RCOOR�� + R��OH��R ����������
RCOOR�� + R��OH��R ����������
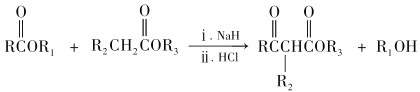
��1��A��B��������,A �Ľṹ��ʽ__________�������ϩ��Ӧ��������_______��
��2��F Ϊ��״�ṹ,��һ�ȴ���ֻ��һ��,��F ���еĹ���������Ϊ__________��
��3��D��������������Ļ�ѧ����ʽ:_______��
��4���������������һ�������¿��γɾۺ��� E,��ṹ��ʽΪ:________��
��5��д���������������ı����������ͬ���칹��Ľṹ��ʽ:________��
���������������Ĺ�������ͬ;
�ں˴Ź����������������շ�,�ҷ����֮��Ϊ 3:2:1;
���ܷ���������Ӧ��
��6���������������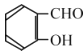 ����������Ӧ�ϳ�
����������Ӧ�ϳ�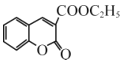 ��
��
��д���м����Ľṹ��ʽ��
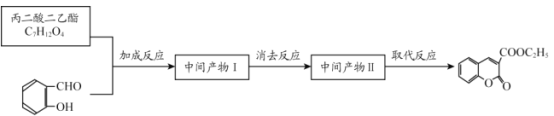
����I__________������II___________��
���𰸡�CH3COOH �ӳɷ�Ӧ �ʻ� ![]() +2C2H5OH
+2C2H5OH![]()
![]() +2H2O
+2H2O 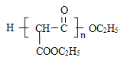
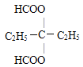 ��
��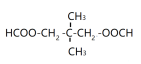
![]()
��������
�������������D���Ҵ���Ӧ�õ�����֪DΪ������ɣ�1����֪A��B�������ԣ�������Ȼ�����AΪCH3COOH��A����ˮ�ͺ���Ӧ�õ�B��B����NaCN��Ӧ�õ�C����BΪBrCH2COOH��CΪNCCH2COOH��������Ϣ��ʾ���߾���Ϊ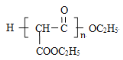 ��
��
��1���ɷ�����֪AΪCH3COOH�������ϩ��Ӧ�õ����������Ϊ�ӳɷ�Ӧ���ʴ�Ϊ��CH3COOH���ӳɷ�Ӧ��
��2��FΪC3H6O,�����Ͷ�Ϊ1����״�ṹ����һ�ȴ���ֻ��һ�֣������������������FΪ��ͪ��������Ϊ�ʻ����ʴ�Ϊ���ʻ���
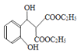
��3���������������D���Ҵ�����������Ӧ�õ�������ʽΪ![]() +2C2H5OH
+2C2H5OH![]()
![]() +2H2O���ʴ�Ϊ��
+2H2O���ʴ�Ϊ��![]() +2C2H5OH
+2C2H5OH![]()
![]() +2H2O��
+2H2O��
��4��������Ϣ��ʾ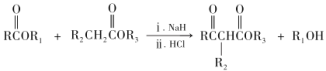 �������������Ҫ�γɸ߾���E����Ҫ�������Ӽ����۷�Ӧ���߾���EΪ
�������������Ҫ�γɸ߾���E����Ҫ�������Ӽ����۷�Ӧ���߾���EΪ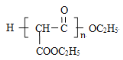 ���ʴ�Ϊ��
���ʴ�Ϊ��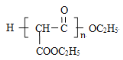 ��
��
��5���������������ͬ���칹��������������������Ĺ�������ͬ��˵�������������ں˴Ź����������������շ壬�ҷ����֮��Ϊ 3:2:1��������ԭ�Ӹ����ֱ�Ϊ6��4��2�����ܷ���������Ӧ��˵������ȩ�������������ݢڿ�֪����������������ʣ��-C5H10,Ҫ������ͬ��ֱ�Ϊ6��4��ֻ��Ϊ�����Ǽ��������������������ĽṹΪ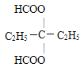 ��
�� ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��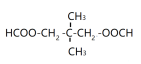 ��
��
��6��![]() �����������������ӳɷ�Ӧ��˫�����ѣ�����û��Ӱ�죬��ȩ��̼��˫�����ѣ�����
�����������������ӳɷ�Ӧ��˫�����ѣ�����û��Ӱ�죬��ȩ��̼��˫�����ѣ�����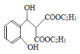 ��
�� ������ȥ��Ӧ�õ�
������ȥ��Ӧ�õ�![]() ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��![]() ��
��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��T1�¶�ʱ���ݻ�Ϊ2L�ĺ����ܱ�������ֻ����1.00molNO2���巢����Ӧ��2NO(g)+O2(g)![]() 2NO2(g) H<0��ʵ���ã�v��=k��c2(NO)��c(O2)��v��=k��c2(NO2)��k����k��Ϊ���ʳ���ֻ���¶�Ӱ�졣��ͬʱ�̲��������n(NO2)���±���
2NO2(g) H<0��ʵ���ã�v��=k��c2(NO)��c(O2)��v��=k��c2(NO2)��k����k��Ϊ���ʳ���ֻ���¶�Ӱ�졣��ͬʱ�̲��������n(NO2)���±���
ʱ��/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO2)/mol | 1.00 | 0.80 | 0.65 | 0.55 | 0.50 | 0.50 |
��1����0��2s�÷�Ӧ��ƽ������v(NO2)=__��
��2��T1�¶�ʱ��ѧƽ�ⳣ��K=__L��mol-1��
��3����ѧƽ�ⳣ��K�����ʳ���k����k������ѧ��ϵ��K=__�������������¶ȸı�ΪT2ʱ��k��=k������T2__T1(����>������<������=��)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʯ���ѽ�õ�ij��A,�����ģ��Ϊ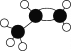 ,������Ҫ�Ļ�������ԭ�ϡ�
,������Ҫ�Ļ�������ԭ�ϡ�
��A�Ľṹ��ʽΪ_______��
��A��������Ȼ�̼��Һ��Ӧ�Ļ�ѧ����ʽΪ_____________________��
��A��ʹ���Ը��������Һ��ɫ�������ķ�Ӧ����Ϊ��______________��
��A��ͬϵ��B����Է���������A��14,B�Ľṹ��________�֡���������˳���칹����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ƣ�NaClO2����һ�ָ�Ч��Ư���������������������ƣ�NaClO3��Ϊԭ����ȡ����������ClO2Ϊ��̬��������˵���������
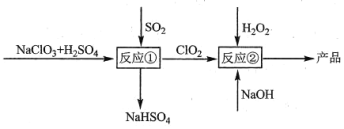
A.��Ӧ�ٽΣ��μӷ�Ӧ��NaClO3��SO2�����ʵ���֮��Ϊ2:1
B.��Ӧ�ٺ����ɵ�����Ҫ��������뷴Ӧ��װ��
C.�����¶ȣ������ڷ�Ӧ����߲���
D.��Ӧ��������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������(H2C2O4)�Ƕ�Ԫ���ᣬNaHC2O4��Һ�����ԡ������£���10 mL 0.01 mol/L NaHC2O4��Һ�еμ�0.01 mol/L NaOH��Һ������NaOH��Һ��������ӣ���Һ������Ũ�ȹ�ϵ�������( )
A.V(NaOH) = 0ʱ��c(H��) >1��10��7mol/L
B.V(NaOH)��10 mLʱ�����ܴ���c(Na��) = 2c(C2O42-)��c(HC2O4- )
C.V(NaOH) = 10 mLʱ����Һ��pHΪ9����10-9= 10-5-2c(H2C2O4)-c(HC2O4-)
D.V(NaOH)��10 mLʱ�����ܴ���c(OH- )��c(Na��)��c(C2O42-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧʵ��С����ѧϰ��ѧ��Դ���ȼҵ���֪ʶ����ʵ���ҽ���ʵ����֤�����������װ������ͼ��ʾװ�ã���֪aΪʯī�缫��bΪ���缫��cΪ���缫���ѳ�ȥ��������Ĥ����dΪ���ʯī�缫���ձ�������������ʳ��ˮ�����з�̪�������õ��ߺ�����ָ�뷢������ƫת�������ж���ȷ����
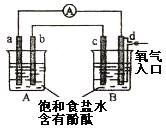
A.b������d����
B.һ��ʱ���a��d�缫������Һ���
C.b�缫�缫��ӦʽΪ��2Cl-��2e-=Cl2��
D.�����һ��ʱ�䣬B�г��ִ�����ɫ����ʱ��ֹͣʵ�飬�ٽ�A����Һ����B�л�ϣ����������ȫ����ʧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ˮ���Ȼ�����CrCl3��Ϊ��ɫ���壬�ڹ�ҵ����Ҫ����ýȾ���ʹ�����ij��ѧС����Cr2O3��CCl4�ڸ������Ʊ���ˮ���Ȼ���������ʵ��װ����ͼ��ʾ��
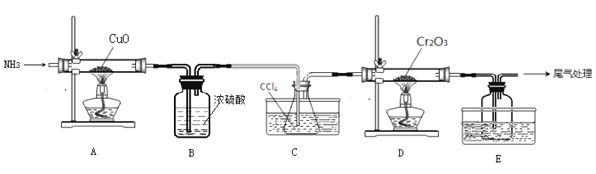
��֪����CrCl3�۵�Ϊ83�棬�׳��⣬��������������ˮ������ˮ�⣬�������ױ�������������Cr2O3��CCl4�ڸ����·�Ӧ�IJ���ΪCrCl3������COCl2 ������ش��������⣺
��1��װ��A�ǵ����Ʊ�װ�ã�������������____________��
��2��װ��B������Ϊ________��װ��C��װ��E��ˮ����Ӧ�ֱ�ʢ��__________��____________��
��3��װ��D������CrCl3������COCl2 ���Ļ�ѧ����ʽΪ_________��
��4����ʵ��װ������Ʋ������ĵط�����д���Ľ�������_________��дһ�㼴�ɣ�
��5����Ʒ��CrCl3���������IJⶨ��
��i����ȡ0.3000 g�õ���CrCl3��Ʒ����ˮ����250mL����ƿ�ж��ݡ�
��ii��ȡ25.00mL��Ʒ��Һ�ڴ�������ƿ�У����������ں�����Թ�����Na2O2,ϡ�Ͳ�������У��ټ��������H2SO4�ữ����Cr3+����ΪCr2O72-���ټ��������KI���壬����ҡ�ȣ�ʹ����ȫ��Cr3+��ʽ����
��iii������1mLָʾ������0.0250 mol��L��1��Na2S2O3��Һ�ζ����յ㣬ƽ�вⶨ���Σ�ƽ�����ı�Na2S2O3��Һ21.00mL����֪2Na2S2O3+I2= Na2S4O6+2NaI��
��ii�м����Թ�����Na2O2��Ҫ������У�����Ҫԭ����____________������KI������Ӧ�����ӷ���ʽΪ________________
�ڵζ�ʵ���ѡ�õ�ָʾ��Ϊ____________��Ʒ��CrCl3��������Ϊ_______%�����������λ��Ч���֣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ M��N �Ǻϳ�ij���ܸ߷��Ӳ��ϵ��м������й��� M��N ˵����ȷ����
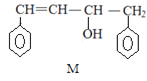
![]()
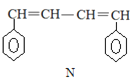
A.M��N �����ڷ����������Ȳ���ͬϵ�Ҳ����ͬ���칹��
B.M��N �ֱ���Һ���ϣ�������ȡ����Ӧ
C.M��N ����ʹ���Ը��������Һ��ɫ
D.M��N ��������ԭ�Ӿ����ܹ�ƽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ����ȷ����
A.�ð�ˮ���չ����Ķ�������![]()
B.��0.5mol L-1 KAl(SO4)2��Һ�е���0.5mol L-1 Ba(OH)2��Һʹ![]() ǡ����ȫ������2Ba2+ 4OH- + Al3++2
ǡ����ȫ������2Ba2+ 4OH- + Al3++2![]() =2BaSO4��+
=2BaSO4��+![]() +2H2O
+2H2O
C.������Na2S2O3��Һ��ȥˮ�е� Cl2: 4Cl2+![]() +5H2O =10H++2
+5H2O =10H++2![]() +8Cl-
+8Cl-
D.����CO2ͨ�뱽������Һ�У�C6H5O-+CO2+H2O��C6H5OH+![]()
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com