
【题目】用含锂废渣(主要金属元素的含量:Li 3.50% Ni 6.55% Ca 6.41% Mg 13.24%)制备Li2CO3,并用其制备锂电池的正极材料LiFePO4。部分工艺流程如下:
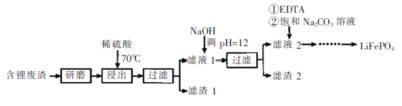
资料:i滤液1、滤液2中部分例子浓度(g·L-1)
Li+ | Ni2+ | Ca2+ | Mg2+ | |
滤液1 | 22.72 | 20.68 | 0.36 | 60.18 |
滤液2 | 21.94 | 7.7×10-3 | 0.08 | 0.78×10-3 |
ii.EDTA能和某些二价金属离子形成稳定的水溶性络合物
iii.某些物质的溶解度(S)
T/℃ | 20 | 40 | 60 | 80 | 100 |
S(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 | 0.72 |
S(Li2SO4)/g | 34.7 | 32.7 | 31.7 | 30.9 |
I.制备Li2CO3粗品
(1)上述流程中为加快化学反应速率而采取的措施是____。
(2)滤渣2的主要成分有____。
(3)向滤液2中先加入EDTA,再加入饱和Na2C03溶液,90℃充分反应后,分离出固体 Li2CO3粗品的操作是_______。
(4)处理lkg含锂3.50%的废渣,锂的浸出率为a,Li+转化为Li2CO3的转化率为b,则粗品中含Li2CO3的质量是________g。(摩尔质量:Li2CO3 74 g.mol4)
II.纯化Li2CO3粗品
(5)将Li2CO3转化为LiHCO3后,用隔膜法电解LiHCO31溶液制备高纯度的LiOH,再转化得电池级Li2CO3。电解原理如图所示,阳极的电极反应式是____,该池使用了_________(填“阳”或“阴”)离子交换膜。

Ⅲ.制备 LiFePO4
(6)将电池级Li2CO3和C、FePO4高温下反应,生成LiFePO4和一种可燃性气体,该反应的化学方程式是_________。
【答案】研磨、70℃加热 Ni(OH)2、Mg(OH)2、Ca(OH)2 趁热过滤 185ab 4OH--4e-=2H2O+O2↑ 阳 ![]()
【解析】
根据流程可知,将含锂废渣研磨后,在70℃条件下用稀硫酸酸浸其中的金属,得到含有的Li+、Ni2+、Ca2+、Mg2+酸性溶液,其中部分Ca2+与硫酸根离子生成CaSO4沉淀,过滤,滤渣1主要是CaSO4,向滤液1中加入NaOH调节pH=12沉淀Ni2+、Ca2+、Mg2+,滤渣2主要为Ni(OH)2、Mg(OH)2还有极少量的Ca(OH)2,滤液2含有Li+,向滤液2中先加入EDTA,再加入饱和Na2CO3溶液,90℃充分反应后,得到沉淀,趁热过滤得到粗品Li2CO3,将Li2CO3转化为LiHCO3后,用隔膜法电解LiHCO3溶液制备高纯度的LiOH,再转化得电池级Li2CO3.将电池级Li2CO3和C、FePO4高温下反应:Li2CO3+2C+2FePO4=2LiFePO4+3CO↑,据此分析作答。
:(1)流程中为加快化学反应速率而采取的措施有研磨、70℃加热;故答案为:研磨、70℃加热;
(2)根据分析滤液1中加入NaOH调节pH=12沉淀Ni2+、Ca2+、Mg2+,故滤渣2主要为Ni(OH)2、Mg(OH)2还有极少量的Ca(OH)2;故答案为:Ni(OH)2、Mg(OH)2、Ca(OH)2;
(3)根据表可知Li2CO3的溶解度小在较高的温度下较小,故90℃充分反应后,通过趁热过滤分离出固体Li2CO3粗品;故答案为:趁热过滤;
(4)lkg含锂3.50%的废渣,锂的浸出率为a,则浸出的n(Li+)=![]() =5amol,Li+转化为Li2CO3的转化率为b,则粗品中含Li2CO3的质量是5amol×0.5×b×74g/mol=185ab g;故答案为:185ab;
=5amol,Li+转化为Li2CO3的转化率为b,则粗品中含Li2CO3的质量是5amol×0.5×b×74g/mol=185ab g;故答案为:185ab;
(5)根据电解图,阳极上发生氧化反应,氢氧根离子放电,电极反应为:4OH--4e-=2H2O+O2↑;阴极上放电的是氢离子,阴极生成OH-,根据题意得到LiOH,则LiOH在阴极生成,Li+移向阴极,故离子交换膜为阳离子交换膜;故答案为:4OH--4e-=2H2O+O2↑;阳;
(6)Li2CO3和C、FePO4高温下反应,生成LiFePO4和一种可燃性气体,根据元素分析该气体为CO,则反应为:![]() ;故答案为:
;故答案为:![]() 。
。


 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案科目:高中化学 来源: 题型:
【题目】2 mol A与2 mol B混合于2L的密闭容器中,发生如下反应:2A(g)+3B(g) ![]() 2C(g)+zD(g);若2 s后,A的转化率为50%,测得v(D)=0.25 mol·L-1·s-1,下列推断正确的是( )
2C(g)+zD(g);若2 s后,A的转化率为50%,测得v(D)=0.25 mol·L-1·s-1,下列推断正确的是( )
A.v(C)=v(D)=0.2 mol·L-1·s-1
B.z=3
C.B的转化率为75%
D.反应前与2 s后容器的压强比为4∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的转化在给定条件下能实现的是( )
A.MgCO3![]() MgCl2(aq)
MgCl2(aq) ![]() Mg
Mg
B.Cu2(OH)2CO3![]() CuO
CuO![]() Cu(OH)2
Cu(OH)2
C.BrCH2COOH![]() HOCH2COOH
HOCH2COOH![]() H-[OCH2CO]n-OH
H-[OCH2CO]n-OH
D.NH3![]() NO
NO![]() HNO3
HNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在2 L密闭容器中发生反应:A(g)+3B(g) === 2C(g) + 4D(g),测得5 min内,A的物质的量减小了10 mol,则5 min内该反应的化学反应速率是
A. υ(A) = 1 mol/(L·min)
B. υ(B) = 1 mol/(L·min)
C. υ(C) = 1 mol/(L·min)
D. υ(D) = 1 mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在l0℃时,10 mL 0.4 mol L-1H2O2溶液发生催化分解:2H2O2![]() 2H2O+O2↑,不同时刻测得生成O2的体积(已折算为标准状况)如下表:
2H2O+O2↑,不同时刻测得生成O2的体积(已折算为标准状况)如下表:
t/min | 0 | 2 | 4 | 6 |
V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 |
下列叙述不正确的是(溶液体积变化忽略不计)
A. 0~2 min的平均反应速率比4~6 min快
B. 0~6 min 的平均反应速率v(H2O2)=3.3×10-2 moL-1 L-1 min-1
C. 反应至 6 min 时,c(H2O2)=0.3 mol·L-1
D. 反应至6 min时,H2O2分解了50%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微信热传的“苯宝宝表情包”可看作是由苯衍生的物质配以相应文字形成的(如图)。下列说法正确的是

A. 化合物(A)不能与乙醇发生反应
B. 化合物(B)分子式为C6H6Cl6
C. 化合物(B)可通过苯与Cl2发生加成反应制得
D. 1mol化合物(A)可与3molH2发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组用0.50 mol·L-1 NaOH溶液和0.50 mol·L-1硫酸进行中和热的测定。
Ⅰ.配制0.50 mol·L-1 NaOH溶液
(1)若实验中大约要使用245 mL NaOH溶液,至少需要称量NaOH固体_____g。
(2)从下表中选择,称量NaOH固体所需要的仪器是(填字母)________。
名称 | 托盘天平(带砝码) | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
仪器 |
|
|
|
|
|
|
序号 | a | b | c | d | e | f |
Ⅱ.测定稀硫酸和稀氢氧化钠溶液中和热的实验装置如图所示。
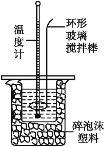
(1)若生成1 mol H2O时反应放出的热量为57.3 kJ,写出该反应的热化学方程式:__________。
(2)取50 mL NaOH溶液和30 mL硫酸进行实验,实验数据如下表。
①请填写下表中的空白:
实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | 温度差平均值(t2-t1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 30.1 | ______ |
2 | 27.0 | 27.4 | 27.2 | 33.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.8 | |
4 | 26.4 | 26.2 | 26.3 | 30.4 | |
②用上述实验数值计算结果为____kJmol-1,与57.3 kJmol-1有偏差,产生偏差的原因可能是_____(填字母)。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】表示下列反应的离子方程式正确的是
A.金属钠加入CuSO4溶液中:![]()
B.金属铝加入NaOH溶液中:![]()
C.铁粉加入FeC13溶液中:![]()
D.铜片插入浓HNO3溶液中:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,H2CO3的Ka1=4.2×10-7,Ka2=5.0×10-11。常温下在20mL0.1mol/LNa2CO3溶液中逐滴加入40mL0.1mol/L'HCl溶液,溶液中含碳元素的各种微粒(CO2因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如图所示。
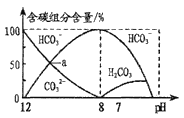
下列说法正确的是
A. 在同一溶液中,H2CO3、HCO3-、CO32-能大量共存
B. a点时:c(Na+)+c(H+)=c(OH-)+3c(CO32-)
C. 当pH=7时,溶液中c(Na+)=c(HCO3-)+2c(CO32-)
D. 当溶液中c(HCO3-):c(CO32-)=2:1时,溶液的pH=10
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com