
【题目】下列事实不能用勒夏特列原理解释的是( )
A.溴水中存在Br2+H2OHBr+HBrO,当加入硝酸银溶液并静置后,溶液颜色变浅
B.反应CO(g)+NO2(g)CO2(g)+NO(g)+Q,Q>0,平衡后,升高温度体系颜色变深
C.用饱和食盐水除去Cl2中的HCl
D.合成氨反应中,为提高原料的转化率,可采用高温加热的条件
【答案】D
【解析】
A. 溴水中有下列平衡:Br2+H2O ![]() HBr+HBrO,当加入AgNO3(s)后,硝酸银与溴离子反应生成溴化银沉淀,平衡正向移动,溶液颜色变浅,能用勒夏特列原理解释,故A不选;
HBr+HBrO,当加入AgNO3(s)后,硝酸银与溴离子反应生成溴化银沉淀,平衡正向移动,溶液颜色变浅,能用勒夏特列原理解释,故A不选;
B. 反应CO(g)+NO2(g)CO2(g)+NO(g)+Q,Q>0,正反应放热,升高温度,平衡逆向移动,能用勒夏特列原理解释,故C不选;
C. 增大氯离子的浓度,平衡Cl2+H2O=H++Cl-+HClO逆向移动使得氯气难溶于饱和食盐水,能用勒夏特列原理解释,故C不选;
D. 合成氨反应是放热反应,升高温度,反应逆向移动,原料的转化率减小,不能通过升高温度提高原料的转化率,故D选;
正确答案是D。


科目:高中化学 来源: 题型:
【题目】(1)1mol氢气在氯气中充分燃烧生成氯化氢气体时放出184.6 kJ的热量,试写出对应的热化学方程式___________________。标准状况下11.2L氢气在氯气中充分燃烧放出的热量是______kJ。
(2)A(g)+B(g)![]() C(g)+D(g)过程中的能量(kJ)变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量(kJ)变化如图所示,回答下列问题。
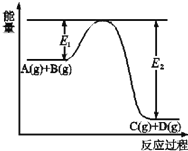
①反应物A(g)和B(g)具有的总能量_______(填大于、小于、等于)生成物C(g)和D(g)具有的总能量。
②该反应是_______反应(填吸热、放热),△H=_____(用E1和E2表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘与氢气在一定条件下反应的热化学方程式如下:
(Ⅰ)I2(g)+H2(g)![]() 2HI(g) ΔH=-9.48 kJ·mol-1
2HI(g) ΔH=-9.48 kJ·mol-1
(Ⅱ)I2(s)+H2(g)![]() 2HI(g) ΔH=+26.48 kJ·mol-1
2HI(g) ΔH=+26.48 kJ·mol-1
下列判断正确的是( )
A. 在一定条件下将2 g H2(g)通入254 g I2(g)中,该过程放出的热量为9.48 kJ
B. 1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ
C. 反应(Ⅰ)的产物比反应(Ⅱ)的产物稳定
D. 物质的量相同时,反应(Ⅰ)的反应物总能量比反应(Ⅱ)的反应物总能量高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A+B![]() C(ΔH < 0)分两步进行:①A+B
C(ΔH < 0)分两步进行:①A+B![]() X(ΔH>0); ②X
X(ΔH>0); ②X![]() C(ΔH<0)。下列示意图中,能正确表示总反应过程中能量变化的是( )。
C(ΔH<0)。下列示意图中,能正确表示总反应过程中能量变化的是( )。
A.
B.
C.
D.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应C2H6(g)![]() C2H4(g)+H2(g) △H>0,在一定条件下于密闭容器中达到平衡。下列各项措施中,不能提高乙烷平衡转化率的是( )
C2H4(g)+H2(g) △H>0,在一定条件下于密闭容器中达到平衡。下列各项措施中,不能提高乙烷平衡转化率的是( )
A.增大容器容积B.升高反应温度
C.恒容下通入乙烷D.恒容下通入惰性气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Fe3O4是一种黑色粉末,又称磁性氧化铁,它的组成可写成FeO·Fe2O3。某化学实验小组通过实验来探究一黑色粉末是否由Fe3O4、CuO组成(不含有其它黑色物质)。探究过程如下:
Ⅰ.提出假设: 假设1.黑色粉末是CuO;假设2.黑色粉末是Fe3O4;
假设3.黑色粉未是CuO和Fe3O4的混合物
Ⅱ.设计探究实验:
方案一:取少量粉末加入足量稀硝酸,若假设2或假设3成立则实验现象是___________,相关反应的离子方程式为__________________________________。
方案二: 查阅资料: Cu2+与足量氨水反应生成深蓝色溶液,Cu2++4NH3·H2O=Cu(NH3)42++4H2O。为探究是假设2还是假设3成立,另取少量粉末加稀硫酸充分溶解后,再加入足量氨水,若产生___________现象,则假设2成立;若产生___________现象,则假设3成立。
方案三:
学生丙利用下图所示装置进行实验,称量反应前后装置C中样品的质量,以确定样品的组成。回答下列问题:
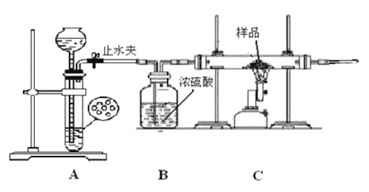
(1)下列实验步骤的先后顺序是___________(填序号)。
①打开止水夹;②关闭止水夹;③点燃C处的酒精喷灯;
④熄灭C处的酒精喷灯 ⑤收集氢气并验纯。
在点燃C处酒精喷灯前要进行的必要操作是__________________________。
(2)假设样品全部参加反应,若实验前样品的质量为4.7克,实验后称得装置C中固体的质量3.6克则假设___________(填“1”“2”或“3”) 正确。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化铜和氯化亚铜都是重要的化原料,常用作石油工业脱臭脱硫和纯化剂、印染媒染剂等。某研究小组用粗铜(含杂质Fe)为原料制备CuCl2·2H2O晶体,再用CuCl2·2H2O晶体制各CuCl。
[制备CuCl2·2H2O晶体]

(1)仪器B的名称是________________;B中反应的离子方程式为_______________________________。
(2)装置C中粗铜粉末与气体充分反应时的生成物是______________________(填化学式)。反应完成后,将C中的固体用稀盐酸完全溶解、再加入试剂M除杂,经一系列操作便可获得CuCl2·2H2O晶体。
①试剂M应当选用___________(填正确答案字母编号)
a.Cu(NO3)2 b.NaOH c.CuO d.NH3·H2O e.Cu(OH)2
②溶解C中生成物固体时,有时会加入少量双氧水,目的是____________________。
③设计简易实验方案确定所CuCl2·2H2O晶体中不含铁化合物:________________________。
[制备CuCl固体]
将CuCl2·2H2O晶体在HCl气流中加热到140℃得无水CuCl2,再加热到300℃以上可获得CuCl固体。
(3)将CuCl2·2H2O晶体在HCl气流中加热脱水的原因是__________________。
(4)为测定CuCl固体的产率,进行如下定量分析:
①将10.26gCuCl2·2H2O晶体先加热到140℃,再加热到300℃以上,充分反应后,将所得固休平均三份,分别转移至三个锥形瓶中。
②分别在三个锥形瓶中加过量FeCl3溶液不断振荡,使固体迅速溶解,再加入2滴1,10—邻菲啰啉一硫酸亚铁络合物作指示剂。
③用1.00mol/L的硫酸铈[Ce(SO4)2]标准液进行滴定。平行测定三份样品溶液,消耗硫酸铈[Ce(SO4)2]标准溶液的平均体积为19.40mL。
反应原理:CuCl+FeCl3=CuCl2+FeCl2,Fe2++Ce4+=Ce3++Fe3+
根据上述定量实验计算CuCl的产率为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是
A. 有机物![]() 属于芳香烃,含有两种官能团
属于芳香烃,含有两种官能团
B. 按系统命名法,化合物![]() 的名称为2,4,6-三甲基-5-乙基庚烷
的名称为2,4,6-三甲基-5-乙基庚烷
C. 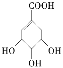 既属于醇类又属于羧酸
既属于醇类又属于羧酸
D. 2-甲基-3-丁烯的命名错误原因是选错了主链
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是一种分子式为C4H8O2的有机物的红外光谱图,则该有机物可能为
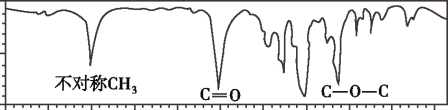
A.CH3COOCH2CH3B.CH3CH2COOH
C.HCOOCH2CH2CH3D.(CH3)2CHCH2COOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com