
【题目】理论上不能设计为原电池的化学反应是,注:△H<0为放热反应
A.CH4(g)+2O2(g)![]() CO2(g)+2H2O(l);△H<0
CO2(g)+2H2O(l);△H<0
B.HNO3(aq)+NaOH(aq)=NaNO3(aq)+H2O(aq);△H<0
C.2H2(g)+O2(g)![]() 2H2O(g);△H<0
2H2O(g);△H<0
D.2FeCl3(l)+Fe(s)==3FeCl2(l);△H<0
【答案】B
【解析】
A.CH4(g)+2O2(g)![]() CO2(g)+2H2O(l) △H<0是自发进行的放热的氧化还原反应,能设计成甲烷燃料电池,故A错误;
CO2(g)+2H2O(l) △H<0是自发进行的放热的氧化还原反应,能设计成甲烷燃料电池,故A错误;
B.HNO3(aq)+NaOH(aq)=NaNO3(aq)+H2O(aq) △H<0中各元素化合价不变,没有电子转移,不是氧化还原反应,则不能设计成原电池,故B正确;
C.2H2(g)+O2(g)![]() 2H2O(g) △H<0是自发进行的放热的氧化还原反应,能设计成氢氧燃料电池,故C错误;
2H2O(g) △H<0是自发进行的放热的氧化还原反应,能设计成氢氧燃料电池,故C错误;
D.2FeCl3(l)+Fe(s)==3FeCl2(l) △H<0是自发进行的放热的氧化还原反应,能设计成原电池,Fe作负极,电解质溶液为氯化铁溶液,故D错误;
故答案为B。


 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案科目:高中化学 来源: 题型:
【题目】某化学兴趣小组的同学用如图所示装置研究有关电化学的问题。当闭合该装置的开关时,观察到电流表的指针发生了偏转。请根据如图所示,回答下列问题:
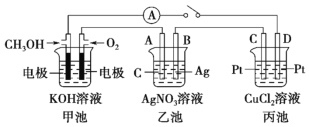
(1)甲池为_____(填“原电池”“电解池”或“电镀池”),通入 CH3OH 电极的电极反应为_____。
(2)乙池中 A(石墨)电极的名称为_____(填“正极”“负极”或“阴极”“阳极”),总反应化学方程式为__________。
(3)当乙池中 B 极质量增加 5.4 g 时,甲池中理论上消耗 O2 的体积为_____mL(标准状况),丙池中_____(填“C”或“D”)极析出_____g 铜。
(4)若丙中电极不变,将其溶液换成 NaCl 溶液,开关闭合一段时间后,甲中溶液的 pH将_____(填“增大”“减小”或“不变”,下同),丙中溶液的 pH 将______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能证明硅酸的酸性弱于碳酸酸性的实验事实是( )
A.CO2溶于水形成碳酸,SiO2难溶于水
B.CO2通入可溶性硅酸盐中析出硅酸沉淀
C.高温下SiO2与碳酸盐反应生成CO2
D.HCl通入可溶性碳酸盐溶液中放出气体,氯化氢通入可溶性硅酸盐溶液中生成沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知以下物质为铁及其化合物之间的相互转化:

试回答:
(1)写出D的化学式___,H的化学式___。
(2)鉴别G溶液的试剂为___。
(3)写出由E转变成F的化学方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸铁铵[NH4Fe(SO4)2·xH2O]是一种重要铁盐。为充分利用资源,变废为宝,在实验室中探究采用废铁屑来制备硫酸铁铵,具体流程如下:

回答下列问题:
(1)步骤①的目的是去除废铁屑表面的油污,方法是_________________。
(2)步骤②需要加热的目的是_________________,温度保持80~95 ℃,采用的合适加热方式是_________________。铁屑中含有少量硫化物,反应产生的气体需要净化处理,合适的装置为_________________(填标号)。

(3)步骤③中选用足量的H2O2,理由是_________________。分批加入H2O2,同时为了_________________,溶液要保持pH小于0.5。
(4)步骤⑤的具体实验操作有______________,经干燥得到硫酸铁铵晶体样品。
(5)采用热重分析法测定硫酸铁铵晶体样品所含结晶水数,将样品加热到150 ℃时,失掉1.5个结晶水,失重5.6%。硫酸铁铵晶体的化学式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】茅台酒中存在少量具有凤梨香味的物质X,其结构如图所示。下列说法正确的是

A. X难溶于乙醇
B. 酒中的少量丁酸能抑制X的水解
C. 分子式为C4H8O2且官能团与X相同的物质有5种
D. X完全燃烧后生成CO2和H2O的物质的量比为1∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁电池是一种新型可充电电池,与普通高能电池相比,该电池可长时间保持稳定的放电电压。高铁电池的总反应为3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是( )
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是( )
A.放电时负极反应为Zn-2e-+2OH-=Zn(OH)2
B.充电时阳极反应为Fe(OH)3-3e-+5OH-=FeO![]() +4H2O
+4H2O
C.放电时每转移3 mol电子,正极有1 mol K2FeO4被氧化
D.放电时正极附近溶液的碱性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验设计正确的是( )
操作 | 现象 | 结论 | |
A | 将SO2通入溴水 | 溴水褪色 | SO2具有漂白性 |
B | 将乙烯通入酸性KMnO4溶液 | 酸性KMnO4溶液褪色 | 乙烯具有还原性 |
C | 将澄清石灰水滴入某溶液 | 出现白色浑浊 | 其溶液中存在CO32- |
D | 将硝酸银溶液滴入某溶液 | 出现白色沉淀 | 其溶液中存在Cl- |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯水中含有多种成分,因而具有多种性质,根据新制氯水分别与如图四种物质发生的反应填空(a、b、c、d、e中重合部分代表物质间反应,且氯水足量)。
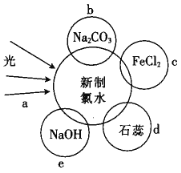
(1)氯水中含有的粒子有![]() 、
、![]() 、______、
、______、![]() 、
、![]() 、______、
、______、![]() 七种。
七种。
(2)久置的氯水变为_____________,原因是___________________________(用化学反应方程式表示)。
(3)b过程中的离子方程式是_______________________。
(4)e过程中所发生的主要反应的化学方程式为____________________________。
(5)能证明氯水具有漂白性的是______________________(填“a”“b”“c”或“d”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com