
【题目】将某植物的叶肉细胞链于适宜沮度和充足的14CO2条件下,先给予一段时间光照,然后再停止光照,检测整个过程叶肉细胞的叶绿体中放射性C3浓度的变化情况,结果如下图.回答下列问题。
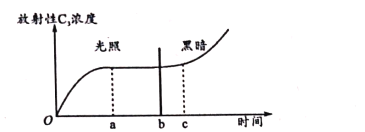
(1)叶肉细胞以14CO2为原料,生成C3的场所是____。图中a~b段放射性C3浓度基本不变,原因是____。
(2)图示结果显示,停止光照后的b~c时间段内,叶肉细胞中放射性C3的浓度并没有上升,原因是____。
(3)某实验小组对叶肉细胞交替进行光照和黑暗处理(先光照后黑暗,每次光照与黑暗处理的时间相同;各组光照强度和处理的总时间也相同),随着光照和黑暗交替频率的增加,推测叶肉细胞光合作用中CO2的同化总量最可能____(填增加或减少或不变),原因是____。
【答案】叶绿体基质 固定生成的速率与还原的速率相等 叶绿体基质中还有光反应产生的ATP和[H],还能维持较短时间的还原反应 增加 光反应产生的ATP和[H]能及时利用和再生
【解析】
光合作用分为两个阶段进行,在这两个阶段中,第一阶段是直接需要光的称为光反应,第二阶段不需要光直接参加,是二氧化碳转变为糖的反过程称为暗反应。光合作用在叶绿体中进行,光反应的场所位于类囊体膜,暗反应的场所在叶绿体基质。光反应的发生需要叶绿体类囊体膜上的色素、酶参与。
(1)14CO2与C5在叶绿体基质中生成C3。图中a~b段放射性C3浓度基本不变,原因是固定生成的速率与还原的速率相等。
(2)图示结果显示,停止光照后的b~c时间段内,叶绿体基质中还有光反应产生的ATP和[H],还能维持较短时间的还原反应,因此叶肉细胞中放射性C3的浓度并没有上升。
(3)随着光照和黑暗交替频率的增加,光反应产生的ATP和[H]能及时利用和再生,故叶肉细胞光合作用中CO2的同化总量最可能增加。


科目:高中化学 来源: 题型:
【题目】从粉煤灰(含莫来石、石英等)中回收![]() 的一种工艺流程如下:
的一种工艺流程如下:
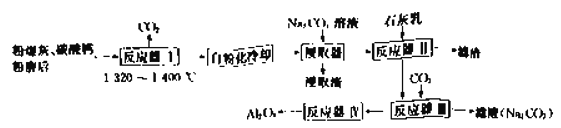
(1)经反应器I可使莫来石和石英转化为![]() (硅酸二钙)和______________(七铝十二钙,填化学式),从而使其中的
(硅酸二钙)和______________(七铝十二钙,填化学式),从而使其中的![]() 得到活化。
得到活化。
(2)控制条件,经反应器I烧结后固体自身不需要机械加工即可变成粉末,“自粉化”的意义是_______。
(3)浸取器中,适量增大![]() 溶液的投料,有利于提高铝酸钙转化为
溶液的投料,有利于提高铝酸钙转化为![]() 的产率,其原因是_______________________________________;同时有少量硅进入浸取渣,硅的存在形式是________________________________(填化学式)。
的产率,其原因是_______________________________________;同时有少量硅进入浸取渣,硅的存在形式是________________________________(填化学式)。
(4)反应器Ⅲ中发生反应的离子方程式为:__________________________________。
(5)反应器Ⅳ采取工艺方法是_____________________;上述工艺流程中可以循环使用的物质是_______________________________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硒是动物和人体所必需的微量元素之一,也是一种重要的工业原料。硒在自然界中稀少而分散,常从精炼铜的阳极泥中提取硒。
(1)粗铜精炼时,通常用精铜作_______极(填“阴”或“阳”)。
(2)Se与S处于同一主族,比S原子多1个电子层,Se的原子序数为____________;其最高价氧化物的化学式为________;该族 2~5周期元素单质分别与H2反应生成1 mol气态氢化物的反应热如下:
a.+99.7 kJmol1 b.+29.7 kJmol1 c.-20.6 kJmol1 d.-241.8 kJmol1
表示生成 1 mol硒化氢反应热的是________________(填字母代号)。
(3)阳极泥中的硒主要以Se和CuSe的形式存在,工业上常用硫酸化焙烧法提取硒,主要步骤如下:
i.将含硒阳极泥与浓硫酸混合焙烧,产生SO2、SeO2的混合气体
ii.用水吸收i中混合气体,可得Se固体
① 请写出CuSe与浓H2SO4反应的化学方程式___________。
② 焙烧过程产生的烟气中含有少量SeO2,可用NaOH溶液吸收,二者反应生成一种盐,该盐的化学式为_________。
③ 写出步骤ⅱ中的化学方程式______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“质量摩尔浓度”也是一种表示溶液组成的物理量,溶质B的质量摩尔浓度是用单位质量的溶剂中所含溶质B的物质的量来表示溶液组成的物理量,单位为molkg-1或molg-1,已知20°C时质量分数为20%的NaOH溶液的密度为1.16 gcm-3,则该溶液的质量摩尔浓度为
A.6.25 molkg-1B.4.25 molkg-1C.6.25 molg-1D.4.25 molg-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学—选修3:物质结构与性质](15分)A、B、C、D为原子序数依次增大的四种元索,A2-和B+具有相同的电子构型;C、 D为同周期元索,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。回答下列问题:
(1)四种元素中电负性最大的是 (填元素符号),其中C原子的核外电子排布式为__________。
(2)单质A有两种同素异形体,其中沸点高的是 (填分子式),原因是 ;A和B的氢化物所属的晶体类型分别为 和 。
(3)C和D反应可生成组成比为1:3的化合物E, E的立体构型为 ,中心原子的杂化轨道类型为 。
(4)化合物D2A的立体构型为 ,中心原子的价层电子对数为 ,单质D与湿润的Na2CO3反应可制备D2A,其化学方程式为 。
(5)A和B能够形成化合物F,其晶胞结构如图所示,晶胞参数,a=0.566nm, F 的化学式为 :晶胞中A 原子的配位数为 ;列式计算晶体F的密度(g.cm-3) 。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图中甲、乙、丙表示某动物细胞中的不同化合物,下列叙述正确的是( )

A. 核糖核苷酸是构成物质甲的基本单位
B. 物质甲为该生物的主要遗传物质
C. 物质丙是构成细胞的基本骨架
D. 物质乙的种类和数量与细胞膜的功能密切相关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人体血液里Ca2+的浓度一般采用mg/cm3来表示。抽取一定体积的血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(H2C2O4),再用KMnO4溶液滴定即可测定血液样品中Ca2+的浓度。某研究性学习小组设计如下实验步骤测定血液样品中Ca2+的浓度。
(配制KMnO4标准溶液)如图是配制50 mL KMnO4标准溶液的过程示意图。
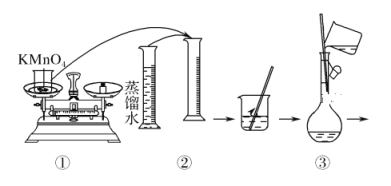
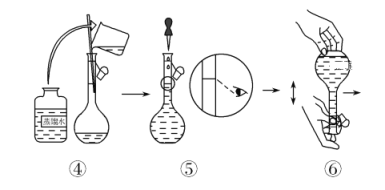
(1)请你观察图示判断,其中不正确的操作有(填序号)________。
(2)其中确定50 mL溶液体积的容器是(填名称)________。
(3)如果用图示的操作配制溶液,所配制的溶液浓度将________(填“偏大”或“偏小”)。
(测定血液样品中Ca2+的浓度)抽取血样20.00 mL,经过上述处理后得到草酸,再用0.020 mol/L KMnO4溶液滴定,使草酸转化成CO2逸出,这时共消耗12.00 mL KMnO4溶液。
(4)已知草酸跟KMnO4溶液反应的离子方程式为:
2MnO4-+5H2C2O4+6H+===2Mnx++10CO2↑+8H2O则方程式中的x=________。
(5)经过计算,血液样品中Ca2+的浓度为________mg/cm3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)在______ molAl2(SO4)3中含0.3molSO42- ,含Al3+约_______________个。
(2)标况下,11.2LNH3的质量为:____________g。
(3)20g某二价金属氯化物(ACl2)中含有0.4mol Cl-,则ACl2的摩尔质量是_________。
(4)在100mLFe2(SO4)3溶液中含Fe3+11.2 g,则溶液中Fe3+浓度____________,取该溶液25ml加水稀释至300mL,则此时稀溶液中SO42﹣的物质的量浓度为____________。
(5)在标况下,22.4L由氮气和氧气组成的混合气体,其质量为30g,则氧气的质量为______g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请回答下列问题
(1)配平化学方程式。__FeCl3+__SO2+__H2O=__FeCl2+__H2SO4+__HCl。
(2)除去括号中的杂质,写出除杂反应的离子方程式
①Na2SO4溶液(Na2CO3):_______________________________________________。
②Ca(NO3)2溶液(CaCl2):_______________________________________________。
(3)写出下列反应的离子方程式:
①向烧碱溶液中通入少量CO2气体:_______________________________________________。
②向澄清石灰水中滴加足量的碳酸氢钠溶液:_______________________________________________。
(4)实验室中,制取Fe(OH)3胶体的离子方程式是_______________________________________________,
证明胶体已经制成的方法是_______________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com