
【题目】(1) 写出CO2的空间构型:___________。
(2) 写出Na3N的电子式:____________________。
(3) 写出C2H6O的化学名称:______________________。
(4) 写出乙烯的实验式:_________________。
【答案】直线形 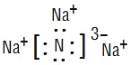 乙醇或二甲醚 CH2
乙醇或二甲醚 CH2
【解析】
(1) CO2分子的结构式为O=C=O,中心原子碳的最外层没有孤对电子,三个原子位于一条直线上;
(2) Na3N由Na+和N3-通过离子键相结合;
(3) C2H6O的分子结构可能是CH3CH2OH,也可能是CH3OCH3;
(4)乙烯的分子式为C2H4,实验式就是最简式。
(1) CO2的结构式为O=C=O,中心原子碳的最外层没有孤对电子,三个原子位于一条直线上,则其空间构型为直线形;答案为:直线形;
(2) Na3N由Na+和N3-通过离子键相结合,则其电子式为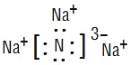 ;答案为:
;答案为: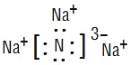 ;
;
(3) C2H6O的分子结构可能是CH3CH2OH,也可能是CH3OCH3;化学名称为乙醇或二甲醚;答案为:乙醇或二甲醚;
(4) 乙烯的分子式为C2H4,实验式就是最简式,则其实验式为CH2;答案为:CH2。


科目:高中化学 来源: 题型:
【题目】实验室采用下图所示装置制备乙酸乙酯。实验结束后,取下盛有饱和碳酸钠溶液的试管,再沿该试管内壁缓缓加入石蕊溶液1毫升,发现石蕊溶液存在于饱和碳酸钠溶液层与乙酸乙酯液层之间(整个过程不振荡试管)。下列有关该实验的描述不正确的是( )
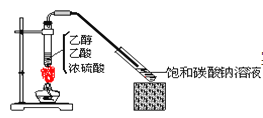
A.制备的乙酸乙酯中混有乙酸和乙醇杂质
B.该实验中浓硫酸的作用是催化和吸水
C.饱和碳酸钠溶液主要作用是降低乙酸乙酯的溶解度及吸收乙醇和乙酸
D.石蕊层为三层,由上而下是蓝、紫、红
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是含某元素的A→G的七种物质分别与X、Y、Z反应的价类二维图。其中X是一种强碱;G为正盐;通常条件下,Z是无色液体;D的相对分子质量比C小16,各物质转化关系如图所示。下列说法正确的是![]()
![]()

A.该元素在周期表中位于第二周期第V族
B.上述转化中发生5个氧化还原反应
C.稳定性:气态F<气态Z
D.A、B、X、G四种物质分别含有离子键和共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温时,将0.1 mol Fe(NO3)3和2 mol HCl溶于水得到2L混合溶液,然后向该溶液中投入m g铁粉,充分反应后,滴加KSCN溶液不变红色。下列有关说法正确的是
A.由于氧化性:Fe3+>H+,故首先发生的反应是Fe+2Fe3+=3Fe2+
B.充分反应后,共消耗56 g铁
C.m=28时,溶液剩余0.9 mol H+
D.当加入16.8 g铁粉时,可生成标准状况下6.72 L气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌铜原电池装置如图所示,下列说法不正确的是

A.电子从锌片流向铜片
B.盐桥中 K+向负极移动
C.锌电极上发生的反应:Zn 2e- =Zn2+
D.该装置实现了氧化反应和还原反应分开进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH4-CO2催化重整可以得到合成气(CO和H2),有利于减小温室效应,其主要反应为CH4(g)+CO2(g)2CO(g)+2H2(g) ΔH=+247 kJ·mol1,同时存在以下反应:积碳反应:CH4(g)C(s)+2H2(g) ΔH=+75 kJ·mol1,消碳反应:CO2(g)+C(s)2CO(g) ΔH=+172 kJ·mol1,积碳会影响催化剂的活性,一定时间内积碳量和反应温度的关系如图。下列说法正确的是

A.高压利于提高 CH4 的平衡转化率并减少积碳
B.增大CO2与CH4的物质的量之比有助于减少积碳
C.升高温度,积碳反应的化学平衡常数K减小,消碳反应的K增大
D.温度高于600℃,积碳反应的化学反应速率减慢,消碳反应的化学反应速率加快, 积碳量减少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求,写出下列反应的化学方程式(电解池中的电极均为惰性电极):
(1) 锌铜原电池(稀硫酸作电解质溶液)的电池反应____________________________________________
(2) 甲醇-空气电池(KOH溶液作电解质溶液)的总反应_______________________________________
(3) 电解硫酸铜溶液的总反应_____________________________________________________________
(4) 电解饱和食盐水(氯碱工业)的总反应____________________________________________________
(5) 实验室制氨气_______________________________________________________________________
(6)工业合成氨_________________________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,盐酸只作氧化剂的是( )
A.Zn+2HCl = ZnCl2+H2↑B.MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
C.Cl2+H2O = H++Cl–+HClOD.CaCO3+2HCl=CaCl2+CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上先将煤转化为CO,再利用CO和水蒸气反应制H2时,存在以下平衡:CO(g)+H2O(g)CO2(g)+H2(g)。
(1)平衡常数的表达式K=_________________________
(2)向1L恒容密闭容器中充入CO和H2O(g),某温度时测得部分数据如下表。
t/min | 0 | 1 | 2 | 3 | 4 |
n(H2O)/mol | 1.20 | 1.04 | 0.90 | 0.70 | 0.70 |
n(CO)/mol | 0.80 | 0.64 | 0.50 | 0.30 | 0.30 |
则从反应开始到2min时,用H2表示的反应速率为__________;该温度下反应的平衡常数K=________(小数点后保留2位有效数字)。
(3)已知该反应在不同的温度下的平衡常数数值分别为
t/℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 1.67 | 1.19 | 1.00 | 0.60 | 0.38 |
①根据表中的数据判断,该反应为________(填“吸热”或“放热”)反应。
②800℃,向2L恒容密闭容器中充入1molCO(g)、1molH2O(g)、2molCO2(g)、2molH2(g),此时v正_______v逆 (填“>”“<”或“=”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com