
����Ŀ���Ը��������Ҫ�ɷ�ΪFe(CrO2)2������Al2O3��Fe2O3��SiO2�����ʣ�Ϊ��Ҫԭ�������ظ����ƾ��壨Na2Cr2O7��2H2O������Ҫ����������ͼ��
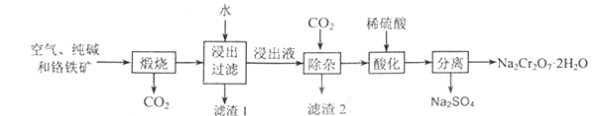
��1�����չ����У��������е�Al2O3�봿�Ӧ�Ļ�ѧ����ʽΪ��____��
��2������1�ijɷ�Ϊ_____������2�ijɷ�Ϊ_____��
��3���ù�����ij�ֲ�����������ã������ʵĻ�ѧʽΪ��_____��
��4���ữʱ�����ķ�ӦΪ��2CrO42-+2H+![]() Cr2O72-+H2O����1L�ữ��������Һ�к���Ԫ�ص�����Ϊ28.6g��CrO42-��
Cr2O72-+H2O����1L�ữ��������Һ�к���Ԫ�ص�����Ϊ28.6g��CrO42-��![]() ת��ΪCr2O72-��
ת��ΪCr2O72-��
���ữʱ������Ӧ��ƽ�ⳣ���ı���ʽΪK=_____��
���ữ��������Һ��c(Cr2O72-)=____��
��3�������йع��ұ�����CrO42-�ķ�ˮҪ����ѧ������ʹ��Ũ�Ƚ���5.0��10-7mol��L-1���²����ŷš���CrO42-�ķ�ˮ����ͨ�����������ַ�����
�ٳ���������������Ա�������BaCrO4������Ksp(BaCrO4)=1.2��10-10�ݣ��ټ�������������δ��������Ba2+����������Ա��κ�ķ�ˮ��Ba2+��Ũ��Ӧ��С��____mol��L-1��������ˮ�������ܴﵽ�����ŷű���
�ڻ�ԭ����CrO42-![]() Cr3+
Cr3+![]() Cr(OH)3��д������������CrO42-���̷���Ӧ�����ӷ���ʽ____��
Cr(OH)3��д������������CrO42-���̷���Ӧ�����ӷ���ʽ____��
���𰸡�Al2O3+Na2CO3![]() 2NaAlO2+CO2�� Fe2O3 H2SiO3��Al(OH)3 CO2
2NaAlO2+CO2�� Fe2O3 H2SiO3��Al(OH)3 CO2 ![]() 0.25mol��L-1 2.4��10-4
0.25mol��L-1 2.4��10-4 ![]()
��������
������[��Ҫ�ɷ�ΪFe(CrO2)2������Al2O3��Fe2O3��SiO2������]���������������ڸ�����������������Fe2O3��Na2CrO4��NaAlO2��Na2SiO3��CO2������ˮ��������ʱ��Fe2O3������ˮ������������Һ��ͨ��CO2�����ɲ�����ˮ��H2SiO3��Al(OH)3����Һ����Ҫ�ɷ�ΪNa2CrO4��̼������(��̼����)������ϡ�����Na2CrO4ת��ΪNa2Cr2O7��̼������(��̼����)ת��Ϊ�����ƣ�Ȼ������õ�Na2Cr2O7��2H2O���Դ˽���⡣
��1����������ͼ��֪�����չ����У��������е�Al2O3�봿�Ӧ������CO2��Ȼ������Ԫ���غ���ƽ���û�ѧ����ʽΪ��Al2O3+Na2CO3![]() 2NaAlO2+CO2����
2NaAlO2+CO2����
��2��������������֪������1ΪFe2O3������2ΪH2SiO3��Al(OH)3��
��3��������ͼ��֪����ѭ�����õ�����ΪCO2��
��4���ٸ���ƽ�ⳣ�����壺���滯ѧ��Ӧ�ﵽƽ��״̬ʱ�������뷴Ӧ���Ũ�ȣ�����ʽϵ���ݴη����˻��Ȼ�Ӧ�����뷴Ӧ�����Ũ�ȣ�����ʽϵ���ݴη����˻��ȿ�֪���÷�Ӧƽ�ⳣ��Ϊ��![]() ��
��
����1L�ữ��������Һ�к���Ԫ�ص�����Ϊ28.6g��![]() ��
��![]() ת��Ϊ
ת��Ϊ![]() ��˵����Ԫ����
��˵����Ԫ����![]() ת��Ϊ
ת��Ϊ![]() �������غ��й�ϵʽ��
�������غ��й�ϵʽ��
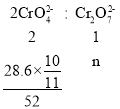
��n=0.25mol��n(![]() )ʣ��=0.05mol������ữ��������Һ��c(
)ʣ��=0.05mol������ữ��������Һ��c(![]() )=
)=![]() =0.25molL-1��
=0.25molL-1��
��3����![]() =5��10-7��c(Ba2+)=1.2��10-10�����c(Ba2+)=2.4��10-4mol/L��
=5��10-7��c(Ba2+)=1.2��10-10�����c(Ba2+)=2.4��10-4mol/L��
������������![]() ���������ӷ�Ӧ����Cr3+��Fe3+��ˮ������������ԭ��Ӧ��ʧ�����غ㡢����غ��Լ�ԭ���غ��֪�䷴Ӧ�����ӷ���ʽΪ��
���������ӷ�Ӧ����Cr3+��Fe3+��ˮ������������ԭ��Ӧ��ʧ�����غ㡢����غ��Լ�ԭ���غ��֪�䷴Ӧ�����ӷ���ʽΪ��![]() ��
��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ȳ(C2H2)�����ȼ����Ϊ��H����1299.6kJ��mol-1���ֱ�д����ʾ��Ȳȼ�շ�Ӧ���Ȼ�ѧ����ʽ�ͱ�ʾ��Ȳȼ���ȵ��Ȼ�ѧ����ʽ____��____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������±��X2�뱽��ͬϵ��ķ�Ӧ��±������ɽ������Ʒ�Ӧ��������ױ��������ķ�Ӧ�����ǵķ�Ӧ�������м��壨����һ�����м��壨��Ϊ��ɫ���壬�۵㣭15�棬�����ɸ�����BF4����һ����Ԫ������������ɵģ��������������ƽ�������ڳ���*��̼ԭ�������������ɻ���̼ԭ���ϣ���ͼ�������ߡ�
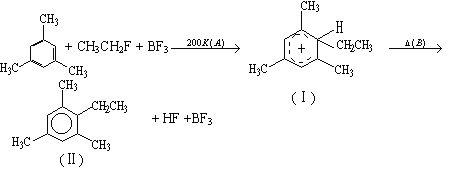
��1���ӷ�Ӧ���Ϳ�����ӦA����___����ӦB����___��ȫ��������___��
��2���м��壨���л�*�ŵ�̼ԭ�ӵ����幹�������л������л�*��̼ԭ�ӽӽ�������_____��
A��*CH��CH B��CH3*CH2CH3 C��![]() D��
D��![]()
��3��ģ�����⣬������з�Ӧ������д�м��壬�����Ƿ�Ӧ��������Ҫ����ƽ����
��![]() +
+![]() ��___
��___
��![]() ��������+CHCl3 ��___
��������+CHCl3 ��___
��![]() + ��
+ ��![]() +HBr___
+HBr___
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������£���������ķ�����һ����ȵ���
A.ͬ��������ͬ�ܶȵ�N2��C3H6��B.ͬ�¶ȡ�ͬ�����O2��N2��
C.ͬ�����ͬ�ܶȵ�CO��C2H4��D.ͬѹǿ��ͬ�����O2��N2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���¶���ͬ����ס����������ͬ���ܱ������У���ͨ��2mol SO2��1 mol O2������Ӧ��
2SO2(g)+O2(g) ![]() 2SO3(g)�ﵽƽ��ʱ����������SO2��ת���ʴ�����������SO2��ת���ʡ������ж���ȷ���� ( )
2SO3(g)�ﵽƽ��ʱ����������SO2��ת���ʴ�����������SO2��ת���ʡ������ж���ȷ���� ( )
A.�ױ���ѹǿ���䣬�ұ����������
B.�ױ���������䣬�ұ���ѹǿ����
C.��������ܶȼ�С����
D.��������ƽ����Է���������С����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����С����ͼ��ʾ�������Ҵ��Ĵ�����ʵ�飬�Թ�A��ʢ����ˮ�Ҵ���B��װ��Cu��CuO����ʯ���������壩��C��װ���dz���ʯ��ˮ����ش��������⣺

��1�����Թ�A�й��������Ŀ���ǣ�___��
��2���ձ���ˮ�������ǣ�___��
��3��������B�й۲쵽����������ɺڱ�죬ԭ���ǣ����û�ѧ����ʽ���ͣ���___��
��4����ʵ������У��Թ�C�ĵ��ܿ�������ð������Һ���ݳ����������Ҫ�ɷ���___��ʵ������Թ�C����Һ�м�������Cu��OH��2����Һ�����ȣ������ǣ�___��
��5��д���Ҵ������������Ļ�ѧ��Ӧ����ʽ��___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͭ�ǹ㷺Ӧ�������������Ԫ�������úϽ�ij����С���ij�Ͼ���ͭԪ��(��25%BeO��71%CuS������FeS��SiO2)�л������ͭ���ֽ����Ĺ���������ͼ��
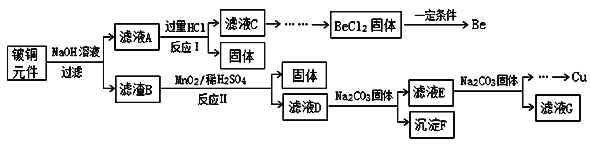
��֪��I���롢��Ԫ�ػ�ѧ�������ƣ�
�����²�����������ܶȻ����������
������ | Cu(OH)2 | Fe(OH)3 | Mn(OH)2 |
�ܶȻ�����(Ksp) | 2.2��10��20 | 4.0��10��38 | 2.1��10��13 |
(1)��ҺA����Ҫ�ɷֳ�NaOH��Na2BeO2�⣬����___________(�ѧʽ)��д����ӦI��Na2BeO2��������ᷴӦ�����ӷ���ʽ��________��
(2)��ҺC�к�NaCl��BeCl2������HCl��Ϊ�ᴿBeCl2���������ʵ�鲽��˳��Ϊ_______(����ĸ)
a.��������İ�ˮ b.ͨ�������CO2 c.���������NaOH d.����������HCl e.ϴ�� f.����
(3)MnO2�ܽ����������е���Ԫ������Ϊ���ʣ�д����Ӧ����CuS������Ӧ�Ļ�ѧ����ʽ��___________������ŨHNO3�ܽ�������ȱ����_______(��дһ��)��
(4)��ҺD��c(Cu2+)��2.2mol��L��1��c(Fe3+)��8.0��10��3mol��L��1��c(Mn2+)��0.01mol��L��1����μ���Na2CO3��Һ����pH�ɽ���ת��������������η��룬���ȳ�������_______(�����ӷ���)��Ϊʹͭ���ӿ�ʼ������������Ӧ������Һ��pH����______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£������̼����(Na2CS3)��õ���ɫ��״���壬��̼��������������ڹ�ũҵ�������й㷺����;��ijС�����ʵ��̽�������̼���Ƶ����ʲ��ⶨ����Һ��Ũ�ȡ�
ʵ��һ��̽��Na2CS3������
(1)��Na2CS3��Һ�е����̪��Һ����Һ���ɫ�������ӷ���ʽ˵����Һ�ʼ��Ե�ԭ��_________��
(2)��Na2CS3��Һ�еμ�����KMnO4��Һ����ɫ��ȥ���÷�Ӧ�б�������Ԫ����__________��
ʵ������ⶨNa2CS3��Һ��Ũ��
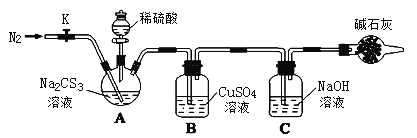
����ͼ��ʾ���Ӻ�װ�ã�ȡ50.0mLNa2CS3��Һ��������ƿ�У���Һ©���Ļ�������������2.0mol/LϡH2SO4���رջ�����
��֪��Na2CS3+ H2SO4��Na2SO4+ CS2+ H2S����CS2��H2S���ж���CS2������ˮ���е�46�棬�ܶ�1.26g/mL����CO2ijЩ�������ƣ���NaOH��������Na2COS2��H2O��
(1)ʢ�ż�ʯ�ҵ�������������_______����ʯ�ҵ���Ҫ�ɷ���______(�ѧʽ)��
(2)C�з�����Ӧ�����ӷ���ʽ��____________��
(3)��Ӧ���������K���ٻ���ͨ��N2һ��ʱ�䣬��Ŀ����_________��
(4)Ϊ�˼���Na2CS3��Һ��Ũ�ȣ��Գ�ַ�Ӧ��B�л������й��ˡ�ϴ�ӡ�������أ���8.4g ���壬������ƿ��Na2CS3�����ʵ���Ũ��Ϊ______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������װ��ģ���������Ƽ����ͨ���Ʊ���NH3��CO2���뱥��ʳ��ˮ��Ӧ���Ʊ�NaHCO3������˵����ȷ���ǣ� ��
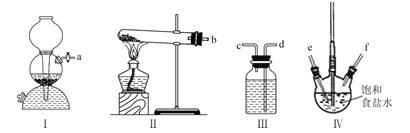
A.ʵ��ʱװ��I����������Ӧ��ͨ�˵�װ��IV��
B.װ��II�е��Լ�ΪŨ����
C.���ܿڵ�����˳��Ϊa-e-f-d-c-b
D.ʵ������У�װ��IV�ڻ���ֻ�������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com