
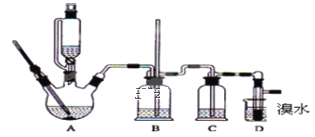
【题目】实验室用少量的溴水和足量的乙烯制备1,2-二溴乙烷的装置如图所示:
有关数据列表如下:
乙醇 | 1,2-二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/gcm-3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | -l30 | 9 | -1l6 |
回答下列问题:
(1)烧瓶A中发生的主要的反应方程式:___________________________________。
(2)安全瓶B可以防倒吸,并可以检查实验进行时试管D是否发生堵塞.请写出发生堵塞时瓶B中的现象:______________________________________________________。
(3)在装置C中应加入_____(填字母),(a.水 b.浓硫酸 c.氢氧化钠溶液)其目的是 ___________________________________________________________________。
(4)若产物中有少量副产物乙醚,可用 ________________ 的方法除去。
(5)反应过程中应用冷水冷却装置D,但又不能过度冷却(如用冰水),其原因是 _________________________________________________________________________。
【答案】CH3CH2OH![]() CH2=CH2↑+H2O; B中水面会下降,玻璃管中水柱会上升。 c 除去CO2和SO2 蒸馏 过度冷却会使使产品凝固而使气路堵塞
CH2=CH2↑+H2O; B中水面会下降,玻璃管中水柱会上升。 c 除去CO2和SO2 蒸馏 过度冷却会使使产品凝固而使气路堵塞
【解析】
装置A:乙醇在浓硫酸、加热条件下发生消去反应生成乙烯,浓硫酸具有强氧化性,将乙醇氧化成二氧化碳,自身被还原成二氧化硫,装置B:B为安全瓶,可以防止倒吸,装置D生成1,2-二溴乙烷,反应后容器内气压减小,1,2-二溴乙烷熔点为9℃,冷却容易析出晶体,堵塞玻璃导管,根据B中内外液面高低变化,可以判断是否发生堵塞,装置C:二氧化碳、二氧化硫能和氢氧化钠溶液反应,二氧化硫能与溴反应,盛放氢氧化钠溶液除去乙烯中的二氧化碳、二氧化硫,装置D:乙烯与溴反应生成1,2-二溴乙烷;溴易挥发,为防止污染空气,D装置之后需要连接盛放氢氧化钠溶液吸收尾气装置。
(1)、三颈烧瓶A中发生反应是乙醇在浓硫酸的作用下加热到170℃产生乙烯;
(2)、1,2-二溴乙烷熔点为9℃,冷却容易析出晶体,堵塞玻璃导管,B为安全瓶,可以防止倒吸,根据玻璃导管中内外液面高低变化,可以判断是否发生堵塞;
(3)、浓硫酸具有强氧化性,将乙醇氧化成二氧化碳,自身被还原成二氧化硫,二氧化碳、二氧化硫能和氢氧化钠溶液反应,二氧化碳在水中溶解度小,浓硫酸既不能吸收二氧化碳,也不能吸收二氧化硫,饱和碳酸氢钠溶液不能吸收二氧化碳;
(4) 1,2-二溴乙烷与乙醚的沸点不同,两者均为有机物,互溶,用蒸馏的方法将它们分离;
(5)、乙烯与溴反应时放热,冷却可避免溴的大量挥发,但不能过度冷却(如用冰水),否则使气路堵塞;
(1)、A中乙醇发生消去反应生成乙烯,反应方程式为: CH3CH2OH![]() CH2=CH2↑+H2O;
CH2=CH2↑+H2O;
故答案为:CH3CH2OH![]() CH2=CH2↑+H2O;
CH2=CH2↑+H2O;
(2)、1,2-二溴乙烷熔点为9℃,冷却容易析出晶体,堵塞玻璃导管,B为安全瓶,可以防止倒吸,根据玻璃导管中内外液面高低变化,可以判断是否发生堵塞;
故答案为B中水面会下降,玻璃管中水柱会上升;
(3)、浓硫酸具有强氧化性,将乙醇氧化成二氧化碳,自身被还原成二氧化硫,所以制取的乙烯气体中会含有CO2和SO2,而SO2具有还原性,也能使溴水褪色,故装置C中盛有的溶液需吸收乙烯中的杂质气体二氧化碳和二氧化硫的,水吸收二氧化碳能力弱,浓硫酸不吸收二氧化碳、二氧化硫,饱和碳酸氢钠溶不吸收二氧化硫,二氧化碳、二氧化硫能和氢氧化钠溶液反应被吸收,SO2+ 2NaOH=Na2SO3+ H2O, CO2+ 2NaOH=Na2CO3+ H2O,不和乙烯反应,故选用氢氧化钠溶液。
故答案为: c;除去CO2和SO2;
(4)、若产物中有少量副产物乙醚,1, 2-二溴乙烷与混有的乙醚互溶,但沸点不同,可用蒸馏的方法除去,
故答案为:蒸馏;
(5)、溴在常温下,易挥发,乙烯与溴反应时放热,溴更易挥发,冷却可避免溴的大量挥发,但1,2-二溴乙烷的凝固点9℃较低,不能过度冷却,否则会使产品凝固而堵塞导管,
故答案为:过度冷却会使使产品凝固而使气路堵塞。


科目:高中化学 来源: 题型:
【题目】孔雀石的主要成分是Cu2(OH)2CO3(含Fe2O3、FeCO3、Al2O3、SiO2杂质),工业上用孔雀石制备硫酸铜的第一步需用过量的硫酸溶解并过滤。常温下,分别取滤液并向其中加入指定物质,反应后的溶液中大量存在的离子组正确的是
A. 加入过量氨水:Fe3+、NH4+、SO42-、OH-
B. 加入过量NaClO溶液:Fe2+、Na+、ClO-、SO42-
C. 加入过量NaOH溶液:Na+、AlO2-、SO42-、OH-
D. 加入过量NaHCO3溶液:Na+、Al3+、SO42-、HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高血脂是一种常见的心血管疾病,治疗高血脂的新药 I 的合成路线如下:
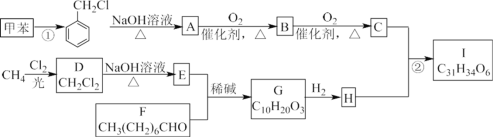
已知:a. 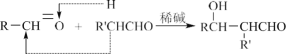 b.
b. 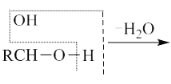 RCHO
RCHO
回答下列问题:
(1)反应①所需试剂、条件分别是________;F 的化学名称为________
(2)②的反应类型是________;A→B 的化学方程式为________。
(3) G 的结构简式为________;H 中所含官能团的名称是________。
(4)化合物 W 的相对分子质量比化合物 C 大 14,且满足下列条件:①遇 FeCl3 溶液显紫色 ②属于芳香族化合物
③能发生银镜反应,W 的可能结构有________种,其中核磁共振氢谱显示有 5 种不同化学环境的氢,峰面积比为2:2:2:1:1 的结构简式为________。
(5)设计用甲苯和乙醛为原料制备 ![]() 的合成路线________ (无机试剂任选)。
的合成路线________ (无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25oC时,H2A的Ka1=10-1.85,Ka2=10-7.19。用0.1mol·L-1NaOH溶液滴定20mL0.1mol·L-1H2A溶液的滴定曲线如图所示(曲线上的数字为pH)。下列说法不正确的是
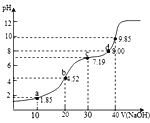
A.a点所得溶液中:2c(H2A)+c(A2-)<0.1mol·L-1
B.NaHA溶液中由水电离出的氢离子浓度小于1.0×10-7mol·L-1
C.c点所得溶液中:c(Na+)<3c(HA_)
D.d点所得溶液中:c(Na+)>c(A2-)>c(HA-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物A的结构简式如图所示.下列叙述正确的是( )
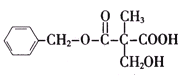
A.A不能和新制Cu(OH)2悬浊液反应
B.A中含有2种含氧官能团
C.A能够发生加成、取代和消去反应
D.1molA和足量的NaOH溶液反应,消耗2molNaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应过程中不存在电子转移的是( )
A.Zn+2HCl=ZnCl2+H2↑
B.Ca(ClO)2+2HCl=CaCl2+2HClO
C.Pb3O4+8HCl(浓)=3PbCl2+Cl2↑+4H2O
D.3Cl2+6KOH(浓)![]() 5KCl+KClO3+3H2O
5KCl+KClO3+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学兴趣小组为研究Cl2的性质并制备氯水,用如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。

(1)加入药品前,检查I中气体发生装置气密性的操作是__。
(2)装置Ⅰ中发生反应的化学方程式为__。
(3)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为应在__和___(填装置序号)之间添加洗气装置,该装置的作用是___。
(4)装置V中NaOH溶液的作用是__,相关反应的化学方程式为___。
(5)反应完毕,为探究装置Ⅳ中溶质的成分,需要的试剂主要有__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是部分短周期元素的单质及其化合物(或其溶液)的转化关系。已知在常温常压下,A是固体,B、C、D、E是非金属单质且都是气体,C呈黄绿色;化合物F是淡黄色固体,化合物G的焰色反应为黄色,化合物Ⅰ和J通常状况下呈气态;D和E反应生成一种刺激性气味的气体。
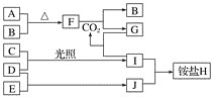
请回答下列问题:
(1)E和J的化学式分别是________和________。
(2)写出F和CO2反应的化学方程式并用单线桥法表示电子转移的情况:_________。
(3)将少量单质C通入盛有淀粉碘化钾溶液的试管中,溶液变蓝色,该反应的离子方程式为_________。
(4)标况下3.36 L气体B与A完全反应,转移电子的数目为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年新发现的元素鉝(Lv)是116号主族元素,其原子核外最外层电子数是6。下列说法不正确的是 ( )
A.Lv位于第七周期第VIA族B.Lv在同主族元素中金属性最弱
C.Lv的同位素原子具有相同的电子数D.中子数为177的Lv核素符号为![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com