
| A、通过电解熔融的Z、Q形成的化合物可制取Z单质 |
| B、原子半径的大小顺序为W>Q>Z>X>Y |
| C、元素Y的最高正化合价为+6 |
| D、XQ3分子中,中心原子是sp3杂化 |


 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案科目:高中化学 来源: 题型:
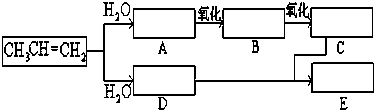
| 催化剂 |
| △ |
| 浓硫酸 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
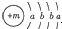 ,X的阳离子与Y的阴离子的电子层结构相同.元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子.
,X的阳离子与Y的阴离子的电子层结构相同.元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子.
查看答案和解析>>
科目:高中化学 来源: 题型:
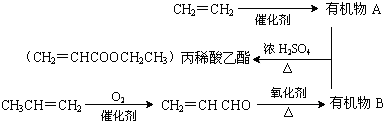
| 催化剂 |
| △ |
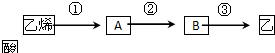
查看答案和解析>>
科目:高中化学 来源: 题型:
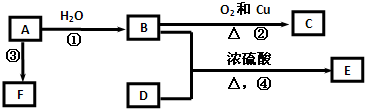
查看答案和解析>>
科目:高中化学 来源: 题型:
 )对花香和果香的香韵具有提升作用,故常用于化妆品和食品工业.乙酸苯甲酯的合成路线如图:
)对花香和果香的香韵具有提升作用,故常用于化妆品和食品工业.乙酸苯甲酯的合成路线如图: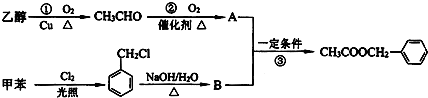
 )互为同系物的是
)互为同系物的是 B.
B.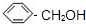 C.
C.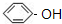 D.
D.
 C.2CH3CHO+H2
C.2CH3CHO+H2| 催化剂 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向碳酸氢钙溶液中滴入过量澄清石灰水:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O | ||||
B、NH4HSO3溶液与足量的NaOH溶液混合加热:NH4++HSO3-+2OH-
| ||||
| C、向NaHSO4溶液中逐滴加入Ba(OH)2溶液至溶液呈中性:H++SO42-+Ba2++OH-═BaSO4↓+H2O | ||||
| D、向KIO3与KI混合溶液中加入醋酸发生反应生成I2:IO3-+5I-+6H+═3I2+3H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com