
����Ŀ��λ��ǰ�����ڵ�8��Ԫ��A��B��C��D��E��F��G��H��ԭ������������������A������ԭ����ԭ�Ӱ뾶��С�ģ�����Bͬ�壬C�Ļ�̬ԭ��2P�ܼ���ֻ��1�����ӣ�F����A�ɰ�ԭ�Ӹ�����1��1��1��2�γɻ����F��Gͬ�壬H��ԭ������Ϊ29������������Ϣ��������ش��������⣺
��1����д������8��Ԫ���е縺������Ԫ����BԪ���γɳ����Ļ�����Ļ�ѧʽ_______���þ���Ԫ�ط��ű�ʾ�Ļ�ѧʽ����д����̬ԭ�ӵĵ�һ����������Ԫ�������ڱ��е�λ��Ϊ________��
��2��д��H��ԭ���ڻ�̬ʱ�ĺ�������Ų�ʽΪ____________��
��3��1mol D2A6���ӣ���״���к���![]() ������ĿΪ____________��
������ĿΪ____________��
��4����֪A2F2���ӽṹ��ͼa��ʾ����������ԭ���ӻ��������Ϊ_________��

��5���ж�A2F2________�����ѻ��ף�����DG2������Ҫ˵��ԭ��___________��
��6��C��E�γ�ij������ľ�����ͼ b��ʾ�����ھ��������ϵ�ԭ�ӵ���λ��Ϊ________�����û�������ܶ�Ϊ![]() g��cm
g��cm![]() �������ӵ�����ΪNA�����������Eԭ�Ӽ�ľ���Ϊ_______ pm���ú�
�������ӵ�����ΪNA�����������Eԭ�Ӽ�ľ���Ϊ_______ pm���ú�![]() ��NA�Ĵ���ʽ��ʾ����
��NA�Ĵ���ʽ��ʾ����
���𰸡� Li2O �ڶ����ڵ�VA�� 1s22s22p63s23p63d104s1��[Ar]3d104s1 7NA(��7��6.02��1023) sp3(�ӻ�) �� ��ΪH2O2Ϊ���Է��ӣ�CS2Ϊ�Ǽ����ܼ���������������ԭ����֪��H2O2���ܽ���CS2�� 4 ![]()
��������λ��ǰ�����ڵ�8��Ԫ��A��B��C��D��E��F��G��H��ԭ������������������A������ԭ����ԭ�Ӱ뾶��С�ģ���AΪ��Ԫ�أ�����Bͬ�壬C�Ļ�̬ԭ��2P�ܼ���ֻ��1�����ӣ���CΪ��Ԫ�أ�BΪ�Ԫ�أ�F����A�ɰ�ԭ�Ӹ�����1��1��1��2�γɻ����FΪ��Ԫ�أ��γ�H2O��H2O2���ֻ����F��Gͬ�壬gΪ��Ԫ�أ�H��ԭ������Ϊ29��HΪͭԪ�أ��ٽ��C��D��E��Fԭ��������������CΪ��Ԫ�أ�FΪ��Ԫ�أ�D��Ϊ̼Ԫ�أ�E��Ϊ��Ԫ�ء�
��1������8��Ԫ���е縺������Ԫ�����������Ԫ���γɳ����Ļ�����Ļ�ѧʽLi2O����̬ԭ�ӵĵ�һ����������Ԫ���ǵ��������ڱ��е�λ��Ϊ�ڶ����ڵ�VA������2��HΪͭԪ�أ�ͭԭ���ڻ�̬ʱ�ĺ�������Ų�ʽΪ1s22s22p63s23p63d104s1��[Ar]3d104s1 ����3��һ��C2H6�����к�6��C-H����һ��C-C����1mol C2H6���ӣ���״���к���![]() ������ĿΪ7mol��7��6.02��1023����4������A2F2���ӽṹͼ����ԭ���γ�2��
������ĿΪ7mol��7��6.02��1023����4������A2F2���ӽṹͼ����ԭ���γ�2��![]() �������������Թµ��Ӷԣ���������ԭ���ӻ��������Ϊ sp3(�ӻ�)����5������A2F2���ӽṹͼ���ж�H2O2Ϊ���Է�����������CS2����ΪH2O2Ϊ���Է��ӣ�CS2Ϊ�Ǽ����ܼ���������������ԭ����֪��H2O2���ܽ���CS2������6��C��E�γ�ij������ľ�����ͼ b��ʾ�����ھ��������ϵ�ԭ�ӵ���λ��Ϊ4��ÿ�������к���Bԭ��Ϊ
�������������Թµ��Ӷԣ���������ԭ���ӻ��������Ϊ sp3(�ӻ�)����5������A2F2���ӽṹͼ���ж�H2O2Ϊ���Է�����������CS2����ΪH2O2Ϊ���Է��ӣ�CS2Ϊ�Ǽ����ܼ���������������ԭ����֪��H2O2���ܽ���CS2������6��C��E�γ�ij������ľ�����ͼ b��ʾ�����ھ��������ϵ�ԭ�ӵ���λ��Ϊ4��ÿ�������к���Bԭ��Ϊ![]() =4��ÿ�������к���Nԭ��Ϊ4������������Ϊ25g��mol��1��4/NA=100/NAg,���ɸû�������ܶ�Ϊ
=4��ÿ�������к���Nԭ��Ϊ4������������Ϊ25g��mol��1��4/NA=100/NAg,���ɸû�������ܶ�Ϊ![]() g��cm
g��cm![]() �þ����ı߳�Ϊ
�þ����ı߳�Ϊ![]() cm=
cm=![]() ��1010pm�����������Eԭ�Ӽ�ľ���Ϊ
��1010pm�����������Eԭ�Ӽ�ľ���Ϊ![]()
![]() ��1010pm��pm���ú�
��1010pm��pm���ú�![]() ��NA�Ĵ���ʽ��ʾ����
��NA�Ĵ���ʽ��ʾ����


 ��1����Ԫ�¿�������ĩϵ�д�
��1����Ԫ�¿�������ĩϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼ��ʾ���л���X������S���տ���Y������̼ԭ����ָ�������ĸ���ͬ��ԭ�ӻ�ԭ���ŵ�̼ԭ�ӣ������з���ȷ���ǣ� ����


A. X���Է���������ȡ�����������Ӿۡ����۷�Ӧ�����������ᷴӦ�����л���
B. Y�ȿ�����FeCl3��Һ������ɫ��Ӧ���ֿ�ʹ����KMnO4��Һ��ɫ
C. 1mol X������NaOH��Һ��Ӧ���������4mol NaOH��
D. X�ṹ����2������̼ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ�鷽������У����е���
A. ��ϡ�������ˣ���ȥ����ͭ���е�����þ�ۺ�����
B. ����ȡ�ķ����������ͺ�ú��
C. ���ܽ⡢���˵ķ�������KNO3��NaCl����Ļ����
D. ��O2��H2�Ļ������ͨ�����ȵ�����ͭ���Գ�ȥ���е�H2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȼ�ϵ����һ������Դ������2CO+O2=2CO2���ȼ�ϵ��ʱ������������Ӧ��������_______����������������������Ӧ�ĵ缫��Ӧ��____________ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʻ�Ϊͬϵ����ǣ� ��
A.��ϩ��1��3������ϩ
B.CH3Cl��CH2Cl2
C.��ϩ�;���ϩ
D.���Ͷ��ױ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵���д�����ǣ���
A. ��������ϩ��lmol����ȫȼ�պ�����2molH2O
B. �����£��춡����Cl2����ȡ����Ӧ���ɵ�һ�ȴ�����2��
C. ��ϩ������������ʳƷ��װ���ϵ�ԭ��
D. ��������к���̼��˫������������ʹ��ˮ��ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����N2��H2Ϊ��Ӧ������ữ��NH4Cl��ҺΪ����ʵ�ԭ��أ�����ԭ������ͼ��ʾ������˵������ȷ����
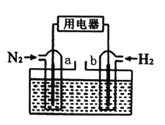
A. b�缫Ϊ����
B. ��Ӧ�����У���Һ�е�Cl-��a�缫�ƶ�
C. a�缫�ĵ缫��ӦʽΪ��N2+6e-+8H+=2NH4+
D. ��ط�ӦΪN2+3H2+2HCl=2NH4Cl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�������ڲ����������ǣ� ��
A.���������ļӳɷ�Ӧ����
B.�Ҵ�����ȥ��Ӧ����
C.������������ȡ����Ӧ����
D.��ϩ�ļӾ۷�Ӧ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��BaCl2��Һ��ͨ��SO2���壬û�г������ɡ���ͨ������ij���ʺ��г������ɣ�������ʲ�����Ϊ
A. HCl B. NO2 C. NH3 D. FeC13
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com