
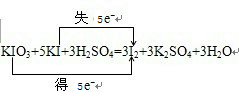
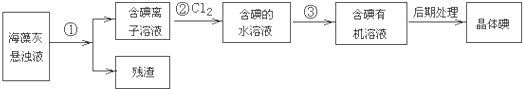
 ,碘单质从碘水中提取可以采用萃取分液法,利用四氯化碳来萃取,然后根据四氯化碳和碘的沸点的不同来分离,
,碘单质从碘水中提取可以采用萃取分液法,利用四氯化碳来萃取,然后根据四氯化碳和碘的沸点的不同来分离, ;萃取、蒸馏.
;萃取、蒸馏.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| 1 |
| 5 |
| A、排出废气中氮的氧化物含量多少与辛烷和空气的体积无关 |
| B、辛烷蒸气和空气的体积比大于2:125时,排出废气中氮的氧化物增多 |
| C、辛烷蒸气和空气的体积比等于2:125时,排出废气中不含一氧化碳和氮的氧化物 |
| D、辛烷蒸气和空气的体积比大于2:125时,排出废气中一氧化碳含量最多 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、石油的分馏和煤的气化都是发生了化学变化 |
| B、苯、溴水、铁粉混合可制成溴苯 |
| C、苯在一定条件下既能发生取代反应,又能发生加成反应,但不能发生氧化反应 |
| D、纤维素、油脂和蛋白质在一定条件下都能水解 |
查看答案和解析>>
科目:高中化学 来源: 题型:
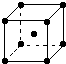 如图是金属钨晶体中的
如图是金属钨晶体中的查看答案和解析>>
科目:高中化学 来源: 题型:
| A、读数时,俯视确定凹液面与刻度线相切 |
| B、容量瓶使用前经蒸馏水清洗后还残留有少量蒸馏水 |
| C、定容后把容量瓶颠倒摇匀,发现液面低于刻度线,又补足了所缺的水 |
| D、配制过程中,用蒸馏水洗涤烧杯和玻璃棒后,未把洗涤液移入容量瓶 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com