
【题目】已知铜和浓硫酸可以在加热条件下发生如下反应(反应方程式已配平):
![]() (浓)
(浓)![]()
![]()
试完成下面的问题:
(1)A物质可以导致酸雨的形成。则A应该属于______(用字母代号填写)
a.酸 b. 碱 c.盐 d.酸性氧化物 e.碱性氧化物
(2)该反应中被氧化的元素是_________________,参加反应的氧化剂与还原剂的物质的量之比为______。
(3)写出该反应的化学方程式并用双线桥标出电子转移的方向和数目:____________。
(4)一定量的铜片与100mL 18 mol/L的浓![]() 充分反应,如果该反应过程中转移了0.2mol电子,生成的
充分反应,如果该反应过程中转移了0.2mol电子,生成的![]() 的质量为_________g,生成的A气体在标准状况下体积为________L(假设气体全部逸出)。
的质量为_________g,生成的A气体在标准状况下体积为________L(假设气体全部逸出)。
【答案】d Cu 1︰1 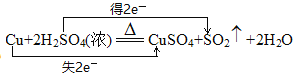 16 2.24
16 2.24
【解析】
(1)根据已配平的化学反应方程式中元素守恒,可确定A为SO2,结合SO2气体能导致酸雨确定其类别。
(2)化合价入手分析,元素化合价升高的过程为氧化反应(或被氧化),得电子的反应物是氧化剂,失电子的反应物为还原剂,由此分析。
(3)运用双线桥表示电子转移的方向和数目时,线桥过等号,箭头由反应物指向生成物且箭头的起点和终点是同种元素,线桥上标明“得ne-”或“失ne-”。
(4)根据Cu+2H2SO4(浓)![]() CuSO4+SO2
CuSO4+SO2![]() +2H2O~转移2e-中计量关系计算。
+2H2O~转移2e-中计量关系计算。
(1)因为有Cu+2H2SO4(浓)![]() CuSO4+A
CuSO4+A![]() +2H2O,根据元素守恒知A是SO2,因A能形成酸雨,且SO2能与碱反应生成盐和水:SO2+2NaOH=Na2SO3+H2O,所以SO2是酸性氧化物,答案选d。
+2H2O,根据元素守恒知A是SO2,因A能形成酸雨,且SO2能与碱反应生成盐和水:SO2+2NaOH=Na2SO3+H2O,所以SO2是酸性氧化物,答案选d。
(2) 根据反应式Cu+2H2SO4(浓)![]() CuSO4+SO2
CuSO4+SO2![]() +2H2O,铜元素的化合价由0价升高到CuSO4中的+2价,故铜元素发生氧化反应(或被氧化);单质铜是还原剂,硫元素化合价由H2SO4中的+6价降低到SO2中的+4价,H2SO4得电子是氧化剂,2molH2SO4中只有1molH2SO4得电子,根据化学计量数可知,参加反应的氧化剂与还原剂的物质的量之比为1:1。
+2H2O,铜元素的化合价由0价升高到CuSO4中的+2价,故铜元素发生氧化反应(或被氧化);单质铜是还原剂,硫元素化合价由H2SO4中的+6价降低到SO2中的+4价,H2SO4得电子是氧化剂,2molH2SO4中只有1molH2SO4得电子,根据化学计量数可知,参加反应的氧化剂与还原剂的物质的量之比为1:1。
(3)运用双线桥表示电子转移的方向和数目时,线桥过等号,箭头的起点和终点都指向同一元素且由反应物指向生成物,线桥上标明“得”或“失”及电子数目: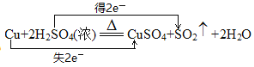 。
。
(4)根据Cu+2H2SO4(浓)![]() CuSO4+SO2
CuSO4+SO2![]() +2H2O~转移2e-,可知每转移2mol电子生成1molCuSO4和1molSO2,所以转移0.2mol电子生成CuSO4的物质的量=
+2H2O~转移2e-,可知每转移2mol电子生成1molCuSO4和1molSO2,所以转移0.2mol电子生成CuSO4的物质的量=![]() ×0.2mol=0.1mol,0.1molCuSO4的质量=0.1mol×160g/mol=16g;转移0.2mol电子时生成SO2气体物质的量=
×0.2mol=0.1mol,0.1molCuSO4的质量=0.1mol×160g/mol=16g;转移0.2mol电子时生成SO2气体物质的量=![]() ×0.2mol=0.1mol,0.1molSO2在标准状况下的体积=0.1mol×22.4L/mol=2.24L。
×0.2mol=0.1mol,0.1molSO2在标准状况下的体积=0.1mol×22.4L/mol=2.24L。


科目:高中化学 来源: 题型:
【题目】盐在化学工业中有重要的应用,请回答下列问题:
(1)用化学方程式表示配制FeCl3溶液时常加入浓盐酸的原因______________________________________________
(2)常温下,在pH=3的Al2(SO4)3溶液与pH=11的Na2S溶液中,水电离出来的c(OH﹣)之比为______,将两溶液混合后,产生白色沉淀和有臭鸡蛋味的气体,其反应的离子方程式为_________________________
(3)c(NH4+)相等的下列溶液①NH4Cl ②NH4HSO4 ③(NH4)2SO4 ④CH3COONH4 ⑤NH3·H2O,溶液的物质的量浓度由小到大的顺序是______________________________________________________ (用序号表示)
(4)已知t℃时①AgCl的Ksp=2×10﹣10;②在t℃时,Ag2CrO4在水中的沉淀溶解平衡曲线如图所示.下列正确的是_______

A.在饱和Ag2CrO4溶液中加入K2CrO4可使溶液由Y点到X点
B.在t℃时Ag2CrO4的Ksp为1×10-12
C.在t℃时反应:Ag2CrO4(s)+2Cl-(aq)![]() 2AgCl(s)+CrO42-(aq)的平衡常数为2.5×107
2AgCl(s)+CrO42-(aq)的平衡常数为2.5×107
D.在t℃时以0.01mol/L的AgNO3溶液滴定20mL浓度均为0.01mol/L的KCl和K2CrO4的混合溶液,CrO42-先沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究硫元素及其化合物的性质具有重要意义。
(1)25 ℃,在0.10 mol·L-1H2S溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-)关系如下图(忽略溶液体积的变化、H2S的挥发)。

①pH=11时,溶液中的c(H2S)+c(HS-)=________mol·L-1。
②某溶液含0.020 mol·L-1Mn2+、0.10 mol·L-1H2S,当溶液pH=________时,Mn2+开始沉淀。[已知:Ksp(MnS)=2.8×10-13]
(2)25 ℃,两种酸的电离常数如下表。
Ka1 | Ka2 | |
H2SO3 | 1.3×10-2 | 6.3×10-8 |
H2CO3 | 4.2×10-7 | 5.6×10-11 |
①HCO![]() 的电离常数表达式K=________。
的电离常数表达式K=________。
②0.10 mol·L-1Na2SO3溶液中离子浓度由大到小的顺序为___________________。
③H2SO3溶液和NaHCO3溶液反应的主要离子方程式为__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】材料是人类赖以生存和发展的重要物质基础。请回答下列问题:
(1)有机合成材料的出现是材料发展史上的一次重大突破。人们常说的三大合成材料是指__________________、__________________、__________________。
(2)聚氯乙烯的商品名为PVC,其结构简式为____________________,PVC管材中还需要加入具有特殊用途的添加剂,如_______________、________________等,因为PVC具有_____________性,所以由它制得的材料可反复加工、多次使用。
(3)合金是生活中常见的材料,某合金具有密度小、强度高的优良性能,常用于制造门窗框架,该合金中含量最高的金属为_______(填元素符号),该元素在周期表中的位置为______________________________。
(4)玻璃是一种常见的硅酸盐材料,制备普通玻璃的原料有CaCO3、_______和_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】防治环境污染,改善生态环境已成为全球的共识。
(1)向煤中加入石灰石作为脱硫剂,可以减少燃烧产物SO2的排放,生成CaSO4。写出SO2减少的化学方程式:___________________________________________。
(2)煤的气化和液化是高效、清洁利用煤炭的重要途径。将焦炭在高温下与水蒸气反应,得到CO和H2,发生该反应的化学方程式为:_______________________________。
(3)在汽车尾气系统中装置催化转化器,可有效降低尾气中的CO、NO、NO2和碳氢化合物等污染性气体。在催化转换器的前半部,CO和NO在催化剂的作用下发生反应,生成CO2和N2,该反应的化学方程式为:___________________________________。
(4)天然水中杂质较多,常需加入明矾、漂白粉等物质处理后才能饮用。其中漂白粉的作用是杀菌消毒,其作用原理可用化学方程式表示为:_________________________。
(5)处理含Cr2O72-的废水可先用(NH4)2Fe(SO4)2将Cr2O72-转化为Cr3+,再用氨水将Cr3+转变为难溶的Cr(OH)3,在该过程中氧化剂为______________,其中氨水转化Cr3+为Cr(OH)3的离子方程式为____________________________________________;该方案处理后的废水中因含有大量________元素,直接排放会导致水体富营养化。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物G是中药黄芩中的主要活性成分之一,具有氧化和抗肿痛作用。G的合成路线如下图所示:
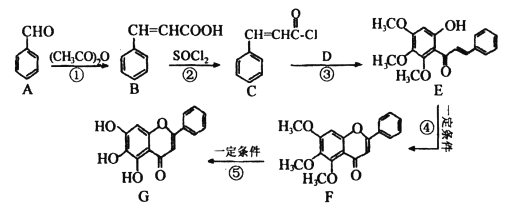
回答下列问题:
(1)写出G中含氧官能团的名称________;G的分子式为________。
(2)反应③的反应类型是______反应。
(3)D的分子式为C9H12O4,写出D的结构简式_________;同时符合下列条件的D的同分异构体有多种,请写出其中两种的结构简式_________。
a.属于苯的衍生物。苯环上共有4个取代基
b.核磁共振氢谱中有5种等效氢
c.与FeCl3溶液发生显色反应
(4)写出反应①化学方程式为___________。
(5)合成路线流程图示例: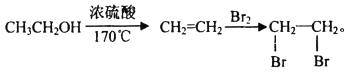 ,参照题中所给信息,任选试剂,由CH3CHO为原料合成
,参照题中所给信息,任选试剂,由CH3CHO为原料合成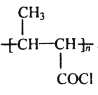 。______________________
。______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室里需要纯净的NaCl固体,但现在只有混有Na2SO4、NH4HCO3的NaCl固体混合物。某学生设计了如图所示方案提取纯净的NaCl固体。(已知:NH4HCO3![]() NH3↑+CO2↑+H2O)
NH3↑+CO2↑+H2O)

如果此方案正确,回答下列问题:
(1)操作①可选择的主要仪器是(________)(多选题)
A.酒精灯 B. 蒸馏烧瓶 C. 坩埚
(2)操作②不用硝酸钡溶液,其理由是______________________________________。
(3)进行操作②后,如何判断SO42 已除尽,方法是________________________。
(4)操作③加的是(________)
A.Na2CO3溶液 B.K2CO3溶液 C. NaNO3溶液
(5)操作④的目的是(________)(多选题)
A.除去过量的BaCl2溶液
B.除去溶解在溶液中的CO2
C. 除去溶解在溶液中的HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(2018·安徽省合肥市高三第三次教学质量检测)H2S在重金属离子处理、煤化工等领域都有重要应用。请回答:
Ⅰ.H2S是煤化工原料气脱硫过程的重要中间体,反应原理为
ⅰ.COS(g)+H2(g)![]() H2S(g)+CO(g)△H=+7kJ·mol1
H2S(g)+CO(g)△H=+7kJ·mol1
ⅱ.CO(g)+H2O(g)![]() CO2(g)+H2(g)△H=42kJ·mol1
CO2(g)+H2(g)△H=42kJ·mol1
已知断裂1mol气态分子中的化学键所需能量如下表所示。
分子 | COS(g) | H2(g) | CO(g) | H2S(g) |
能量(kJ·mol1) | 1310 | 442 | x | 669 |
(1)计算表中x=_______。
(2)T℃时,向VL容积不变的密闭容器中充入1mol COS(g)、1mol H2(g)和1mol H2O(g),发生上述两个反应。
①在T℃时测得平衡体系中COS为0.80 mol,H2为0.85 mol,则T℃时反应ⅰ的平衡常数K=_______(保留2位有效数字)。
②上述反应达平衡后,若向其中再充入1mol COS(g)、1molH2(g)和1mol H2O(g),则再次达平衡后H2的体积分数_______(填“增大”、“减小”或“不变”);若升高温度,则CO的平衡体积分数_______(填“增大”、“减小”或“不变”),其理由是_______。
Ⅱ.H2S在高温下分解制取H2,同时生成硫蒸气。
(3)向2L密闭容器中加入0.2molH2S,反应在不同温度(900~1500℃)下达到平衡时,混合气体中各组分的体积分数如下图所示,则在此温度区间内,H2S分解反应的主要化学方程式为_______;在1300℃时,反应经2min达到平衡,则0~2min的反应速率v(H2S)=_______。
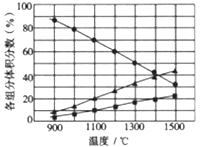
Ⅲ.H2S用作重金属离子的沉淀剂。
(4)25℃时,向浓度均为0.001mol·L1Sn2+和Ag+的混合溶液中通入H2S,当Sn2+开始沉淀时,溶液中c(Ag+)=_______。(已知:25℃时,Ksp(SnS)=1.0×1025,Ksp(Ag2S)=1.6×1049)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肉桂酸甲酯M,常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精。M属于芳香族化合物,苯环上只含有一个直支链,能发生加聚反应和水解反应。测得M的摩尔质量为162g·mol-1,只含碳、氢、氧,且原子个数之比为5:5:1。
(1)肉桂酸甲酯的结构简式是______________________。
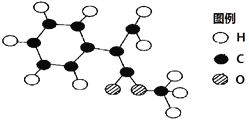
(2)G为肉桂酸甲酯的一种同分异构体,其分子结构模型如下图所示(图中球与球之间连线表示单键或双键)。G的结构简式为_________________。
(3)用芳香烃A为原料合成G的路线如下:
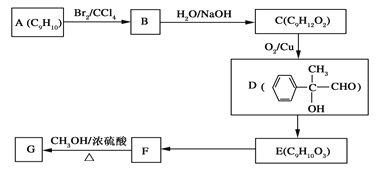
①化合物E中的官能团有________(填名称)。
②E→F的反应类型是________,
F→G的化学方程式为__________________________________________________。
③写出两种符合下列条件的F的稳定的同分异构体的结构简式_________________。
ⅰ.分子内含苯环,且苯环上只有一个支链;
ⅱ.在催化剂作用下,1mol该物质与足量氢气充分反应,最多消耗5mol H2;
ⅲ.它不能发生水解反应,但可以发生银镜反应。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com