
【题目】如图是Zn和Cu形成的原电池,下列说法正确的是( )
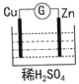
A.正极发生氧化反应
B.SO![]() 向负极移动
向负极移动
C.电子是由Zn片通过溶液流向Cu片
D.正极的电极反应式为Zn-2e-=Zn2+
科目:高中化学 来源: 题型:
【题目】氮、铬及其相关化合物用途非常广泛。回答下列问题:
(1)基态N原子的核外电子排布式为___,Cr位于元素周期表第四周期___族。
(2) Cr与K位于同一周期且最外层电子数相同,两种元素原子第一电离能的大小关系为___;Crcl3的熔点(83℃)比CrF3的熔点(1100℃)低得多,这是因为___。
(3) Cr的一种配合物结构如图所示:

①阴离子C1O4-的空间构型为___形。
②配离子中,中心离子的配位数为___,N与中心原子形成的化学键称为___键。
③配体H2 NCH2 CH2 NH2(乙二胺)中碳原子的杂化方式是______ ,分子中三种元素电负性从大到小的顺序为___
(4)氮化铬的熔点为1770℃,它的一种晶体的晶胞结构如图所示,其密度为5. 9 g·cm -3,氮化铬的晶胞边长为___(列出计算式)nm.

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磺酰氯(SO2Cl2)是一种有机氯化剂,也是锂电池正极活性物质。已知磺酰氯是一种无色液体,熔点-54.1℃,沸点69.1℃,遇水发生剧烈水解。
(1)已知:SO2(g) +Cl2(g)+ SCl2(g)![]() 2SOCl2(g) △H=a kJ·mol-1
2SOCl2(g) △H=a kJ·mol-1
SO2Cl2(g)+ SCl2(g)![]() 2SOCl2(g) △H=b kJ·mol-1
2SOCl2(g) △H=b kJ·mol-1
则反应:SO2(g) + Cl2(g)![]() SO2Cl2(g) △H =______kJ·mol-1(用含a、b的代数式表示);该反应平衡常数表达式为K =______。
SO2Cl2(g) △H =______kJ·mol-1(用含a、b的代数式表示);该反应平衡常数表达式为K =______。
(2)磺酰氯可与白磷发生反应为:P4+ 10SO2Cl2= 4PCl5+ 10SO2↑,若生成1molSO2,则转移电子的物质的量为_____mol。
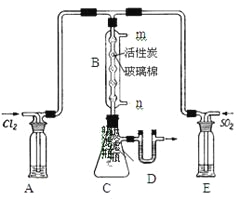
(3)某学习小组的同学依据反应:SO2(g)+ Cl2(g)![]() SO2Cl2(g) △H <0,设计的制备磺酰氯装置如图。
SO2Cl2(g) △H <0,设计的制备磺酰氯装置如图。
![]()
![]()
①若用浓盐酸与二氧化锰为原料制取Cl2,其反应的化学方程式为_____。
②上图所示的装置说法正确的是_____(不定项选择)。
a.A、E处洗气瓶中盛放的可能分别是饱和食盐水和饱和Na2SO3溶液
b.B处反应管内五球中玻璃棉上的活性炭作催化剂
c.B处反应管冷却水应从m接口通入
d.装置C处吸滤瓶应放在冰水中冷却
e.D处U形管中盛放的可能是碱石灰
③从化学平衡移动角度分析,反应管通水冷却的目的为______。
(4)GET公司开发的Li-SO2Cl2军用电池,其示意图如图所示,
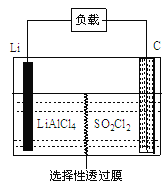
已知电池反应为:2Li + SO2Cl2=" 2LiCl" + SO2↑;则电池工作时,正极的电极反应式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溶液中的反应X+3Y![]() 2Z分别在①、②、③三种不同实验条件下进行,它们的起始浓度为c(X)=c(Y)=0.100molL-1、c(Z)=0molL-1,反应物X的浓度随时间变化如图所示。②、③与①比较只有一个实验条件不同,下列说法不正确的是
2Z分别在①、②、③三种不同实验条件下进行,它们的起始浓度为c(X)=c(Y)=0.100molL-1、c(Z)=0molL-1,反应物X的浓度随时间变化如图所示。②、③与①比较只有一个实验条件不同,下列说法不正确的是
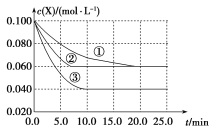
A.反应0~5.0min实验③的反应速率最快B.条件②的反应最先达到平衡
C.②与①比较,②可能压强更大D.该反应的正反应是吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表第四周期共有18种元素。回答下列问题:
(l)第四周期元素的基态原子中,最高能层中的s轨道上只有一个电子的元素有_____;
镍元素基态原子的电子排布式为____;p区元素第一电离能由大到小的前三种元素依次为____;
(2)GaBr3、GeBr4、AsBr3、AsBr5中,中心原子的轨道杂化类型为sp3的化合物是____;分子的立体构型为平面三角形的化合物是_____;AsBr5的分子构型为 ,则AsBr5是_____(填“极性”或“非极性”)分子。
,则AsBr5是_____(填“极性”或“非极性”)分子。
(3)已知GaF3的沸点为19.5℃、GaC13的沸点为201.3℃、GaBr3的沸点为292℃,导致沸点如此变化的原因是___________.
(4)Ca、CaO、CaC12等含钙物质的焰色均为砖红色,焰色形成的原因是钙元素在一定条件下产生原子_______光谱。CaO晶胞如图所示,CaO晶体中Ca2+的配位数为____;若CaO的密度为dg/cm3,则CaO的晶胞参数a=__________nm。
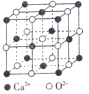
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知有关反应的能量变化如图,试回答下列问题。
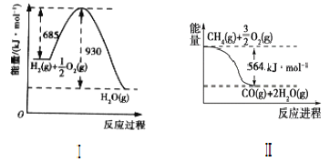
(1)根据图像,写出Ⅰ的热化学方程式:____。
(2)写出CH4(g)与H2O(g)反应制取CO(g)和H2(g)的热化学方程式:____。
(3)在(2)的反应中,相关的化学键键能数据如下表所示。判断H2O(g)中O—H的键能为___。
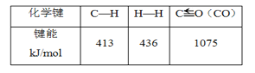
(4)试比较下列两组△H的大小(填“>”、“<”或“=”)
①C(s)+CO2(g)=2CO(g)△H1,C(s)+![]() O2(g)=CO(g)△H2则△H1___△H2。
O2(g)=CO(g)△H2则△H1___△H2。
②CH4(g)+H2O(g)=CO(g)+3H2(g)△H3,CH4(g)+H2O(l)=CO(g)+3H2(g)△H4,则△H3___△H4
③2H2(g)+O2(g)=2H2O(1)△H4,2H2(g)+O2(g)=2H2O(g)△H5,则△H4___△H5。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法正确的是( )
A.BrCH2CHBrCH2Br的名称为三溴丙烷
B.甘氨酸和丙氨酸混合物脱水成肽,最多可生成4种二肽
C.萘环(![]() )上的一个H原子被—C4H9取代后的产物共有6种
)上的一个H原子被—C4H9取代后的产物共有6种
D.C3H6和C4H8一定是同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向氨水中通入![]() ,得到含有
,得到含有![]() 、
、![]() 等物质的溶液,溶液中部分微粒的物质的量分数与pH的关系如图所示。下列说法正确的是
等物质的溶液,溶液中部分微粒的物质的量分数与pH的关系如图所示。下列说法正确的是![]()

A.随着![]() 的通入,溶液中
的通入,溶液中 不断增大
不断增大
B.已知常温下,![]() 的
的![]() 溶液
溶液![]() ,则常温下
,则常温下![]()
C.![]() 溶液中存在关系:
溶液中存在关系:![]()
D.![]() 时,溶液中
时,溶液中![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】国务院强调,“南水北调”工程必须坚持节水、治污和生态环境保护与工程建设相协调,以水资源合理配置为主线,把节水、治污和生态环境保护与调水作为一个完整的系统来分析的原则。在调水工程中,沿途工业污水的任意排放是造成水质恶化的最大隐患。经检测,某工厂废液中含有大量的![]() 、
、![]() 、
、![]() 、
、![]() 。试分析并回答下列问题:
。试分析并回答下列问题:
(1)该废液中可能大量存在的阴离子是________(填序号)。
A ![]() B
B ![]() C
C ![]() D
D ![]()
(2)为了回收废液中的金属银,某同学设计了如图所示的实验方案。若按照该方案获得金属银108g,在保证不污染环境且![]() 循环利用的情况下,可得出理论上应提供标准状况下的
循环利用的情况下,可得出理论上应提供标准状况下的![]() ________L。
________L。
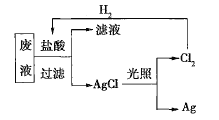
(3)为了实现(2)中氯气的循环利用,有人设想以氢气和氯气为原料利用原电池原理直接制盐酸,假设这种想法可行,下列说法肯定错误的是________(填序号)。
A 两极材料都用石墨,用稀盐酸作电解质溶液
B 通入氢气的电极为原电池的正极
C 电解质溶液中的阳离子向通入氯气的电极移动
D 通入氯气的电极的电极反应式为![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com