
【题目】已知有关反应的能量变化如图,试回答下列问题。
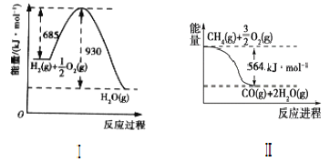
(1)根据图像,写出Ⅰ的热化学方程式:____。
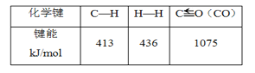
(2)写出CH4(g)与H2O(g)反应制取CO(g)和H2(g)的热化学方程式:____。
(3)在(2)的反应中,相关的化学键键能数据如下表所示。判断H2O(g)中O—H的键能为___。
(4)试比较下列两组△H的大小(填“>”、“<”或“=”)
①C(s)+CO2(g)=2CO(g)△H1,C(s)+![]() O2(g)=CO(g)△H2则△H1___△H2。
O2(g)=CO(g)△H2则△H1___△H2。
②CH4(g)+H2O(g)=CO(g)+3H2(g)△H3,CH4(g)+H2O(l)=CO(g)+3H2(g)△H4,则△H3___△H4
③2H2(g)+O2(g)=2H2O(1)△H4,2H2(g)+O2(g)=2H2O(g)△H5,则△H4___△H5。
【答案】H2(g)+![]() O2(g)=H2O(g) ΔH=-245kJ/mol CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH=+171kJ·mol-1 451kJ/mol > < <
O2(g)=H2O(g) ΔH=-245kJ/mol CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH=+171kJ·mol-1 451kJ/mol > < <
【解析】
(1)根据图像,反应Ⅰ是1molH2与![]() molO2的反应,反应放出的热量为930 kJ/mol -685 kJ/mol =245kJ/mol,故热化学方程式为H2(g)+
molO2的反应,反应放出的热量为930 kJ/mol -685 kJ/mol =245kJ/mol,故热化学方程式为H2(g)+![]() O2(g)=H2O(g) ΔH=-245kJ/mol;
O2(g)=H2O(g) ΔH=-245kJ/mol;
(2)设H2(g)+![]() O2(g)=H2O(g) ΔH=-245kJ/mol为式①,
O2(g)=H2O(g) ΔH=-245kJ/mol为式①,
根据图II得,CH4(g)+![]() O2(g)=CO(g)+2H2O(g) ΔH=-564kJ/mol,设此反应为式②,
O2(g)=CO(g)+2H2O(g) ΔH=-564kJ/mol,设此反应为式②,
反应CH4(g)+H2O(g)=CO(g)+3H2(g)可由②-3×①得到,该反应的ΔH=-564kJ/mol-3×(-245kJ/mol)= +171kJ/mol,故热化学方程式为CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH=+171kJ·mol-1;
(3)设O—H的键能为x,413 kJ/mol×4+2x-1075 kJ/mol -436 kJ/mol×3=171 kJ/mol,解得x=451kJ/mol;
(4)①C与CO2的反应为吸热反应,故△H1>0,C与O2的反应为放热反应,故△H2<0,所以△H1>△H2;
②H2O(g)生成 H2O(l)的过程为放热,所以第一个反应放出的热量更多,故△H3<△H4;
③H2O(l) 生成H2O(g) 的过程为吸热,所以第二个反应放出的热量少,故△H4<△H5;


 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案科目:高中化学 来源: 题型:
【题目】⑴常温下将0.2 mol/L HCl溶液与0.2 mol/L MOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=6,试回答以下问题:
①混合溶液中由水电离出的c(H+)_______0.2 mol/L的HCl溶液中由水电离出的c(H+);(填“>”、“<”、或“=”)
②求出混合溶液中下列算式的精确计算结果(填具体数字):c(Cl-)-c(M+)=_____mol/L;
c(H+)-c(MOH)=__________mol/L
⑵常温下若将0.2 mol/L HA溶液与0.1 mol/L NaOH溶液等体积混合,测得混合溶液的pH<7,则说明在相同条件下HA的电离程度______NaA的水解程度。(填“>”、“<”、或“=”)
⑶已知:难溶电解质Cu(OH)2在常温下的Ksp = 2×1020,则常温下:某CuSO4溶液中c(Cu2+) = 0.02 mol·L1,如要生成Cu(OH)2沉淀,应调整溶液的pH最小为_________。
⑷已知:温度和浓度相等时,氨水的电离程度与醋酸相等。常温下,下列4种溶液:
①0.1mol/L CH3COONa ②0.1mol/L CH3COONH4 ③0.1mol/L CH3COOH
④0.1mol/LCH3COONa和0.1mol/LNaOH的混合溶液
按pH由大到小顺序排列___________(填序号)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知气体有机物A是一种重要的化工原料,其在标准状况下的密度为![]() 。已知乙烯与乙酸在一定条件下能发生反应生成乙酸乙酯。
。已知乙烯与乙酸在一定条件下能发生反应生成乙酸乙酯。
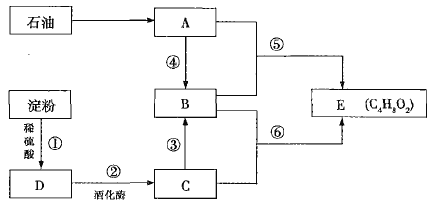
(1)C中的官能团名称是________;⑥的反应类型是________。
(2)反应⑤的化学反应方程式为___________________________________________(反应条件忽略)。
(3)下列说法正确的是________(填序号)。
A.淀粉发生反应①后直接加入银氨溶液可以检验D的生成
B.B、C、E可以用饱和碳酸钠溶液鉴别
C.反应⑥中浓硫酸的作用是催化剂和吸水剂
D.①和④的反应类型相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,水的电离达到平衡:H2O![]() H++OH-△H>0,下列叙述正确的是( )
H++OH-△H>0,下列叙述正确的是( )
A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低
B.向水中加入少量固体亚硫酸氢钠,c(H+)增大,水的电离程度增大
C.由水电离出的c(H+)=1×10-12mol/L的溶液pH一定为12
D.将水加热,Kw增大,pH减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是Zn和Cu形成的原电池,下列说法正确的是( )
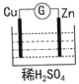
A.正极发生氧化反应
B.SO![]() 向负极移动
向负极移动
C.电子是由Zn片通过溶液流向Cu片
D.正极的电极反应式为Zn-2e-=Zn2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质在适宜的条件下反应,其中氧化剂与还原剂的物质的量之比为2:1的是( )
A. ![]()
B. Fe2O3+2Al![]() Al2O3+2Fe
Al2O3+2Fe
C. CaH2+2H2O===Ca(OH)2+2H2↑
D. 3NO2+H2O===2HNO3+NO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢能源是一种重要的清洁能源。现有两种可产生H2的化合物甲和乙。将6.00g甲加热至完全分解,只得到一种短周期元素的金属单质和6.72LH2(已折算成标准状况),甲与水反应也能产生H2,同时还产生一种白色沉淀物,该白色沉淀可溶于NaOH溶液。化合物乙在催化剂存在下可分解得到H2和另一种单质气体丙,丙在标准状态下的密度为1.25g/L。请回答下列问题:
(1)甲的化学式是__________;乙的电子式是__________。
(2)甲与水反应的化学方程式是__________。
(3)气体丙与金属镁反应的产物是__________(用化学式表示)。
(4)乙在加热条件下与CuO反应可生成Cu和气体丙,写出该反应的化学方程式__________。有人提出产物Cu中可能还含有Cu2O,请设计实验方案验证之__________(已知Cu2O+2H+=Cu+Cu2++H2O)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组用下列装置进行乙醇催化氧化的实验。

(1)请写出装有铜网的试管中反应的化学方程式:___。
(2)不断鼓入空气,熄灭酒精灯,反应仍能继续进行,说明该乙醇催化氧化反应是____反应(填“吸热”或“放热”)。
(3)甲和乙两个水浴作用不相同。甲的作用是___;乙的作用是___。
(4)反应进行一段时间后,集气瓶收集到的气体主要是___。
(5)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,要除去该物质,选择的试剂是__(填写字母):
a.氯化钠溶液 b.苯 c.碳酸氢钠溶液 d.金属钠
再通过___(填实验操作名称)即可得到乙醛。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.过量的100gNa2O2与CO2反应后,固体质量变成了105.6g,此反应转移电子为0.4mol
B.在Fe与含nmolHNO3的稀溶液反应中,被还原的HNO3不一定为![]() nmol
nmol
C.在Mg与Al做电极,其它溶液做电解质构成原电池中,Mg一定为负极
D.碱性氧化物一定为金属氧化物,酸性氧化物不一定是非金属氧化物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com