
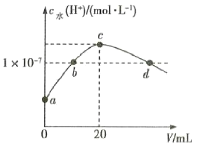
����Ŀ�������£�H2C2O4�ĵ��볣����Ka1=5.4��10-2��Ka2=5.0��10-5����V1mL0.1molL-1H2C2O4��Һ�еμ�0.1molL-1KOH��Һ�������Һ��ˮ�����cˮ��H+����KOH��Һ���V�Ĺ�ϵ��ͼ��ʾ������˵����ȷ���ǣ�������
A.V1=20mL
B.b���d���Ӧ����Һ�ж����ڣ�c��K+��=c��HC2O4-��+2c��C2O42-��
C.�����£���ˮϡ��b���Ӧ����Һ��ϡ�ͺ���ҺpH��С
D.�����£�KHC2O4��Kh1=2��10-10
���𰸡�D
��������
A������ͼ���ܹ�ˮ����δٽ�ˮ�ĵ��룬��V1mL0.1molL-1H2C2O4��Һ�еμ�0.1molL-1KOH��Һ20mL��ǡ�÷�Ӧ����K2CrO4����Һ�Լ��ԣ���ʱˮ�����cˮ(H+)�����˲������V1=10mL����A����
B��b��d��ˮ�����������1��10-7mol/L��b��Ϊ������Һ����Һ�д��ڵ���غ㣬c (K+)+c(H+)=c(OH-)+c(HC2O4-)+2c(C2O42-)��������Һ�еõ�c (K+)=c(HC2O4-)+2c(C2O42-)��d��Ϊ������Һc (K+)��c(HC2O4-)+2c(C2O42-)����B����
C�������¼�ˮϡ��b���Ӧ����ҺΪKHC2O4��K2C2O4�Ļ����Һ��ϡ�ʹٽ�����������ӵ��롢���������ˮ�⣬ϡ�ͺ���ҺpH��7����C����
D�������£�C2O42-+H2O=HC2O4-+OH-��Kh1=![]() =
=![]() =2��10-10����D��ȷ��
=2��10-10����D��ȷ��
��ѡD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijԪ�ص�һ��ԭ���γɵ����ӿɱ�ʾΪ![]() n-������˵����ȷ���ǣ� ��
n-������˵����ȷ���ǣ� ��
A.![]() n-�к��е�������Ϊa+b
n-�к��е�������Ϊa+b
B.![]() n-�к��еĵ�����Ϊa-n
n-�к��еĵ�����Ϊa-n
C.Xԭ�ӵ�������Ϊa+b+n
D.һ��Xԭ�ӵ�����ԼΪ![]() g
g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ɫ��״����X�����ǵ��һ�ֽ��ȶ������M��334 g��mol��1���йػ�ѧ������ת�����£�
��X��343Kʱ����CO��������B��CO2��
��X��573Kʱ���ֽ�����A��B��
��X��ˮ��������D��
��D��HCl��B��Z��H2O��
��Z���ȷ���һ����������������Y�ȡ�
��֪A��B��Z�dz������ʡ��Է������ش�
(1)���B��Ԫ�ش��ڵ�_____________�塣
(2)д���ڵĻ�ѧ����ʽ��_______________��
(3)д��Y�ķ���ʽ��_________
(4)B��KI�������ɵ������ӵķ�����_________
(5)д���ܵ����ӷ���ʽ��____________��
(6)���ݽ�Ϊ��ȫ�ķ�Ӧ�٣�������ijһ���䷴Ӧԭ��(����)���ڹ�ҵ�Ͽ��Բⶨ������CO�ĺ������Լ�����ⶨ������________��
(7)Z���ȷ·�Ӧ�ķ���ʽһ��ΪZ���ȷ���Y���⻯���Ҳ����һ�ֿ��ܣ��仯ѧ����ʽ��______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��E ��Ϊ�л������ B �ǻ�ѧʵ���г������л�� ��������ˮ����������ζ��A �IJ����ɺ���һ������ʯ�ͻ�����չ��ˮƽ��G �������г����ĸ߷��Ӳ��ϡ��й����ʵ�ת����ϵ��ͼ����ʾ��
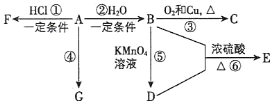
(1)д�� A �Ľṹʽ_____��B �й����ŵ�����Ϊ_____��
(2)д�����з�Ӧ�Ļ�ѧ����ʽ��
��Ӧ��____��
��Ӧ��____��
��3��ʵ�������÷�Ӧ����ȡ E��������ͼװ�ã�
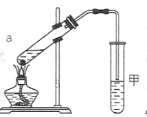
��a �Թ�����Ҫ��Ӧ�Ļ�ѧ����ʽΪ_____��
��ʵ�鿪ʼʱ���Թܼ��еĵ��ܲ�����Һ���µ�ԭ����_____�����۲쵽�Թܼ���_____ʱ����Ϊ��Ӧ������ɡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�����ܱ������н��еĿ��淴Ӧ3H2 + N2![]() 2NH3��������Ӧ�Ƿ��ȷ�Ӧ�������й�������ȷ����
2NH3��������Ӧ�Ƿ��ȷ�Ӧ�������й�������ȷ����
A.ʹ�ô�����Ϊ�˼ӿ췴Ӧ���ʣ��������Ч��
B.�����¶ȿɼӿ��淴Ӧ���ʣ������ܸı�����Ӧ����
C.N2����ʱ��H2��100%ת��ΪNH3
D.�ﵽƽ��ʱ��H2��NH3��Ũ�Ⱦ����ٸı䣬��ʱv����v����0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NF3�������������ڳ��³�ѹ������ɫ����ζ�����壬�����ӹ�ҵ��һ�������ĵ�����ʴ�����塣�ش��������⣺
��1��NF3�ĵ���ʽΪ______��NԪ�صĻ��ϼ�Ϊ______��
��2��F2��NH3ֱ�ӷ�Ӧ����NF3�Ļ�ѧ����ʽΪ______��
��3��ʵ����ģ�ҵ�����õ������NH4HF2��NH4FHF������ȡNF3������Ϊ��NiΪ�������ϵĺϽ��ں����������������������������ķ�Ӧ��������Ϊ̼�ظ֣�����Һ�ɻ��������á�
�ٵ��ʱNF3��______�����ɣ�����������������______���ѧʽ����
�ڵ����Һ����Ni����Fe��Cu�ĵ��ʼ�NH4HF2�ȣ��ɾ��������̽��л��������ã�
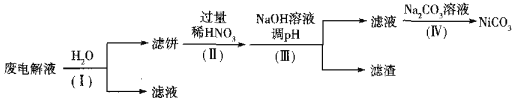
��֪��ʵ�������£����ֽ������ӿ�ʼ�����������ȫ��pH���±�
�������� | Ni2+ | Fe2+ | Cu2+ | Fe3+ |
��ʼ����ʱ��pH | 7.2 | 7.0 | 4.7 | 1.9 |
������ȫʱ��pH | 9.2 | 9.0 | 6.7 | 3.2 |
����I��Ŀ����______��������˱���Ni������������ӷ���ʽΪ______��HNO3�Ļ�ԭ����ΪNO������������pHʱ��������pHӦ���Ƶķ�Χ��______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����⻯��(NaBH4)��������ԭ�������Ϸ��ݼ������ڴ�����������ˮ��Ӧ��ȡ�������۹�����ͼ��ʾ������˵������ȷ����(����)
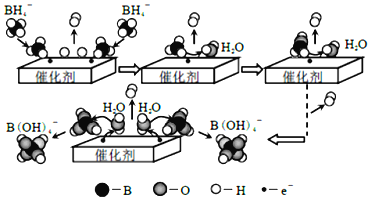
A.ˮ�ڴ˹���������ԭ��
B.����D2O����H2O����Ӧ�����ɵ������к���H2��HD��D2
C.ͨ�����ƴ����������ͱ���������Կ��������IJ�������
D.��ˮ��Ӧ�����ӷ���ʽΪ��BH4-+4H2O=B(OH)4-+4H2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Sorbicillin (��ƻ�����X)��������ù��ʱ��һ������Ʒ����ṹ��ʽ������ͼ��ʾ�� �����йػ�����X��˵����ȷ����

A. ����������̼ԭ�ӿ��ܴ���ͬһƽ��
B. 1 mol������X������2 mol Na2CO3��Ӧ
C. 1mol������X������Ũ��ˮ����ȡ����Ӧ����3molBr2
D. ������X��H2��ȫ�ӳɣ�ÿ����������к���4������̼ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͭ�ǹ㷺Ӧ�������������Ԫ�������úϽ�ij����С���ij����ͭԪ��(��25%BeO��71%CuS������FeS��SiO2)�л������ͭ���ֽ����Ĺ�ҵ�������£�
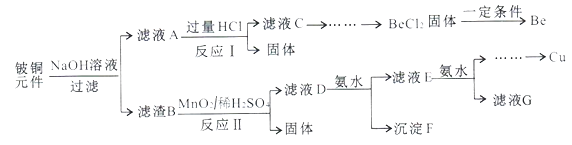
��֪��i���롢��Ԫ�ػ�ѧ�����������γ�BeO22-��ii�������²�����������ܶȻ��������±���
������ | Cu(OH)2 | Fe(OH)3 | Mn(OH)2 |
�ܶȻ�������Ksp�� | 2.2��10��20 | 4.0��10��38 | 2.1��10��13 |
(1)��NaOH��Һ�ܽ���ͭԪ������������ܽ��ʵĴ�ʩ��_______��������д�����֣���ҺA����Ҫ�ɷֳ�NaOH�⣬����_____���ѧʽ����
(2)д����ӦI�к��뻯������������ᷴӦ�����ӷ���ʽ_______��д����ӦI�����ɹ���Ļ�ѧ����ʽ��________��
(3)��ҺC�к�NaCl��BeCl2������HCl��Ϊ�ᴿBeCl2���������ʵ�鲽��˳��Ϊ____������ĸ����
a.��������İ�ˮ b.ͨ�������CO2 c.���������NaOH
d.����������HCl e.ϴ�� f.����
(4)MnO2�ܽ����������е���Ԫ������Ϊ���ʣ�д����ӦII��CuS������Ӧ�Ļ�ѧ����ʽ��______��
(5)��С���1kg���־���ͭԪ���л��յõ�433g Cu���������Cu�IJ���Ϊ_______��������λ��Ч���֣���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com