
【题目】如图所示为元素周期表的一部分,下列说法中正确的是( )
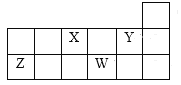
A.Z元素的最高价氧化物对应的水化物能与X的最简单气态氢化物的水溶液反应
B.X、Y、Z、W元素形成的简单离子半径由小到大的顺序为Z<X<Y<W
C.W的最简单气态氢化物的水溶液能与其最高价氧化物对应的水化物反应生成W元素对应的单质
D.X、Z两种元素的氧化物中所含化学键的类型相同
【答案】C
【解析】
从周期表结构分析,X是N,Y是F,Z是Al,W是S;
A.Al元素的最高价氧化物对应的水化物是Al(OH)3,N的最简单气态氢化物为NH3,其水溶液是氨水;
B.X、Y、Z、W元素形成的简单离子为:N3-、F-、Al3+、S2-;
C.S的最简单气态氢化物为H2S,高价氧化物对应的水化物为H2SO4;
D.N的氧化物有NO、NO2等,Al的氧化物是Al2O3;
据此解答。
A.氨水是弱碱,不能和Al(OH)3反应,A错误;
B.N3-、F-、Al3+核外都有两层电子,S2-有三层电子,S2-半径最大,N3-、F-、Al3+电子层数相同,层同看序数,序小半径大,所以S2->N3->F->Al3+,B错误;
C.H2S有还原性,浓H2SO4有强氧化性,浓硫酸能将H2S氧化成S,C正确;
D.氮氧化物中都是非金属元素,含共价键,Al2O3含离子键,D错误。
答案选C。


 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:
【题目】某化学课外小组用图装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。
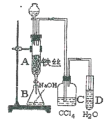
(1)写出A中反应的化学方程式_______________。
(2)观察到A中的现象是_____________________。
(3)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是________,写出有关的化学方程式______________________________。
(4)C中盛放CCl4的作用是________________。
(5)能证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入AgNO3溶液,若产生淡黄色沉淀,则能证明。另一种验证的方法是向试管D中加入_______,现象是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下是某课题组设计的合成聚酯类高分子材料的路线:
已知:同一碳原子上连两个羟基时结构不稳定,易脱水生成醛或酮
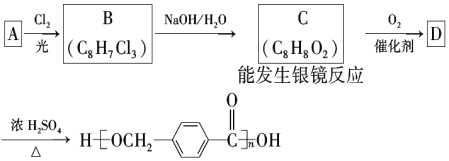
请根据以上信息回答下列问题:
(1)烃A的结构简式为________、
(2)A的化学名称为________。
(3)由B生成C的化学方程式为________。
(4)C的同分异构体中,既能与FeCl3溶液发生显色反应,又能发生银镜反应的有机物共有________种,其中在核磁共振氢谱中出现五组峰的有机物的结构简式为__________________________。
(5)D的结构简式为________,D的某同分异构体中含有苯环的碳酸二酯在酸性条件下发生水解反应的化学方程式为__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质结构与性质的说法,不正确的是( )
A.I3AsF6晶体中存在I3+离子,I3+离子的几何构型为V形
B.硫离子电子共有18种运动状态,且其2p与3p轨道能量不相等
C.12g石墨中含有σ键的物质的量为3mol
D.第四周期元素中,Ga的第一电离能低于Ca
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W四种短周期主族元素在周期表中的相对位置如图,下列说法不正确的是( )
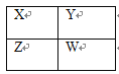
A.Y的气态氢化物的稳定性一定比W的强
B.W的原子序数可能是Y的原子序数的2倍
C.Y原子形成的简单离子半径一定比X原子形成的简单离子半径大
D.若Z元素最高价氧化物的水化物是强酸,则W元素的单质具有强氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羟基磷酸钙[Ca10(PO4)6(OH)2]具有优良的生物相容性和生物活性,它在口腔保健中具有重要作用,可以防止龋齿等,回答下列问题。
(1)Ca10(PO4)6(OH)2中,元素的电负性按由大到小的顺序依次是___。
(2)上述元素都能形成氢化物,其中PH3与同主族元素N形成的氢化物的沸点是PH3___NH3(填“>”或“<”),原因是___。
(3)碳酸钙的分解温度远高于碳酸镁,其原因是__。
(4)黑磷是磷的一种同素异形体,与石墨烯类似,其晶体结构片段如图所示:其中最小的环为6元环,每个环平均含有__个P原子。
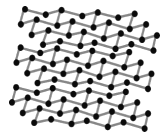
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤的液化可以合成甲醇。下列有关说法正确的是
①“气化”:C(s)+2H2O(g)===CO2(g)+2H2(g)ΔH1=+90.1kJ·mol—1
②催化液化I:CO2(g)+3H2(g)===CH3OH(g)+H2O(g)△H2=-49.0kJ·mol—1
③催化液化Ⅱ:CO2(g)+2H2(g)===CH3OH(g)+![]() O2(g)△H3=akJ·mol
O2(g)△H3=akJ·mol
A. 催化液化I的反应在高温下更容易自发进行
B. C(s)+H2O(g)+H2(g)==CH3OH(g)△H=+41.1kJ·mol—1
C. △H2>△H3
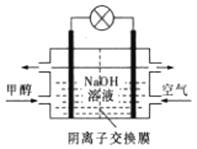
D. 如图所示为甲醇燃料电池的工作原理示意图,负极的电极反应为CH3OH-6e—+6OH—=CO2↑+5H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.6mol·L-1Fe2(SO4)3和1.2mol·L-1CuSO4的混合溶液200mL,加入一定量铁粉充分反应后,测得溶液中Fe2+与Cu2+物质的量之比为2:1,则加入铁粉的物质的量为( )
A.0.30molB.0.22molC.0.16molD.0.48mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com