
【题目】下列关于物质结构与性质的说法,不正确的是( )
A.I3AsF6晶体中存在I3+离子,I3+离子的几何构型为V形
B.硫离子电子共有18种运动状态,且其2p与3p轨道能量不相等
C.12g石墨中含有σ键的物质的量为3mol
D.第四周期元素中,Ga的第一电离能低于Ca
【答案】C
【解析】
A.晶体中存在I3+离子,I3+中心原子的价层电子对数为2+![]() =4,为sp3杂化,VSEPR模型为四面体形,中心I原子的孤电子对数为
=4,为sp3杂化,VSEPR模型为四面体形,中心I原子的孤电子对数为![]() ,I3+离子的几何构型为V形,A正确;
,I3+离子的几何构型为V形,A正确;
B.每个电子运动状态都不同,硫离子核外有18个电子,故有18种运动状态,但电子层离核越远能量越高,故2p与3p轨道能量不相等,B正确;
C.12g石墨的物质的量为12g÷12g/mol=1mol,石墨为碳原子的六元环结构,一个碳原子与另外六个碳原子间形成σ键,属于每个碳原子的σ键数目为![]() ,故1mol石墨中含有1.5molσ键,C错误;
,故1mol石墨中含有1.5molσ键,C错误;
D.Ga是31号元素,该原子核外有31个电子,其核外电子排布式为1s22s22p63s23p63d104s24p1,Ca的核外电子排布式为1s22s22p63s23p64s2,达到全满状态,较稳定,故Ga的第一电离能低于Ca,D正确;
答案选C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列离子![]() 或化学
或化学![]() 方程式正确的是
方程式正确的是
A.苯酚钠溶液中通入少量二氧化碳:![]() +H2O+CO2→
+H2O+CO2→![]() +CO32-
+CO32-
B.CH3CO18OC2H5在稀硫酸催化下水解:CH3CO18OC2H5+H2O![]() CH3COOH+C2H518OH
CH3COOH+C2H518OH
C.向CH2BrCOOH中加入足量的氢氧化钠溶液并加热:CH2BrCOOH+OH-![]() CH2BrCOO-+H2O
CH2BrCOO-+H2O
D.乙烯通入到溴水中:H2C=CH2+Br2→C2H4Br2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物甲的分子式为CxHyO2,其中氧的质量分数为20.25%,碳的质量分数为68.35%。在酸性条件下,甲水解生成乙和丙两种有机物;在相同温度和压强下,同质量的乙和丙的蒸气所占的体积相同,则甲的结构可能有
A.18种B.16种C.14种D.8种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值。下列说法正确的是( )
A.常温常压下,124 g P4中所含P—P键数目为4NA
B.100 mL 1mol·L1FeCl3溶液中所含Fe3+的数目为0.1NA
C.密闭容器中,2 mol SO2和1 mol O2催化反应后分子总数为2NA
D.标况下,11.2 L甲烷和乙烯的混合气体充分燃烧,所形成的O—H键数目为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。已知反应:
①CH4 (g) +2O2 (g) = CO2 (g) +2H2O(l) ΔH1 = a kJ mol-1
②CH4(g) + 2O2 (g) = CO2 (g) +2H2O(g) ΔH2 = bkJ mol-1
其他数据如下表所示,下列说法正确的是
化学键 | C=O | C—H | O—H | O=O |
键能/(kJ mol-1) | 798 | 413 | 463 | x |
A.ΔH1 < ΔH2
B.H2O(g) = H2O(1) ΔH=(a-b)kJ mol -1
C.当有4NA个O-H键生成时,反应放出的热量为a kJ
D.上文中x =![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示为元素周期表的一部分,下列说法中正确的是( )
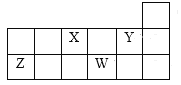
A.Z元素的最高价氧化物对应的水化物能与X的最简单气态氢化物的水溶液反应
B.X、Y、Z、W元素形成的简单离子半径由小到大的顺序为Z<X<Y<W
C.W的最简单气态氢化物的水溶液能与其最高价氧化物对应的水化物反应生成W元素对应的单质
D.X、Z两种元素的氧化物中所含化学键的类型相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.按系统命名法,化合物![]() 的名称为2,4-二乙基-6-丙基辛烷
的名称为2,4-二乙基-6-丙基辛烷
B.若两种二肽互为同分异构体,则二者的水解产物一定不相同
C.醋酸和硬脂酸互为同系物,C2H6和C9H20也一定互为同系物
D.1mol某有机物的结构简式为 通过消去反应脱去1molHCl时,能得到5种不同产物(不考虑立体异构)
通过消去反应脱去1molHCl时,能得到5种不同产物(不考虑立体异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将镁铝铁合金投入到300 mL硝酸溶液中,金属恰好完全溶解生成Mg2+、Al3+和Fe3+;硝酸全部被还原为一氧化氮,其体积为6.72 L(标准状况),当加入300 mL某浓度氢氧化钠溶液时,金属阳离子恰好全部沉淀,干燥后测得质量为27.2 g。下列有关推断正确的是( )
A. 参加反应的硝酸的物质的量为0.9 mol
B. 参加反应的金属的质量为11.9 g
C. 硝酸的物质的量浓度为3 mol·L-1
D. 氢氧化钠的物质的量浓度为6 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】COCl2(g)![]() CO(g)+Cl2(g);ΔH>0。当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO的浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是( )
CO(g)+Cl2(g);ΔH>0。当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO的浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是( )
A.①②④B.①④⑥C.②③⑥D.③⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com