
����Ŀ��ʵ��������1mol/L��NaOH��Һ240mL��
��1��ʵ�����������ƽ����___gNaOH���壻
��2������ƿ��ʹ��ǰ�IJ�����___
��3����ʵ��ʱ�������������������Һ��Ũ��ƫ�����___��
�ٳ����������ƹ����ʱ������� ������ƿ������ˮϴ�Ӻ������������ˮ��
����Һδ��ȴ��ת������ƿ�� ����ת������������Һ��δϴ���ձ���
�ݶ���ʱ���ӿ̶��ߡ���ҡ�Ⱥ�����Һ��Һ����ڿ̶��ߣ��ּ�ˮ���̶��ߡ�
��4��ȡ���Ƶ�1mol/L��NaOH��Һ10mL����ϡ�ͳ�100mL���ٴ���ȡ��10mL����10mL��Һ�����ʵ���Ũ��Ϊ____��
���𰸡�10.0 �������ƿ�Ƿ�©Һ �ۢ� 0.1mol/L
��������
��1������1mol/L��NaOH��Һ240mL��Ӧѡ��250mL������ƿ��
��2����ʹ������ƿǰӦ��������ƿ�Ƿ�©Һ��
��3���ٳ����������ƹ����ʱ�������NaOH���⣬���¹�����������
������ƿ������ˮϴ�Ӻ������������ˮ����������Һ��Ũ����Ӱ�죻
����Һδ��ȴ��ת������ƿ���¶Ƚϸߣ�����������Һ�����ƫС��
����ת������������Һ��δϴ���ձ�������������Һ��NaOH�ĺ���ƫ�ͣ�
�ݶ���ʱ���ӿ̶��ߣ�����������Һ�����ƫС��
��ҡ�Ⱥ�����Һ��Һ����ڿ̶��ߣ��ּ�ˮ���̶��ߣ�����������Һ�����ƫ��
��4������c1![]() V1=c2
V1=c2![]() V2���㡣
V2���㡣
��1������1mol/L��NaOH��Һ240mL��Ӧѡ��250mL������ƿ������ҪNaOH������=1mol/L![]() 0.25L
0.25L![]() 40g/mol=10.0g��
40g/mol=10.0g��
��2����ʹ������ƿǰӦ��������ƿ�Ƿ�©Һ��������ƿ��ת��۲��Ƿ�©ˮ���ٽ�ƿ����ת180�ȹ۲��Ƿ�©ˮ��
��3���ٳ����������ƹ����ʱ�������NaOH���⣬���¹�����������NaOH��Ũ��ƫС���ٴ���
������ƿ������ˮϴ�Ӻ������������ˮ����������Һ��Ũ����Ӱ�죬�ڴ���
����Һδ��ȴ��ת������ƿ���¶Ƚϸߣ�����������Һ�����ƫС��Ũ��ƫ����ȷ��
����ת������������Һ��δϴ���ձ�������������Һ��NaOH�ĺ���ƫ�ͣ�Ũ��ƫС���ܴ���
�ݶ���ʱ���ӿ̶��ߣ�����������Һ�����ƫС��Ũ��ƫ����ȷ��
��ҡ�Ⱥ�����Һ��Һ����ڿ̶��ߣ��ּ�ˮ���̶��ߣ�����������Һ�����ƫ��Ũ��ƫС������
��Ϊ�ۢݣ�
��4������c1![]() V1=c2
V1=c2![]() V2��c1=c2
V2��c1=c2![]() V2/V1=1mol/L
V2/V1=1mol/L![]() 10mL/100mL=0.1mol/L��
10mL/100mL=0.1mol/L��


 ��ʦ�㲦��ϵ�д�
��ʦ�㲦��ϵ�д� Ӣ�żƻ���ĩ����ϵ�д�
Ӣ�żƻ���ĩ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ��������Ĺ����У�SO2�ڽӴ����б�������ΪSO3���壬��֪�÷�ӦΪ���ȷ�Ӧ���ֽ�2 mol SO2��1 mol O2����һ�ܱ������г�ַ�Ӧ�ų�����98.3 kJ����ʱ���SO2��ת����Ϊ50%���������Ȼ�ѧ����ʽ��ȷ����
A. 2SO2(g)+O2(g)![]() 2SO3(g) ��H=196.6 kJ��mol1
2SO3(g) ��H=196.6 kJ��mol1
B. 2SO2(g)+O2(g)![]() 2SO3(g) ��H=98.3 kJ��mol1
2SO3(g) ��H=98.3 kJ��mol1
C. SO2(g)+1/2O2(g)![]() SO3(g) ��H=+98.3 kJ��mol1
SO3(g) ��H=+98.3 kJ��mol1
D. SO2(g)+1/2O2(g)![]() SO3(g) ��H=49.2 kJ��mol1
SO3(g) ��H=49.2 kJ��mol1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ����������ȼ�ϵ����ˮ����ϵͳԭ����ͼ��ʾ���������ӽ���ĤI��II�ֱ��������ӽ���Ĥ�������ӽ���Ĥ�е�һ�֣�ͼ���л���ˮ�е��л������C6H10O5��ʾ�������й�˵����ȷ����

A. a�缫Ϊ�õ�صĸ��������ӽ���ĤI�������ӽ���Ĥ
B. a�缫������Һ��������Ũ������b�缫������Һ��pH��С
C. a�缫�ĵ缫��ӦʽΪC6H10O5��24e����7H2O��6CO2����24H+
D. �м�����Na+�������ң�Cl����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����³�ѹ�£�һ��������(Cl2O)Ϊ�ػ�ɫ���壬�е�Ϊ3.8 �棬42 �����ϻ�ֽ�����Cl2��O2��Cl2O������ˮ����ˮ��Ӧ����HClO��
���Ʊ���Ʒ��
�������Ϳ���(�����뷴Ӧ)�������1��3���ͨ�뺬ˮ8%��̼�������Ʊ�Cl2O������ˮ����Cl2O(����Cl2)�Ʊ���������Һ��

��1����װ�õ�����˳��Ϊ___��___��___��________��____��___________
��2��װ��B�ж�����ݺͽ������������_��װ��C��������__��
��3���Ʊ�Cl2O�Ļ�ѧ����ʽΪ___��
��4����Ӧ�����У�װ��B�������ˮ�У���Ŀ����___��
��5���˷��������������ֱ������ˮ�Ʊ���������Һ��������Ҫ�ŵ㣬�ֱ���____��
���ⶨŨ�ȣ�
��6����֪������ɱ�FeSO4�����ʻ�ԭ��������ʵ�鷽���ⶨװ��E������Һ�д���������ʵ���Ũ�ȣ���ȡ10 mL������������Һ����ϡ����100 mL���ٴ�����ȡ��10.00 mL����ƿ�У�������10.00 mL 0.80 mol��L��1��FeSO4��Һ����ַ�Ӧ����0.050 00 mol��L��1������KMnO4��Һ�ζ����յ㣬����KMnO4��Һ24.00 mL����ԭ��������Һ��Ũ��Ϊ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�ⶨij����ͭ��Ʒ������ͭ�ĺ���(���ʲ�����ˮ������ͭԪ�أ������������ʷ�����Ӧ)����������ͼʵ�飺

��1������ʵ������з�����Ӧ�Ļ�ѧ����ʽΪ______��
��2��������֪�����г����C�ձ��вμӷ�Ӧ������ͭ����(X)�ı���ʽ___��
��3����������ʵ�����õ�����������Һ����Ҫ��������Ϊ40%������������Һ������Ϊ___��
��4����Ʒ������ͭ����������Ϊ___��
��5��D�ձ���Һ�����ʵ���������Ϊ____��
��6������ʪ��ұ��ķ���ұ����100kg������4%��ͭ����Ҫ��������ͭ������Ϊ���٣���д��������̣�____
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ��������A����֪���п��ܺ���MgCl2��CuSO4��CaCO3��FeCl3���������е����ֻ���֡�����ͼ��ʾ����ʵ�飬���ֵ�������ͼ��������������������з����ķ�Ӧ��ǡ����ȫ���У���
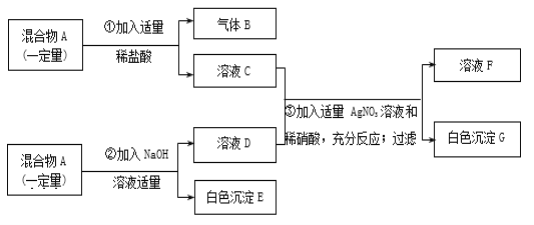
�Ը���ʵ����̺ͷ��������������жϣ���д���¿հף�
��1������B�Ļ�ѧʽΪ______��
��2���ڻ����A������������п϶������ڵ�������_____��д��ѧʽ����
��3������ҺF�У���Ҫ����___�����ʣ����д������е�������ӷ�����____��
��4��д��1�����ɰ�ɫ����G�Ļ�ѧ����ʽ��_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȼ��11.2L����״�������飬���ɶ�����̼��ˮ�����ʵ������Ƕ��٣�______
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����н�������A������ס��ҡ���������B��C��D��E��F��G������֮���ܷ������·�Ӧ(ͼ����Щ��Ӧ�IJ���ͷ�Ӧ������û��ȫ�����)��

�����������Ϣ�ش��������⣺
��1��ʵ������ȡ�����Ļ�ѧ����ʽΪ4HCl(Ũ)+MnO2![]() Cl2��+MnCl2+2H2O��MnO2��______���������Ӧ�����������ڱ�������Ϊ2.24L����������HCl�����ʵ�����_____mol
Cl2��+MnCl2+2H2O��MnO2��______���������Ӧ�����������ڱ�������Ϊ2.24L����������HCl�����ʵ�����_____mol
��2��д�����з�Ӧ�����ӷ���ʽ��
�ٽ���A��ˮ__________________________________________��
������B��������_______________________________________��
��3����������ѧ����ʽ��ʾ����G��������ϵͳ������ԭ��_______________________��
��4���û�ѧ����ʽ����F���ڷ����ڿ�����ʧЧ��ԭ��___________________________��
��5������ϸ��˿���������Ҿ���ȼ�գ�������____________________����ȼ�ղ�����ɱ�����Һ�����ˮ�п��Եõ��������������壬������������������ֱ����_________֮�䡣���������������е������ϡ���ᣬ������__________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������������Һ���й���������ȷ����
��� | �� | �� | �� | �� |
pH | 10 | 10 | 4 | 4 |
��Һ | ��ˮ | ����������Һ | ������Һ | ���� |
A. ��ͬ����ۡ�����Һ�ֱ���NaOH��ȫ��Ӧ������NaOH���ʵ������ۣ���
B. �ֱ��ˮϡ��10����������Һ��pH���٣��ڣ��ܣ���
C. �١�������Һ�������ϣ�������Һ��c��NH4������c��Cl������c��OH������c��H����
D. VaL����Һ��VbL����Һ��ϣ�������Ϊ�����Һ�����Va��Vb��������Ϻ���ҺpH��5����Va�UVb��9�U11
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com