
【题目】具有抗菌作用的白头翁素衍生物H的合成路线如下图所示:

已知:
![]()
(1)A属于芳香烃,其名称是___________________。
(2)B的结构简式是____________________________。
(3)由C生成D的化学方程式是___________________________________________。
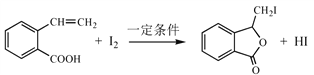
(4)由E与I2在一定条件下反应生成F的化学方程式是____________________________;此反应同时生成另外一个有机副产物且与F互为同分异构体,此有机副产物的结构简式是_____________________________________。
(5)试剂b是_____________________________。
(6)下列说法正确的是___________(选填字母序号)。
a. G存在顺反异构体
b. 由G生成H的反应是加成反应
c. 1 mol G最多可以与1 mol H2发生加成反应
d. 1 mol F或1 mol H与足量NaOH溶液反应,均消耗2 molNaOH
(7)以乙烯为起始原料,结合已知信息选用必要的无机试剂合成,写出合成 的路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)_______。
的路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)_______。
【答案】 1,2-二甲苯(邻二甲苯) ![]()
![]()
 NaOH醇溶液 bd
NaOH醇溶液 bd 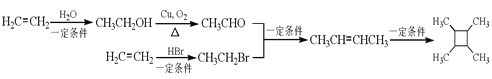
【解析】试题分析:本题考查有机推断和有机合成,涉及有机物的命名,有机物结构简式和化学方程式的书写,有机物的结构和性质,有机合成路线的设计。由A(C8H10)氧化成B(C8H8O2),B发生取代反应生成C,C的结构简式为![]() 可逆推出:A的结构简式为
可逆推出:A的结构简式为![]() ,B的结构简式为
,B的结构简式为![]() ;对比C和D(C9H9O2Br)的分子式以及C→D的反应条件,C→D为酯化反应,试剂a为CH3OH,D的结构简式为
;对比C和D(C9H9O2Br)的分子式以及C→D的反应条件,C→D为酯化反应,试剂a为CH3OH,D的结构简式为![]() 。
。![]() 与HCHO在一定条件下发生题给已知i的反应生成
与HCHO在一定条件下发生题给已知i的反应生成![]() ,
,![]() 在NaOH溶液中发生水解,水解产物酸化后获得E,E的结构简式为
在NaOH溶液中发生水解,水解产物酸化后获得E,E的结构简式为![]() ;E中含碳碳双键和羧基,E→F(C9H7O2I)发生题给已知ii的反应,对比F和G的分子式,F→G为消去反应,G→H发生题给已知iii的反应,结合H的结构简式,推出F的结构简式为
;E中含碳碳双键和羧基,E→F(C9H7O2I)发生题给已知ii的反应,对比F和G的分子式,F→G为消去反应,G→H发生题给已知iii的反应,结合H的结构简式,推出F的结构简式为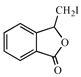 ,G的结构简式为
,G的结构简式为 。
。
(1)A属于芳香烃,A的结构简式为![]() ,A的名称为邻二甲苯(或1,2—二甲苯)。
,A的名称为邻二甲苯(或1,2—二甲苯)。
(2)B的结构简式为![]() 。
。
(3)C生成D的反应为酯化反应,反应的化学方程式为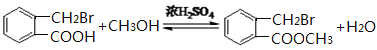 。
。
(4)E与I2在一定条件下反应生成F的化学方程式是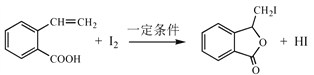 。此反应发生的是题给已知ii的反应,由于E中的碳碳双键不对称,此反应生成的另外一个与F互为同分异构体的有机副产物的结构简式是
。此反应发生的是题给已知ii的反应,由于E中的碳碳双键不对称,此反应生成的另外一个与F互为同分异构体的有机副产物的结构简式是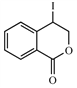 。
。
(5)在试剂b存在时F→G发生消去HI的反应,试剂b为NaOH醇溶液。
(6)a项,G的结构简式为 ,有1个碳碳双键的碳原子上连接2个H原子,G不存在顺反异构体,错误;b项,由G生成H发生题给已知iii的反应,该反应是加成反应,正确;c项,G中含有1个苯环和1个碳碳双键,苯环和碳碳双键都能与H2发生加成反应,1 mol G最多可以与4 mol H2发生加成反应,错误;d项,F中含1个酯基和1个碘原子,1 mol F能消耗2molNaOH,H中含2个酯基,1 mol H能消耗2 molNaOH,正确;答案选bd。
,有1个碳碳双键的碳原子上连接2个H原子,G不存在顺反异构体,错误;b项,由G生成H发生题给已知iii的反应,该反应是加成反应,正确;c项,G中含有1个苯环和1个碳碳双键,苯环和碳碳双键都能与H2发生加成反应,1 mol G最多可以与4 mol H2发生加成反应,错误;d项,F中含1个酯基和1个碘原子,1 mol F能消耗2molNaOH,H中含2个酯基,1 mol H能消耗2 molNaOH,正确;答案选bd。
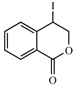
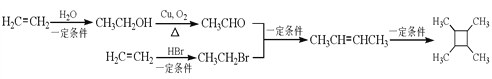
(7)根据原料CH2=CH2和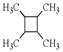 的结构简式,结合题给已知反应iii,合成
的结构简式,结合题给已知反应iii,合成 必须先合成CH3CH=CHCH3,CH3CH=CHCH3与CH2=CH2对比,碳链增长且CH3CH=CHCH3中含碳碳双键,结合题给已知反应i,则由CH2=CH2合成CH3CHO和CH3CH2Br。反应的路线为:CH2=CH2与H2O、HBr在一定条件下发生加成反应生成CH3CH2OH、CH3CH2Br,CH3CH2OH发生催化氧化生成CH3CHO,CH3CHO与CH3CH2Br在一定条件下发生题给已知i的反应生成CH3CH=CHCH3,CH3CH=CHCH3一定条件下发生题给已知iii的反应生成
必须先合成CH3CH=CHCH3,CH3CH=CHCH3与CH2=CH2对比,碳链增长且CH3CH=CHCH3中含碳碳双键,结合题给已知反应i,则由CH2=CH2合成CH3CHO和CH3CH2Br。反应的路线为:CH2=CH2与H2O、HBr在一定条件下发生加成反应生成CH3CH2OH、CH3CH2Br,CH3CH2OH发生催化氧化生成CH3CHO,CH3CHO与CH3CH2Br在一定条件下发生题给已知i的反应生成CH3CH=CHCH3,CH3CH=CHCH3一定条件下发生题给已知iii的反应生成 。合成路线可表示为:
。合成路线可表示为:
 。
。


科目:高中化学 来源: 题型:
【题目】向100mL FeBr2溶液中通入标准状况下的Cl2 3.36L,Cl2全部被还原,最终测得溶液中c(Br﹣)是c(Cl﹣ )的一半,则原FeBr2溶液的物质的量浓度(molL﹣1)是( )
A.0.75
B.1.5
C.2
D.3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在透明溶液中,下列各组离子能大量共存的是
A. HCO3-、ClO-、K+、H+ B. Na+、Fe2+、NO3-、H+
C. K+、Cu2+、Cl-、SO42- D. OH-、NH4+、Cl-、SO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温度为T时,向2.0L恒容密闭容器中充入1.0 mol PCl5,反应PCl5(g)![]() PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:下列说法正确的是
PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:下列说法正确的是
t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/ mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
A.反应在前50 s的平均速率为v(PCl3)=0.0032mol·L-1·s-1
B.保持其他条件不变,升高温度,平衡时c(PCl3)=0.11mol·L-1,则反应的△H<0
C.相同温度下,起始时向容器中充入1.0mol PCl5、0.20mol PCl3和0.20molCl2,达到平衡前v(正)>v(逆)
D.相同温度下,起始时向容器中充入2.0mol PCl3和2.0molCl2,达到平衡时,PCl3的转化率小于80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列情况会对人体健康造成较大危害的是( )
A.自来水中通入少量Cl2进行消毒杀菌
B.利用SO2的漂白作用使食品增白
C.用食醋清洗热水瓶胆内壁附着的水垢(CaCO3)
D.用小苏打(NaHCO3)发酵面团制作馒头
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通常工业上监测SO2含量是否达到排放标准的化学反应原理是SO2+ H2O2+ BaCl2= BaSO4↓+ 2HC1 ,用NA表示阿伏加德罗常数的值,下列说法不正确的是
A. 0.1 molBaCl2中所含离子总数约为0.3 NA
B. 25℃时,pH=l的HC1溶液中含有H+的数目约为0.1 NA
C. 标准状况下,17gH2O2中所含电子总数约为9 NA
D. 生成2.33gBaSO4沉淀时,吸收SO2的体积在标准状况下约为0.224L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列是部分短周期中第二、第三周期元素的原子半径及主要化合价.
元素代号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
原子半径(nm) | 0.186 | 0.160 | 0.152 | 0.153 | 0.110 | 0.099 | 0.075 | 0.074 |
主要化合价 | +1 | +2 | +1 | +3 | +5、 | +7、 | +5、 | ﹣2 |
回答下列问题:
(1)写出它们的元素名称:①②③④⑤⑥⑦⑧
(2)⑧在元素周期表中的位置是(周期、族)
(3)8个元素的最高价氧化物的水化物中,酸性最强的是(填化学式).
(4)①元素和⑥元素形成化合物的电子式是 .
(5)写出④最高价氧化物对应水化物与⑥的氢化物水溶液反应的离子方程式: .
(6)下列叙述正确的是(填字母). A.③、④处于不同周期
B.②的阳离子与⑧的阴离子的核外电子数相等
C.⑥在同主族元素中非金属性最强
D.⑤元素与⑦元素两者核电荷数之差是8
E.①与⑧形成的化合物具有两性.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,组成一种原电池.试回答下列问题(灯泡功率合适): 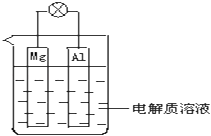
(1)电解质溶液为稀H2SO4时,灯泡(填“亮”或“不亮”,填“亮”做a题,填“不亮”做b题). a.若灯泡亮,则Mg电极上发生的反应为:;Al电极上发生的反应为:
b.若灯泡不亮,其理由为:.
(2)电解质溶液为NaOH(aq)时,灯泡(填“亮”或“不亮”,填“亮”做a题,填“不亮”做b题). a.若灯泡亮,则Mg电极上发生的反应为:;Al电极上发生的反应为:
b.若灯泡不亮
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com