
ЁОЬтФПЁПСзЫсТШрдкЯИАћЫЎЦНЩЯФмгааЇвжжЦаТаЭЙкзДВЁЖОЕФИаШОЃЌПЩгЩТШр(H)гыСзЫсдквЛЖЈЬѕМўЯТжЦЕУЃЌЫќЕФвЛжжКЯГЩЗНЗЈШчЯТЃК
вбжЊЃК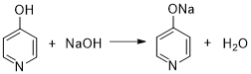
ЛиЕНЯТСаЮЪЬтЃК
(1)AжаКЌгаЕФЙйФмЭХУћГЦЮЊ_____________ЁЃ
(2)BЕФЗжзгЪНЮЊ_____________ЁЃ
(3)ЬМдзгЩЯСЌга4ИіВЛЭЌЕФдзгЛђЛљЭХЪБЃЌИУЬМдзгГЦЮЊЪжадЬМдзгЃЌHжага_________ИіЪжадЬМдзгЁЃ
(4)FЁњHЕФЗДгІРраЭЮЊ_____________ЁЃ
(5)CгыNaOHШмвКЗДгІЕФЛЏбЇЗНГЬЪНЮЊ___________________________________________ЁЃ
(6)EгыЧтЦјЗДгІКѓЕФВњЮяMЕФЗжзгЪНЮЊC9H8NOClЃЌЗћКЯЯТСаЬѕМўЕФMга__________жжЁЃ
ЂйгіFeCl3ШмвКЗЂЩњЯдЩЋЗДгІ ЂкГ§БНЛЗЭтВЛКЌЦфЫћЛЗзДНсЙЙ
ЂлБНЛЗЩЯжЛга2ИіШЁДњЛљ ЂмКЌгаЃNH2КЭ![]()
ЦфжаКЫДХЙВеёЧтЦзга5зщЗхЃЌЧвЗхУцЛ§жЎБШЮЊ1ЃК2ЃК2ЃК1ЃК2ЕФMЕФНсЙЙМђЪНЮЊ___________ЁЃ(ШЮаД2жж)
ЁОД№АИЁПЯѕЛљЁЂТШдзг C6H6NCl 1 ШЁДњЗДгІ 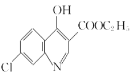 +2NaOH
+2NaOH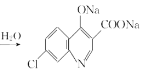 +CH3CH2OH+H2O 12
+CH3CH2OH+H2O 12 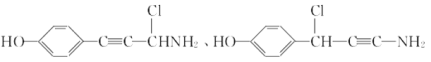
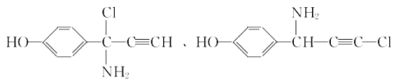
ЁОНтЮіЁП
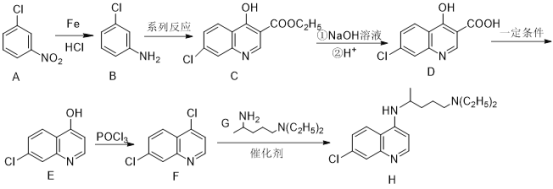
гЩЭМПЩжЊЃЌЛЏКЯЮяAЃЈ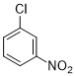 ЃЉОЙ§ЛЙдЃЌЯѕЛљБЛЛЙдГЩАБЛљЃЌЕУЕНBЃЈ
ЃЉОЙ§ЛЙдЃЌЯѕЛљБЛЛЙдГЩАБЛљЃЌЕУЕНBЃЈ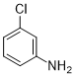 ЃЉЃЌBОЙ§ЗДгІЕУЕНCЃЈ
ЃЉЃЌBОЙ§ЗДгІЕУЕНCЃЈ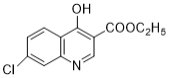 ЃЉЃЌCОЙ§NaOHНЋѕЅЛљЫЎНтКѓМгH+НЋпСрЄЛЗЩЯЕФбѕФЦБфЛиєЧЛљЕУЕНDЃЈ
ЃЉЃЌCОЙ§NaOHНЋѕЅЛљЫЎНтКѓМгH+НЋпСрЄЛЗЩЯЕФбѕФЦБфЛиєЧЛљЕУЕНDЃЈ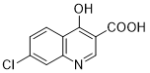 ЃЉЃЌDдквЛЖЈЬѕМўЯТЭбШЅєШЛљЃЌЕУЕНEЃЈ
ЃЉЃЌDдквЛЖЈЬѕМўЯТЭбШЅєШЛљЃЌЕУЕНEЃЈ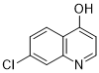 ЃЉЃЌEдкШ§ТШбѕСзЕФзїгУЯТЗЂЩњШЁДњЃЌНЋєЧЛљШЁДњЮЊТШЃЌЕУЕНFЃЈ
ЃЉЃЌEдкШ§ТШбѕСзЕФзїгУЯТЗЂЩњШЁДњЃЌНЋєЧЛљШЁДњЮЊТШЃЌЕУЕНFЃЈ ЃЉЃЌFжаЕФClгы
ЃЉЃЌFжаЕФClгы![]() жаЕФАБЛљЧтЗЂЩњШЁДњЕУЕНзюжеВњЮяТШрЁЃ
жаЕФАБЛљЧтЗЂЩњШЁДњЕУЕНзюжеВњЮяТШрЁЃ
ЃЈ1ЃЉЛЏКЯЮяAЮЊ ЃЌЙйФмЭХЪЧЯѕЛљКЭТШдзгЃЛ
ЃЌЙйФмЭХЪЧЯѕЛљКЭТШдзгЃЛ
ЃЈ2ЃЉЛЏКЯЮяBЮЊ ЃЌЗжзгЪНЪЧC6H6NClЃЛ
ЃЌЗжзгЪНЪЧC6H6NClЃЛ
ЃЈ3ЃЉЛЏКЯЮяHЕФЪжадЬМжЛга1ИіЃЌгУЁА*ЁББъМЧЃЌШчЭМ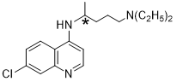 ЃЛ
ЃЛ
ЃЈ4ЃЉгЩЗжЮіПЩжЊЃЌFЁњHЕФЗДгІЮЊШЁДњЗДгІЃЛ
ЃЈ5ЃЉИљОнЗжЮіКЭвбжЊЃЌCгыNaOHШмвКЗДгІЕФЛЏбЇЗНГЬЪНЮЊЃК
 +2NaOH
+2NaOH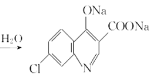 +CH3CH2OH+H2OЃЛ
+CH3CH2OH+H2OЃЛ
ЃЈ6ЃЉИљОнЬтвтЃЌЛЏКЯЮяMжагаЗгєЧЛљЁЂБНЛЗЁЂЬМЬМШ§МќЁЂАБЛљЃЌЧвБНЛЗЩЯжЛга2ИіШЁДњЛљЃЌЭЌЗжвьЙЙЬхгаЃК![]() ЁЂ
ЁЂ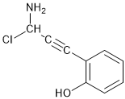 ЁЂ
ЁЂ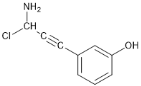 ЁЂ
ЁЂ![]() ЁЂ
ЁЂ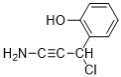 ЁЂ
ЁЂ ЁЂ
ЁЂ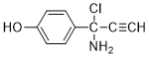 ЁЂ
ЁЂ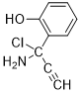 ЁЂ
ЁЂ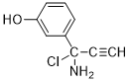 ЁЂ
ЁЂ![]() ЁЂ
ЁЂ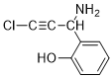 ЁЂ
ЁЂ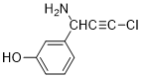 ЃЌЙВ12жжЃЛ
ЃЌЙВ12жжЃЛ
ЦфжаЃЌЦфжаКЫДХЙВеёЧтЦзга5зщЗхЃЌЧвЗхУцЛ§жЎБШЮЊ1ЃК2ЃК2ЃК1ЃК2ЕФгаЫФжжЃК![]() ЁЂ
ЁЂ![]() ЁЂ
ЁЂ ЁЂ
ЁЂ![]() ЃЛ
ЃЛ


 ХргХПкЫуЬтПЈЯЕСаД№АИ
ХргХПкЫуЬтПЈЯЕСаД№АИ ПЊаФПкЫуЬтПЈЯЕСаД№АИ
ПЊаФПкЫуЬтПЈЯЕСаД№АИ ПкЫуЬтПЈКгББЩйФъЖљЭЏГіАцЩчЯЕСаД№АИ
ПкЫуЬтПЈКгББЩйФъЖљЭЏГіАцЩчЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПАБдкЙЄХЉвЕЩњВњжагІгУЙуЗКЃЎ
ЃЈ1ЃЉИљОнШчЭМаДГіКЯГЩАБЕФШШЛЏбЇЗНГЬЪНЪЧ____________________ЃЎ

ЃЈ2ЃЉНЋ1mol N2ЃЈgЃЉКЭ3mol H2ЃЈgЃЉЗХдквЛУмБеШнЦїжаЃЌНјааЗДгІЃЌВтЕУЗДгІЗХГіЕФШШСП______ЃЈЬюЁАДѓгкЁБЁЂЁАЕШгкЁБЛђЁАаЁгкЁБЃЉ92.2kJЃЌдвђЪЧ______ЃЛШєМгШыДпЛЏМСЃЌЁїH__________ЃЈЬюЁАБфДѓЁБЁЂЁАВЛБфЁБЛђЁАБфаЁЁБЃЉЃЎ
ЃЈ3ЃЉN2H4ПЩЪгЮЊNH3ЗжзгжаЕФHБЛЉNH2ШЁДњЕФВњЮяЃЎЗЂЩфЮРаЧЪБвдN2H4ЃЈgЃЉЮЊШМСЯЁЂNO2ЮЊбѕЛЏМСЃЌЖўепЗДгІЩњГЩN2КЭH2OЃЈgЃЉЃЎ
вбжЊЃКN2ЃЈgЃЉ+2O2ЃЈgЃЉЈT2NO2ЃЈgЃЉЁїH1=+67.7kJmolЉ1
N2H4ЃЈgЃЉ+O2ЃЈgЃЉЈTN2ЃЈgЃЉ+2H2OЃЈgЃЉЁїH2=Љ534kJmolЉ1
дђ1mol N2H4гыNO2ЭъШЋЗДгІЕФШШЛЏбЇЗНГЬЪНЮЊ______________________ЃЎ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПИпЬњЫсМиЪЧвЛжжИпаЇЖрЙІФмЕФаТаЭЗЧТШТЬЩЋЯћЖОМСЃЌжївЊгУгквћЫЎДІРэЁЃЪЕбщаЁзщжЦБИИпЬњЫсМиЃЈK2FeO4ЃЉВЂЬНОПЦфаджЪЁЃ
зЪСЯЃКK2FeO4ЮЊзЯЩЋЙЬЬхЃЌЮЂШмгкKOHШмвКЃЛОпгаЧПбѕЛЏадЃЌдкЫсадЛђжаадШмвКжаПьЫйВњЩњO2ЃЌдкМюадШмвКжаНЯЮШЖЈЁЃ
(1)жЦБИK2FeO4ЃЈМаГжзАжУТдЃЉ
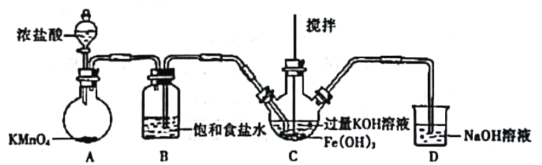
ЂйШчЭМЫљЪОЃЌAЮЊТШЦјЗЂЩњзАжУЁЃзАжУAЁЂBЁЂCЁЂDжаДцдкДэЮѓЕФЪЧ______________ЃЈЬюађКХЃЉЁЃ
ЂкCжаЕУЕНзЯЩЋЙЬЬхКЭШмвКЁЃCжаЭЈШыТШЦјЗЂЩњЗДгІЃЌЩњГЩИпЬњЫсМиЃЈK2FeO4ЃЉЕФЛЏбЇЗНГЬЪНЮЊ_______ЃЌДЫЭтCl2ЛЙПЩФмгыЙ§СПЕФKOHЗДгІЁЃ
(2)ЬНОПK2FeO4ЕФаджЪ
ЂйШЁCжазЯЩЋШмвКЃЌМгШыЯЁСђЫсЃЌВњЩњЛЦТЬЩЋЦјЬхЃЌЕУШмвКaЃЌОМьбщЦјЬхжаКЌгаCl2ЁЃЮЊжЄУїЪЧЗёK2FeO4ЃЌбѕЛЏСЫClЃЖјВњЩњCl2ЃЌЩшМЦвдЯТЗНАИЃК
ЗНАИI | ШЁЩйСПШмвКaЃЌЕЮМгKSCNШмвКжСЙ§СПЃЌШмвКГЪКьЩЋЁЃ |
ЗНАИII | гУKOHШмвКГфЗжЯДЕгCжаЫљЕУЙЬЬхЃЌдйгУKOHШмвКНЋK2FeO4ШмГіЃЌЕУЕНзЯЩЋШмвКbЁЃШЁЩйСПbЃЌЕЮМгбЮЫсЃЌгаCl2ВњЩњЁЃ |
i.гЩЗНАИIжаШмвКБфКьПЩжЊШмвКaжаКЌга__________РызгЃЌЕЋИУРызгЕФДцдкВЛФмХаЖЯвЛЖЈЪЧK2FeO4ЃЌбѕЛЏСЫCl2ЃЌвђЮЊK2FeO4ЃЌдкЫсадШмвКжаВЛЮШЖЈЃЌЧыаДГіK2FeO4дкЫсадШмвКжаЗЂЩњЗДгІЕФРызгЗНГЬЪН___________________________________ЁЃ
iiЃЎЗНАИЂђПЩжЄУїK2FeO4ЃЌбѕЛЏСЫClЃЃЎгУKOHШмвКЯДЕгЕФФПЕФЪЧ_______________ЁЃ
ЂкИљОнK2FeO4ЕФжЦБИЪЕбщЕУГіЃКбѕЛЏадCl2_____FeO42Ѓ ЃЈЬюЁАЃОЁБЛђЁАЃМЁБЃЉЃЌЖјЗНАИЂђЪЕбщБэУїЃЌCl2КЭFeO42ЃЕФбѕЛЏадЧПШѕЙиЯЕЧЁКУЯрЗДЃЌдвђЪЧ_______________ЁЃ
(3)ШєдкжЦБИзАжУCжаМгШыFe(OH)3ЕФжЪСПЮЊ14.0gЃЌГфЗжЗДгІКѓОЙ§ТЫЁЂЯДЕгЁЂИЩдяЕУK2FeO4ЙЬЬх19.3gЃЌдђK2FeO4ЕФВњТЪЮЊ______________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПДгЫсадЪДПЬЗЯвК(КЌFeCl2ЁЂCuCl2ЁЂHClМАЩйСПFeCl3)жаЛиЪеЭВЂдйЩњFeCl3ЫсадШмвКЕФЙ§ГЬжаЃЌВЛЩцМАЕФВйзїЪЧ
A.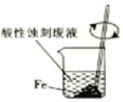 B.
B.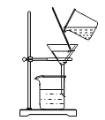
C.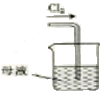 D.
D.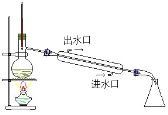
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЩшNAЮЊАЂЗќМгЕТТоГЃЪ§жЕЃЌЯТСагаЙиа№Ъіе§ШЗЕФЪЧЃЈ ЃЉ
A.НЋ78Na2O2гыЙ§СПH2OЗДгІзЊвЦЕФЕчзгЪ§ЮЊNA
B.2molSO2гы1molO2ЗДгІЩњГЩЕФSO3ЗжзгЪ§ЮЊ2NA
C.БъзМзДПіЯТ,2.24L SO3жаЫљКЌдзгЪ§ЮЊ0.4NA
D.1molCl2ВЮМгЗДгІзЊвЦЕчзгЪ§вЛЖЈЮЊ2NA
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁП300ЁцЯТЃЌдквЛШнЛ§ЮЊ2 LЕФКуШнУмБеШнЦїжаМгШы0.2 mol COКЭ0.4 mol H2ЃЌЗЂЩњШчЯТЗДгІЃКCO(g)ЃЋ2H2(g) ![]() CH3OH(g) ЁЃЯТСаИїЮяРэСПЫцЗДгІЪБМфБфЛЏЧїЪЦЕФЧњЯпВЛе§ШЗЕФЪЧ
CH3OH(g) ЁЃЯТСаИїЮяРэСПЫцЗДгІЪБМфБфЛЏЧїЪЦЕФЧњЯпВЛе§ШЗЕФЪЧ
A. 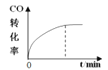 B.
B. 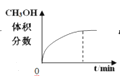
C. 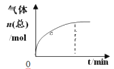 D.
D. 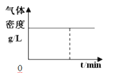
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПКЃДјжаКЌгаЗсИЛЕФЕтЃЎЮЊСЫДгКЃДјжаЬсШЁЕтЃЌФГбаОПадбЇЯАаЁзщЩшМЦВЂНјааСЫвдЯТЪЕбщЃЈБНЃЌвЛжжВЛШмгкЫЎЃЌУмЖШБШЫЎаЁЕФвКЬхЃЉЃК
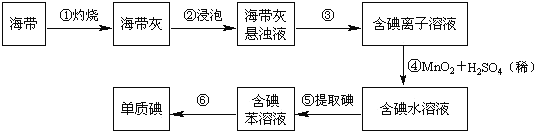
ЧыЬюаДЯТСаПеАзЃКЃЈ1ЃЉВНжшЂйзЦЩеКЃДјЪБЃЌГ§ашвЊШ§НХМмЭтЃЌЛЙашвЊгУЕНЕФЪЕбщвЧЦїЪЧЃЈДгЯТСавЧЦїжабЁГіЫљашЕФвЧЦїЃЌгУБъКХзжФИЬюаДдкПеАзДІЃЉ___________ЃЎ
AЃЎЩеБ BЃЎлслі CЃЎБэУцУѓ DЃЎФрШ§НЧ EЃЎОЦОЋЕЦ FЃЎИЩдяЦї
ЃЈ2ЃЉВНжшЂлЕФЪЕбщВйзїУћГЦЪЧ_________ЃЛВНжшЂоЕФФПЕФЪЧДгКЌЕтБНШмвКжаЗжРыГіЕЅжЪЕтКЭЛиЪеБНЃЌИУВНжшЕФЪЕбщВйзїУћГЦЪЧ_________ЃЎ
ЃЈ3ЃЉВНжшЂнЪЧнЭШЁЁЂЗжвКЃЌФГбЇЩњбЁдёгУБНРДЬсШЁЕтЕФРэгЩЪЧ________________________ЃЎ
ЃЈ4ЃЉЧыЩшМЦвЛжжМьбщЬсШЁЕтКѓЕФЫЎШмвКжаЪЧЗёЛЙКЌгаЕЅжЪЕтЕФМђЕЅЗНЗЈЪЧЃК____________ЃЎ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁП25 ЁцЪБЃЌВПЗжЮяжЪЕФЕчРыГЃЪ§ШчЯТБэЫљЪОЃК
ЛЏбЇЪН | CH3COOH | H2C2O4 | H2S |
ЕчРыГЃЪ§ | 1.8ЁС10Ѓ5 | Ka1ЃН5.4ЁС10Ѓ2 Ka2ЃН5.4ЁС10Ѓ5 | Ka1ЃН1.0ЁС10Ѓ7 Ka2ЃН7.1ЁС10Ѓ15 |
ЧыЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉШєАбCH3COOHЁЂH2C2O4ЁЂHC2O4-ЁЂH2SЁЂHS- ЖМПДзїЪЧЫс,ЦфжаЫсадзюШѕЕФЪЧ________ЁЃ
ЃЈ2ЃЉCH3COOHЁЂH2C2O4ЁЂH2SЕФЫсадгЩЧПЕНШѕЕФЫГађЮЊ_____________________ЁЃ
ЃЈ3ЃЉNaHSШмвКгыNaHC2O4ШмвКЗДгІЕФРызгЗНГЬЪНЮЊ_______________ЁЃ
ЃЈ4ЃЉ0.1 molЁЄLЃ1H2SШмвКжаc(H+)=________ molЁЄLЃ1ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯжгаФГЬњЬМКЯН№ЃЌФГЛЏбЇаЫШЄаЁзщЮЊСЫВтЖЈЬњЬМКЯН№жаЬњЕФжЪСПЗжЪ§ЃЌВЂЬНОПХЈСђЫсЕФЛЙдВњЮяЃЌЩшМЦСЫШчЭМЫљЪОЕФЪЕбщзАжУКЭЪЕбщЗНАИ(МаГжвЧЦївбЪЁТд)ЃЌЧыФуВЮгыДЫЯюЛюЖЏВЂЛиД№ЯргІЮЪЬтЃК
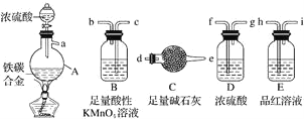
ЃЈ1ЃЉИУзАжУЕФСЌНгЫГађa___(ЬюНгПкзжФИ)ЃЌСЌНгКУзАжУКѓЃЌЪзЯШгІНјааЕФВйзїЪЧ____ЁЃ
ЃЈ2ЃЉmgЬњЬМКЯН№жаМгШыХЈH2SO4ЃЌЕуШМОЦОЋЕЦвЛЖЮЪБМфКѓЃЌгУЕЮЙмЮќШЁAжаЕФШмвКЕЮШыЕНЪЪСПЫЎжазїЮЊЪдбљЃЌЪдбљжаЫљКЌН№ЪєРызгЕФГЩЗжгавдЯТШ§жжПЩФмЃКAЃКжЛКЌгаFe3ЃЋЃЛBЃКжЛКЌгаFe2ЃЋЃЛCЃК____ЃЌШєЮЊAЃЌдђAжаЗДгІЕФЛЏбЇЗНГЬЪНЮЊ___ЃЌбщжЄCжжПЩФмЕФЪЕбщЗНЗЈ___ЁЃ
ЃЈ3ЃЉД§AжаВЛдйвнГіЦјЬхЪБЃЌЭЃжЙМгШШЃЌВ№ЯТCВЂГЦжиЃЌCдіжиbgЁЃЬњЬМКЯН№жаЬњЕФжЪСПЗжЪ§____(аДБэДяЪН)ЁЃ
ЃЈ4ЃЉФГЭЌбЇШЯЮЊРћгУДЫзАжУВтЕУЬњЕФжЪСПЗжЪ§ЦЋДѓЃЌЧыФуаДГіПЩФмЕФдвђЃК_____ЁЃ
ЃЈ5ЃЉЫцзХЗДгІЕФНјааЃЌAжаЛЙПЩФмЗЂЩњФГаЉРызгЗДгІЁЃаДГіЯргІЕФРызгЗНГЬЪН____ЁЃ
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com