
【题目】Ⅰ.如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
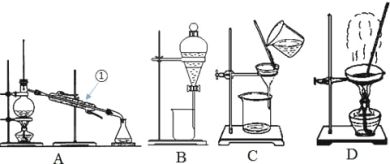
(1)从氯化钾溶液中得到氯化钾固体,选择装置____(填代表装置图的字母);
(2)分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的液体混合物,可选择装置A,该分离方法的名称为_____,装置A中①的名称是______。
(3)实验室用B装置从碘水中分离出I2,将碘水和苯注入分液漏斗中充分振荡并静置后,碘主要溶解在_____(填“上层”或“下层”)液体中,该层溶液颜色为_____,该装置在分液时为使液体顺利下滴,应进行的具体操作_____。
Ⅱ.用胆矾晶体(CuSO4·5H2O)配制0.40mol/L的CuSO4溶液240mL,回答下列问题:
(1)所需仪器为:托盘天平、药匙、烧杯、量筒、玻璃棒、胶头滴管,还需要哪些玻璃仪器才能完成该实验,请写出:_____。
(2)请写出该实验的简要的实验步骤:
①计算 ②称量胆矾_____g ③溶解 ④转移 ⑤洗涤并转移 ⑥定容 ⑦摇匀
(3)如图是该同学转移溶液的示意图,图中的错误是_____。

【答案】D 蒸馏 冷凝管 上层 紫红色 打开分液漏斗的上口活塞 250mL容量瓶 25 转移溶液时,应用玻璃棒引流
【解析】
Ⅰ. (1)蒸发可以实现易溶于水的固体和水的分离;
(2)分离沸点不同的互溶物质用蒸馏的方法;
(3)碘单质在苯中的溶解度大于在水中的溶解度,苯的密度比水小,将碘水和苯注入分液漏斗中充分振荡并静置后,上层为紫红色的碘的苯溶液,下层为水层;分液时,应打开分液漏斗的上口活塞,起到平衡气压的作用,便于液体顺利下滴;
Ⅱ. (1)实验室没有240mL容量瓶,用胆矾晶体(CuSO4·5H2O)配制0.40mol/L的CuSO4溶液240mL时,应选用250mL容量瓶;
(2)先计算250mL0.40mol/L的CuSO4溶液中硫酸铜的物质的量,再计算胆矾的质量;
(3)转移溶液时,应用玻璃棒引流。
Ⅰ.(1)蒸发可以实现易溶于水的固体和水的分离,从氯化钾溶液中得到氯化钾固体可用蒸发,D为蒸发装置,故答案为:D;
(2)分离沸点不同的互溶物质用蒸馏的方法,四氯化碳和甲苯的沸点不同,用蒸馏的方法分离,A为蒸馏装置,装置A中①的名称是冷凝管,故答案为:蒸馏;冷凝管;
(3)B为萃取分液装置,碘单质在苯中的溶解度大于在水中的溶解度,笨的密度比水小,将碘水和苯注入分液漏斗中充分振荡并静置后,上层为紫红色的碘的苯溶液,下层为水层;分液时,应打开分液漏斗的上口活塞,起到平衡气压的作用,便于液体顺利下滴,故答案为:上层;紫红色;打开分液漏斗的上口活塞;
Ⅱ.(1)实验室没有240mL容量瓶,用胆矾晶体(CuSO4·5H2O)配制0.40mol/L的CuSO4溶液240mL时,应选用250mL容量瓶,用到的仪器有托盘天平、药匙、烧杯、量筒、250mL容量瓶、玻璃棒、胶头滴管,故答案为:250mL容量瓶;
(2)250mL0.40mol/L的CuSO4溶液中硫酸铜的物质的量为0.25L×0.40mol/L=0.1mol,则称量胆矾的质量为0.1mol×250g/mol=25g,故答案为:25g;
(3)由题给图示可知,图中的错误是转移溶液时没有用玻璃棒引流,故答案为:转移溶液时,应用玻璃棒引流。


科目:高中化学 来源: 题型:
【题目】已知5KCl+KClO3+3H2SO4=3Cl2↑+3K2SO4+3H2O,下列说法不正确的是( )
A.该反应中的H2SO4只体现酸性,不体现氧化性
B.1molKClO3参加反应时有5mol电子转移
C.发生氧化反应与还原反应的氯元素的质量比为5:1
D.生成标准状况下22.4LCl2,则有![]() molKClO3被还原
molKClO3被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羰基硫(COS)可作为一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害。在恒容密闭容器中,将CO和H2S混合加热并达到下列平衡:
CO(g)+H2S(g)![]() COS(g)+H2(g) K=0.1
COS(g)+H2(g) K=0.1
反应前CO物质的量为10mol,平衡后CO物质的量为8mol。下列说法正确的是
A. 升高温度,H2S浓度增加,表明该反应是吸热反应
B. 通入CO后,正反应速率逐渐增大
C. 反应前H2S物质的量为7mol
D. CO的平衡转化率为80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,10L密闭容器中加入5.0molSO2、4.5molO2,经10min后反应达到平衡,此时容器中气体的平均分子量为58。请计算(写出计算过程):
(1)10min内SO2的转化率;
(2)容器内反应前与平衡时的压强之比(最简整数比) ;
(3)该温度下的平衡常数。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素![]() 、
、![]() 、
、![]() 、
、![]() 的原子序数依次增大,
的原子序数依次增大,![]() 的最高正价与最低负价代数和为0,
的最高正价与最低负价代数和为0,![]() 、
、![]() 、
、![]() 形成的化合物甲的结构如图所示,
形成的化合物甲的结构如图所示,![]() 在同周期中原子半径最小。下列说法正确的是( )
在同周期中原子半径最小。下列说法正确的是( )
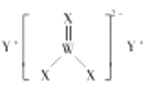
A.原子半径大小:![]()
B.电负性大小:![]()
C.![]() 、
、![]() 形成的化合物为离子化合物
形成的化合物为离子化合物
D.化合物甲中阴离子的空间构型为三角锥形
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaOH、FeCl3、AlCl3三种固体组成的混合物溶于足量水后,产生1.07g沉淀,再向所得悬浊液中逐滴加入1mol/L HCl溶液,加入HCl溶液的体积与生成沉淀的关系如图所示.

试回答:
(1)A点沉淀为______,(填化学式)B点沉淀为________.(填化学式)
(2)原固体混合物中各物质的物质的量分别是多少?___________
(3)C点处的盐酸的体积是多少毫升? ____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜铁是目前人们使用量最大的合金材料,铁及其化合物也是人们日常生活中应用广泛的一类物质。回答下列问题:
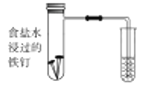
(1)下图中铁钉发生的电化学腐蚀类型是________,负极反应式为__________。
(2)实验室配置![]() 溶液时,需向溶液中滴加几滴稀硫酸,其目的是__________,
溶液时,需向溶液中滴加几滴稀硫酸,其目的是__________,![]() 溶液中离子浓度由大到小的顺序是________。
溶液中离子浓度由大到小的顺序是________。
(3)高铁盐酸是一种新型的环境消毒剂及水体净化剂,如高铁酸钾(![]() )。其中
)。其中![]() 的化合价是________,其净水过程中既表现出强氧化性,又表现了强吸附性,则
的化合价是________,其净水过程中既表现出强氧化性,又表现了强吸附性,则![]() 与水反应的离子方程式为__________。
与水反应的离子方程式为__________。
(4)羰基铁酸[![]() ]是一种二元弱酸,其第一步电离方程式为__________。
]是一种二元弱酸,其第一步电离方程式为__________。
(5)25℃时,向含![]() 的溶液中加入一定量的
的溶液中加入一定量的![]() 后,
后,![]() 恰好达到溶液平衡,测得溶液的
恰好达到溶液平衡,测得溶液的![]() ,
,![]() 。通过计算判断所得的
。通过计算判断所得的![]() 中是否含有
中是否含有![]() 杂质:________(已知:
杂质:________(已知:![]() ,
,![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方案与现象正确且能达到相应实验目的的是( )
选项 | 实验目的 | 实验方案与现象 |
A | 证明新制氯水具有酸性 | 向新制氯水中滴加紫色石蕊试液,溶液变为红色且颜色保持不变 |
B | 证明酸性条件下,氧化性:H2O2 > Fe3 + | 向Fe(NO3)2溶液中滴加用硫酸酸化的H2O2溶液,溶液变黄色 |
C | 证明同温下,溶度积常数: Ksp(AgCl)> Ksp(Ag2CrO4) | 向体积为100 mL、浓度均为0.01 mol·L-1的NaCl和Na2CrO4混合溶液中滴加 0.01 mol·L-1AgNO3溶液,先产生白色沉淀,后产生砖红色沉淀Ag2CrO4 |
D | 证明溶液X中含有 | 向溶液X中先滴加盐酸无明显现象,再滴加BaCl2溶液,出现白色沉淀 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可用KMnO4和浓盐酸反应制取氯气,其变化可表述为2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl↑2+8H2O。
(1)请将上述化学方程式改写为离子方程式:__。
(2)浓盐酸在反应中显示出来的性质是__(填编号)。
①只有还原性②还原性和酸性③只有氧化性④氧化性和酸性
(3)此反应中氧化产物是Cl2,若产生0.5molCl2,则转移电子的物质的量为__mol。
(4)用双线桥法表示该反应电子转移的方向和数目__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com