
【题目】下列生活中常见物质的俗名与化学式相对应的是( )
A. 生石灰—Ca(OH)2 B. 重晶石—BaCO3
C. 明矾—CuSO4·5H2O D. 小苏打—NaHCO3
科目:高中化学 来源: 题型:
【题目】实验是科学探究的重要途径,请根据如图回答相关问题:
(1)A的仪器名称是___________;
(2)B可收集的一种气体是___________(写化学式);
(3)用C装置制取氧气的化学方程式_______________________________;
(4)D所示的蒸发操作中,用玻璃棒搅拌的目的是_____________________;
(5)E表示铁丝在氧气中燃烧,图中实验操作可能会导致的后果是_______________;
(6)F表示称量固体氢氧化钠的质量,出现的错误是_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气中含有上百种化合物,污染物中以NO为主。请回答下列与NO相关的问题:
(1)汽车发动机工作时燃料燃烧会使氮气转化为NO。
已知:N2(g)+O2(g)=2NO(g) △H=+akJ·mol-1。NO中氮氧键键能为b kJ·mol-1、O=O键能为 c kJ·mol-1。
计算N_N的键能为____________kJ·mol-1(用含a、b、c的代数式表示)。
(2)NO和CO在一定温度和催化剂的条件下可发生反应:
2NO(g)+2CO(g)![]() N2(g)+2CO2(g) △H=-538 kJ·mol-1。
N2(g)+2CO2(g) △H=-538 kJ·mol-1。
一定温度下,向体积为2L的密闭容器中充入一定量的NO和CO,发生上述反应。反应过程中测定的部分数据见下表:
时间/min | n(NO)/mol | n(CO)/mol | n(N2)/mol | n(CO2)/mol |
0 | 0.100 | 0.200 | 0 | 0 |
4 | 0.020 | |||
6 | 0.050 | |||
8 | 0.025 |
①反应在0~4 min内的平均速率v(CO)=_____________。
②下列叙述中,能说明反应已达到平衡的是____________。
a.NO的消耗速率和CO2的生成速率相等 b.容器内的压强不再变化
c.混合气体的密度不再变化 d.N2的百分含量不再变化
③计算该温度下的平衝常数K=____________。
④8min时,其他条件不变,向该反应容器中再通入0.05molNO和0.100CO,重新达到平衡时混合气体中N2的百分含量将____________(填“减小”、“增大”或“不变” )。
(3)工业上采用电解NO的方法制备NH4NO3,其工作原理如图。X、Y皆为Pt电极,为使电解产物全部转化为NH4NO3,需补充NH3。
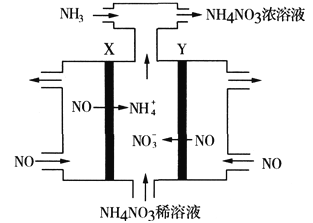
①Y电极上的电极反应式为_______________________________。
②若X电极上有11.2L(已换算成标准状况)NO发生反应,则生成NH4NO3的质量为____________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CaC2晶体的晶胞结构与NaCl晶体的相似(如图所示),但CaC2晶体中由于哑铃形的C22-存在,使晶胞沿一个方向拉长。下列关于CaC2晶体的说法中正确的是( )

A.1 个 Ca2+周围距离最近且等距离的 C22-数目为 6
B.该晶体中的阴离子与F2是等电子体
C.6.4 g CaC2晶体中含阴离子0.1 mol
D.与每个Ca2+距离相等且最近的Ca2+共有12个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA代表阿伏加德罗常数的数值,下列说法正确的是
A. 1 molNa2O2含有的阴、阳离子的数目为4NA
B. 常温常压下,0.1molC8H18所含有的共价键数目为2.5NA
C. 含有0.2 mol H2SO4的浓硫酸与足量铜反应,转移的电子数为0.2NA
D. 1 L 0.1mol/L醋酸溶液中含有的氢离子数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体混合物,由NaOH、AlCl3、MgCl2组成,将它放入足量的水中,充分搅拌后,有0.58g白色沉淀,在所得到的浊液中逐滴加入0.5mol/L的盐酸,加入盐酸的体积与生成沉淀的质量(g)关系如图所示。(假定:加入NaOH溶液后,Al3+、Mg2+转化为沉淀不存在先后顺序)

(1)沉淀的最大值,即m= ___________________g。
(2)沉淀完全溶解时,所消耗盐酸的体积a=________________mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E、F六种元素,A是周期表中原子半径最小的元素,B是电负性最大的元素,C的2p轨道中有三个未成对的单电子,F原子核外电子数是B与C核外电子数之和,D是主族元素且与E同周期,E正一价阳离子M能层电子己排满。D与B可形成离子化合物其晶胞结构如图所示。请回答下列问题: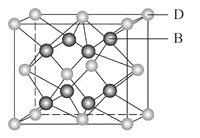
(1)E元素原子基态时的价电子排布图为___________;
(2)A2F分子中F原子的杂化类型是_______,F的氧化物FO3分子空间构型为______;
(3)CA3极易溶于水,其原因主要是________,试判断CA3溶于水后形成CA3·H2O的合理结构________(填字母代号),从氢键的形成角度回答推理依据是:___________。
(a) (b)
(b)
(4)E的晶胞常采取________堆积方式。
(5)从图中可以看出,D跟B形成的离子化合物的化学式为_________;该离子了化合物晶体的密度为ag/cm3,则晶胞的体积是_______cm3(写出表达式即可,NA表示阿伏加德罗常数的值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列流程中有机物均为芳香族化合物。H为一种酯,其合成路线如下:

已知以下信息:
① 有机物B能发生银镜反应,D的相对分子质量比C大4,E的苯环上的一溴代物有两种。
②![]()
③![]()
请回答下列问题:
(1)A的结构简式____________ ,C→D的反应类型为_____________;B中含氧官能团名称为__________ ,F中不含氧的官能团的名称为___________ ; H的结构简式为___________;
(2)E→F与F→G的顺序不能颠倒,理由是___________;
(3)F→G ①的化学方程式为___________;
(4)G还可以通过缩聚反应制得高分子材料,试写出其结构简式___________;
(5)A的同分异构体很多,其中能使FeCl3溶液显紫色有___________种,写出一种核磁共振氢谱有4组峰的分子的结构简式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱式碳酸铜[2CuCO3·Cu(OH)2]可用于制造烟火等。在较低温度下,将Cu(NO3)2饱和溶液倒入一定浓度的Na2CO3溶液中,即有碱式碳酸铜生成,同时有CO2逸出。
(1)Cu基态核外电子排布式为________。
(2)向Cu(NO3)2溶液中加入过量的氨水可生成[Cu(NH3)4]2+、1 mol[Cu(NH3)4]2+中含有σ键的数目为________。
(3)与CO2互为等电子体的一种微粒为________ (填化学式)。 NO3-的空间构型为________(文字描述)。
(4)烟火燃放过程中会产生SO2、NO等有毒气体,N、O、S 原子的第一电离能由大到小的顺序是________。
(5)Cu的一种氯化物晶体的晶胞结构如图所示,该氯化物的化学式是________。
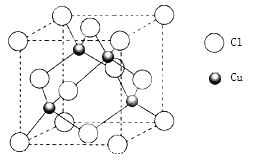
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com