
| 实验序号 | 加入n(NaCl)/mol | 测得溶液中n(Cu2+)/mol | 测得溶液中n(Cl-)/mol |
| 1 | 3 | 0 | 1 |
| 2 | 2.4 | 0 | 0.4 |
| 3 | 2 | 0 | 0 |
| 4 | 1.2 | 0 | 0 |
| 5 | 1 | 0 | 0 |
| 6 | 0.4 | 0.2 | 0 |
| 0.8mol |
| 0.2L |
| (1-0.8)mol |
| 0.2L |


科目:高中化学 来源: 题型:
| A、乙炔、乙醛、乙二醇 |
| B、乙烯、乙酸、葡萄糖 |
| C、乙烯、丁烯、环已烷 |
| D、乙烯、乙醇、丙烯酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在铁柱上铆上一些锌片 |
| B、制造铁柱时,向铁中渗入一定比例的铜制成合金 |
| C、在铁柱表面涂上一层较厚的沥青 |
| D、在铁柱表面镀锡 |
查看答案和解析>>
科目:高中化学 来源: 题型:
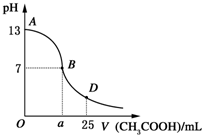 I.如图所示,向25mL 0.1mol?L-1 NaOH溶液中逐滴滴加0.2mol?L-1 CH3COOH溶液过程中溶液pH的变化曲线.请回答:
I.如图所示,向25mL 0.1mol?L-1 NaOH溶液中逐滴滴加0.2mol?L-1 CH3COOH溶液过程中溶液pH的变化曲线.请回答:| 锥形瓶中溶液 | 滴定管中溶液 | 选用指示剂 | 选用滴定管 | |
| A | 碱 | 酸 | 酚酞 | (乙) |
| B | 酸 | 碱 | 甲基橙 | (甲) |
| C | 碱 | 酸 | 酚酞 | (甲) |
| D | 酸 | 碱 | 石蕊 | (乙) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、20 mol/(L?s) |
| B、40 mol/(L?s) |
| C、60 mol/(L?s) |
| D、15 mol/(L?s) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D |
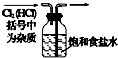 | 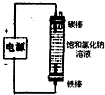 | 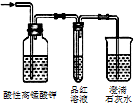 | 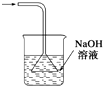 |
| 除去氯气中的杂质 | 制取84消毒液(NaClO) | 检验二氧化硫中是否混有二氧化碳 | 吸收氯化氢尾气 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、若生成1 mol Fe,则吸收的热量小于akJ |
| B、若要提高CO的转化率,则应该加入适当的过量Fe0 |
| C、若容器内压强不随时间变化,则可以判断该反应已达到化学平衡状态 |
| D、达到化学平衡状态时,若c(CO)=0.100 mol/L,则c(CO2)=0.0263 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
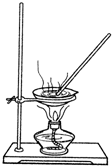 某研究性学习小组的同学设计一套方案,在实验室中制取肥皂(如图为硬脂酸甘油酯在碱性条件下水解的装置图)及甘油.已知酒精的沸点为78.5℃、甘油的沸点为290℃,硬脂酸甘油酯的沸点为260℃.
某研究性学习小组的同学设计一套方案,在实验室中制取肥皂(如图为硬脂酸甘油酯在碱性条件下水解的装置图)及甘油.已知酒精的沸点为78.5℃、甘油的沸点为290℃,硬脂酸甘油酯的沸点为260℃.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在FeSO4溶液中加入少量铁粉以防止Fe2+被氧化 |
| B、合成氨工业上,采用高压以提高NH3的产率 |
| C、实验室中常用排饱和食盐水的方法收集Cl2 |
| D、工业生产硫酸的过程中使用过量的空气以提高SO2的利用率 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com