
【题目】已知X,M都是中学教材常见元素,下列对两个离子反应通式的推断中,其中正确的是( )
(甲) XO3n﹣+Xn﹣+H+→X单质+H2O(未配平); (乙)Mm++mOH﹣=M(OH)m↓
①若n=1,则XO3n﹣中X元素为+5价,X位于周期表第ⅤA族
②若n=2,则X最高价氧化物的水化物可能与它的氢化物反应
③若m=1,则M(NO3)m溶液和氨水互滴时的现象可能不同
④若m=2,则在空气中蒸干、灼烧MSO4溶液一定能得到MSO4
⑤若m=3,则MCl3与足量氢氧化钠溶液反应一定生成M(OH)m .
A.①③
B.②③
C.①②
D.④⑤
【答案】B
【解析】解:①n=1,XO3n﹣中X元素为+5价,常见非金属元素中呈+5价的元素有第ⅤA族(氮、磷)、第ⅤⅡA族(氯、溴、碘)所以符合条件的酸根阴离子主要有:IO3﹣、ClO3﹣、BrO3﹣、NO3﹣ , 甲反应为ClO3﹣+5Cl﹣+6H+=3Cl2+3H2O,IO3﹣+5I﹣+6H+=3I2+3H2O,故①错误;
②n=2,XO3n中X元素为+4价,常见非金属元素中碳、硅、硫有+4价,结合通式只有X为硫符合题意,离子方程式为:SO32﹣+2S2﹣+6H+=3S↓+3H2O,硫的最高价含氧酸为硫酸,氢化物为硫化氢,故②正确;
③m=1,+1价阳离子有:Ag+、Na+、K+等,只有氢氧化银是难溶于水的沉淀;Ag++OH﹣=AgOH↓;氢氧化银溶于氨水,硝酸银溶液滴入氨水,生成银氨溶液无明显现象;将氨水滴入硝酸银溶液中 产生沉淀,继续滴加沉淀溶解,互滴顺序不同现象不同,故③正确;
④m=2,硫酸亚铁中+2价铁在空气中易被氧化为+3价,其化学方程式为:FeSO4+2H2OFe(OH)2+3H2O;4Fe(OH)2+O2+2H2O=4Fe(OH)3 , 2Fe(OH)3 ![]() Fe2O3+3H2O Fe2O3+3H2SO4=Fe(SO4)3+3H2O 总反应为:12FeSO4+3O2
Fe2O3+3H2O Fe2O3+3H2SO4=Fe(SO4)3+3H2O 总反应为:12FeSO4+3O2 ![]() 2Fe2O3+4Fe2(SO4)3 , 即硫酸亚铁溶液经蒸干、灼烧得到硫酸铁和氢氧化铁混合物,故④错误;
2Fe2O3+4Fe2(SO4)3 , 即硫酸亚铁溶液经蒸干、灼烧得到硫酸铁和氢氧化铁混合物,故④错误;
⑤m=3,常见金属中只有铁、铝符合条件,铝和过量氢氧化钠沉淀会溶解,故⑤错误;
故选B.
①n=1,XO3n﹣中X元素为+5价,常见非金属元素中呈+5价的元素有第ⅤA族(氮、磷)、第ⅤⅡA族(氯、溴、碘)所以符合条件的酸根阴离子主要有:IO3﹣、ClO3﹣、BrO3﹣、NO3﹣ , 甲反应为ClO3﹣+5Cl﹣+6H+=3Cl2+3H2O,IO3﹣+5I﹣+6H+=3I2+3H2O;
②n=2,XO3n﹣中X元素为+4价,常见非金属元素中碳、硅、硫有+4价,结合通式只有X为硫符合题意,离子方程式为:SO32﹣+2S2﹣+6H+=3S↓+3H2O,硫的高价含氧酸为亚硫酸,氢化物为硫化氢;
③m=1,+1价阳离子有:Ag+、Na+、K+等,只有氢氧化银是难溶于水的沉淀;Ag++OH﹣=AgOH↓;氢氧化银溶于氨水,硝酸银溶液滴入氨水,生成银氨溶液无明显现象;将氨水滴入硝酸银溶液中 产生沉淀,继续滴加沉淀溶解,互滴顺序不同现象不同;
④m=2,硫酸亚铁中+2价铁在空气中易被氧化为+3价,其化学方程式为:FeSO4+2H2OFe(OH)2+3H2O;4Fe(OH)2+O2+2H2O=4Fe(OH)3 , 2Fe(OH)3 ![]() Fe2O3+3H2O Fe2O3+3H2SO4=Fe(SO4)3+3H2O 总反应为:12FeSO4+3O2
Fe2O3+3H2O Fe2O3+3H2SO4=Fe(SO4)3+3H2O 总反应为:12FeSO4+3O2 ![]() 2Fe2O3+4Fe2(SO4)3 , 即硫酸亚铁溶液经蒸干、灼烧得到硫酸铁和氢氧化铁混合物;
2Fe2O3+4Fe2(SO4)3 , 即硫酸亚铁溶液经蒸干、灼烧得到硫酸铁和氢氧化铁混合物;
⑤m=3,常见金属中只有铁、铝符合条件.


 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.实验室从海带提取单质碘的方法是:取样→灼烧→溶解→过滤→萃取
B.用乙醇和浓H2SO4制备乙烯时,可用水浴加热控制反应的温度
C.氯离子存在时铝表面的氧化膜易被破坏,因此含盐腌制品不宜直接放在铝制容器中
D.将(NH4)2SO4、CuSO4溶液分别加入蛋白质溶液都出现沉淀,表明二者均可使蛋白质变性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定体积的Ba(OH)2溶液中,OH-的物质的量浓度为0.01mol/L。向其中逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀时,溶液中OH-的物质的量浓度为0.001mol/L。
(1)该Ba(OH)2溶液中Ba(OH)2的物质的量浓度为__________________。
(2)Ba2+恰好完全沉淀时,发生反应的离子方程式为_______________________。
(3)若反应后溶液的体积等于Ba(OH)2和NaHSO4溶液的体积之和,则Ba(OH)2溶液与NaHSO4溶液的体积比是__________。
(4)如向NaHSO4溶液中逐渐加入Ba(OH)2溶液至中性,则发生反应的离子方程式为__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,向盛有50mL pH=2的HA溶液的绝热容器中加入pH=13的NaOH溶液,加入NaOH溶液的体积(V)与所得混合溶液的温度(T)的关系如图所示.下列叙述正确的是( ) 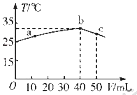
A.HA溶液的物质的量浓度为0 0l mol.L﹣1
B.b→c的过程中,温度降低的原因是溶液中发生了吸热反应
C.a→b的过程中,混合溶液中可能存在:c(A﹣)=c(Na+)
D.25℃时,HA的电离平衡常数K约为1.43×10﹣2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用芳香烃X和烯烃Y可以合成紫外线吸收剂BAD.
已知:G不能发生银镜反应,B遇FeCl3溶液显紫色,C到D的过程为引入羧基(﹣COOH)的反应.其中BAD结构简式为: 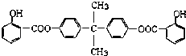
BAD的合成路线如下: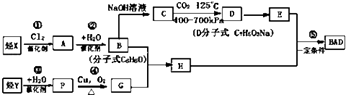
试回答下列问题:
(1)写出结构简式YD .
(2)属于加成反应的有(填数字序号) .
(3)1molBAD最多可与含molNaOH的溶液完全反应.
(4)写出方程式反应④ . F+E .
(5)E有多种同分异构体,判断符合下列要求的同分异构体数目为种.
①能发生银镜反应②遇FeCl3溶液显紫色③核磁共振氢谱图中有四个吸收峰.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g)+B(g)C(g)+D(g)发生过程中的能量变化如图,△H 表示反应的焓变.下列说法正确的是( ) 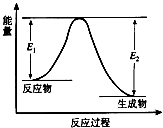
A.反应体系中加入催化剂,反应速率增大,E1减小,E2增大
B.反应体系中加入催化剂,反应速率增大,△H不变
C.△H<0,反应达到平衡时,升高温度,A的转化率增大
D.△H>0,反应达到平衡时,升高温度,A的转化率减少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】往1.0molL﹣1KI溶液中加入固体I2 , 发生反应:I2(aq)+I﹣ (aq)═I3﹣(aq)△H;I﹣的物质的量浓度c(I﹣)随温度T的变化曲线如图所示.已知反应第一次达到平衡时用时10s,则下列说法正确的是( ) 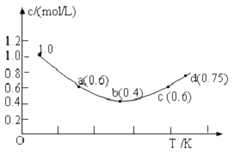
A.该反应的△H>0
B.a、c两点对应的I﹣反应速率相等
C.b点时0~10s I﹣的平均反应速率为0.04molL﹣1s﹣1
D.d点时该反应在对应温度下处于平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】检验SO2气体中是否混有CO2的方法是( )
A.先通过足量澄清石灰水,再通过足量品红溶液
B.先通过足量饱和NaHCO3溶液,再通过澄清石灰水
C.先通过足量NaOH溶液,再通过澄清石灰水
D.先通过足量酸性KMnO4溶液,再通过澄清石灰水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com