
【题目】燃煤废气中的氮氧化物(NOx)、CO2、SO2等气体,常要采用不同方法处理,以实现节能减排、废物利用等。
(1)下列为二氧化硫和氮的氧化物转化的部分环节:
①已知:2SO2(g)+O2(g)![]() 2SO3(g) △H=-196.6 kJmol-1
2SO3(g) △H=-196.6 kJmol-1
2NO(g)+O2(g)![]() 2NO2(g) △H=-113.0 kJ·mol-1
2NO2(g) △H=-113.0 kJ·mol-1
则SO2气体与NO2气体反应生成SO3气体和NO气体的热化学方程式为_________。
②一定条件下,工业上可通过下列反应实现燃煤烟气中液态硫的回收,其中Y是单质:SO2(g)+2CO(g) ![]() 2X(g)+Y(l)。为了测定在某种催化剂作用下的反应速率,某化学兴趣小组在某温度下、固定容器中用超灵敏气体传感器测得不同时间的SO2和CO浓度如下表:
2X(g)+Y(l)。为了测定在某种催化剂作用下的反应速率,某化学兴趣小组在某温度下、固定容器中用超灵敏气体传感器测得不同时间的SO2和CO浓度如下表:
时间/s | 0 | 1 | 2 | 3 | 4 |
c(SO2)/mol·L-1 | 1.00 | 0.50 | 0.23 | 3.00×10-37 | 3.00×10-37 |
c(CO)/mol·L-1 | 4.00 | 3.00 | 2.46 | 2.00 | 2.00 |
X的化学式为___________;当时间为第4 s时,2v(SO2)正____(填“>”“=”或“<”)v(X)逆。
(2)有科学家经过研究发现,在210~290℃、催化剂条件下用H2可将CO2转化生成甲醇蒸气和水蒸气。一定条件下,往2 L恒容密闭容器中充入1 mol CO2和3. 0 mol H2,在不同催化剂作用下,相同时间内CO2的转化率随温度变化如图所示:

①催化剂效果最佳的是催化剂
②此反应在a点时已达平衡状态,a点的转化率比c点高的原因是___________。已知容器内的起始压强为100 kPa,则图中c点对应温度下反应的平衡常数Kp=______(保留两位有效数字)(Kp为以分压表示的平衡常数, 分压=总压×物质的量分数)。
【答案】SO2(g) +NO2(g) ![]() SO3(g)+NO(g) △H=-41.8 kJ·mol-1 CO2 = I a点达到平衡,c点温度升高,反应是放热反应,平衡逆向,转化率减小
SO3(g)+NO(g) △H=-41.8 kJ·mol-1 CO2 = I a点达到平衡,c点温度升高,反应是放热反应,平衡逆向,转化率减小 ![]()
【解析】
⑴①根据盖斯定律,第一个方程式减去第二个方程式,再除以2得到热化学方程式;②Y为S,根据原子守恒思想得出X的化学式;当时间为第4 s时,已经达到平衡,则速率比等于计量系数比。
⑵①T3温度以前,相同温度下,催化剂Ⅰ的催化效率更高;②该反应是放热反应,温度越高,平衡逆向移动,建立三段式,先计算平衡后的压强,再根据压强平衡常数计算。
⑴①第一个方程式减去第二个方程式,再除以2得到SO2气体与NO2气体反应生成SO3气体和NO气体的热化学方程式为SO2(g) +NO2(g) ![]() SO3(g) +NO(g) △H=-41.8 kJ·mol-1;故答案为:SO2(g) +NO2(g)
SO3(g) +NO(g) △H=-41.8 kJ·mol-1;故答案为:SO2(g) +NO2(g) ![]() SO3(g) +NO(g) △H=-41.8 kJ·mol-1。
SO3(g) +NO(g) △H=-41.8 kJ·mol-1。
②Y为S,根据原子守恒思想得出X的化学式为CO2;当时间为第4 s时,已经达到平衡,则速率比等于计量系数比,故2v(SO2)正 = v(X)逆;故答案为:CO2;=。
⑵①T3温度以前,相同温度下,催化剂Ⅰ的催化效率更高;故答案为:I。
②该反应是放热反应,温度越高,平衡逆向移动,因此a点的转化率比c点高的原因是a点达到平衡,c点温度升高,反应是放热反应,平衡逆向,转化率减小;
利用压强之比等于物质的量之比,![]() ,反应后的压强为
,反应后的压强为![]() ,
,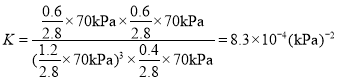 ;故答案为:a点达到平衡,c点温度升高,反应是放热反应,平衡逆向,转化率减小;
;故答案为:a点达到平衡,c点温度升高,反应是放热反应,平衡逆向,转化率减小;![]() 。
。


科目:高中化学 来源: 题型:
【题目】金属材料、无机非金属材料、有机高分子材料是人类使用的三大类基础材料,它们以各自的特点满足着人类多方面的需要。
(1)金属材料中,有一类贮氢合金能够结合氢气形成金属化合物,并在一定条件下分解释放出氢气,该贮运原理属于_______变化,钢铁是制造轮船的主要金属材料,船身外通常装上一定数目比铁更活泼的金属块以防止腐蚀,该金属块可以选择_______(选填“铜块”、“锌块”、“铅块”);
(2)无机非金属材料中,用于电子工业的高纯碳酸钙、高纯氧化钙生产流程如下:

请回答下列问题:
①硝酸钙与碳酸铵在溶液中反应,其基本反应类型为_______;
②实验室常采用_______操作进行沉淀分离;
③生产高纯碳酸钙时,选择“220℃恒温干燥”而不选择“灼烧”的原因是_______;
④高纯氧化钙生产过程中,“干燥”的主要目的是为了防止______(用化学方程式表示);
(3)有机高分子材料“玉米塑料”,因其可降解被广泛用来替代一次性泡沫塑料,“玉米塑料”的使用可减少_______污染,20世纪30年代,尼龙因其抽成细丝极像蚕丝而被推向世界,生活中可采用______方法区分尼龙和蚕丝。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,水存在H2O![]() H++OH--Q的平衡,下列叙述一定正确的是( )
H++OH--Q的平衡,下列叙述一定正确的是( )
A.向水中滴入少量稀盐酸,平衡逆向移动,Kw减小
B.将水加热,Kw增大,pH减小
C.向水中加入少量固体NH4Cl,平衡逆向移动,c(H+)降低
D.向水中加入少量固体硫酸钠,c(H+)=10-7mol/L,Kw不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】增塑剂DCHP可由环己醇制得。环己醇和DCHP的结构简式如图所示,下列说法中正确的是( )
.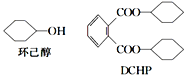
A.DCHP的分子式为C20H24O4
B.与环己醇互为同分异构体,且含醛基的结构有8种(不考虑立体异构)
C.环己醇和DCHP均属于芳香化合物
D.环己醇分子中的所有碳原子一定共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述不正确的是( ).
A.在滴有酚酞的 Na2CO3溶液中慢慢滴入BaCl2溶液至过量,溶液的红色褪去
B.往Na2CO3溶液中加水,![]() 增大
增大
C.pH相同的①NH4Cl、②NH4Al (SO4)2、③NH4HSO4三种溶液中c(NH4+):①>②>③
D.在水电离出的c(H+)=1×10-12 mol/L的溶液中,Al3+一定不可能大量存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下列各组物质制备和收集气体,能采用如图装置的是

A.浓氨水与生石灰反应制NH3
B.浓盐酸与二氧化锰反应制Cl2
C.过氧化氢溶液与二氧化锰反应制O2
D.FeS与稀硫酸反应制H2S
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯是重要的化工原料,以乙烯为原料在不同条件下可合成下列物质(部分条件未标出)。完成下列填空:

(1)乙醇能与乙酸反应生成有果香味的物质,其名称为_______,该反应类型是_________。
(2)反应⑥的化学方程式是 _________________,实验现象是 _____________。
(3)反应③用KOH的乙醇溶液处理二氯乙烯的方程式为 ________。
(4)苯乙烯中所含官能团的名称 ____________________。
(5)苯乙烯合成聚苯乙烯的化学方程式是 _______________________。
(6)以乙醇和苯乙烯为原料合成有机物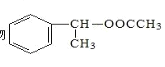 ,写出合成路线图。______
,写出合成路线图。______
合成路线流程图实例如下:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲烷作为一种新能源在化学领域应用广泛,请回答下列问题。
(1)高炉冶铁过程中,甲烷在催化反应室中产生水煤气(CO和H2)还原氧化铁,有关反应为:CH4(g)+CO2(g)===2CO(g)+2H2(g) ΔH=260 kJ·mol-1
已知:2CO(g)+O2(g)===2CO2(g)
ΔH=-566 kJ·mol-1。
则CH4与O2反应生成CO和H2的热化学方程式为_________________________________。
(2)如下图所示,装置Ⅰ为甲烷燃料电池(电解质溶液为KOH溶液),通过装置Ⅱ实现铁棒上镀铜。

①a处应通入________(填“CH4”或“O2”),b处电极上发生的电极反应式是__________________________________。
②电镀结束后,装置Ⅰ中溶液的pH________(填写“变大”“变小”或“不变”,下同),装置Ⅱ中Cu2+的物质的量浓度________。
③电镀结束后,装置Ⅰ溶液中的阴离子除了OH-以外还含有________(忽略水解)。
④在此过程中若完全反应,装置Ⅱ中阴极质量变化12.8 g,则装置Ⅰ中理论上消耗甲烷________L(标准状况下)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com