
����Ŀ��ú��ˮú�����״����Ҵ��ȶ�����Ҫ�Ļ���ԭ�ϡ�
��1��ˮú������ԭ���ǣ�C(s)+H2O(g) ![]() CO(g)+ H2(g) ��H = +131.3kJ��mol-1��
CO(g)+ H2(g) ��H = +131.3kJ��mol-1��
����˵���÷�Ӧ�ﵽƽ��״̬����______������ĸ����
A��v��(CO)= v��(H2) B��c(CO)=c(H2)
C�����������У������ܶȲ��� D�����������У�����ѹǿ����
�ڸ÷�Ӧ�ﵽ��ѧƽ��ʱ����Ҫ����ˮ������ת���ʿɲ�ȡ�Ĵ�ʩ��____������ĸ����
A������̼�����ʵ��� B������ˮ���������ʵ���
C������ѹǿ D�������¶�
��2����֪��CO(g)+ 2H2 (g)![]() CH3OH(g)�������ʵ����� CO��H2�ڴ��������·�Ӧ���ɼ״���ƽ��������������ݻ�ѹ��Ϊԭ����һ�루�����������䣩����ƽ����ϵ������Ӱ����______������ĸ����
CH3OH(g)�������ʵ����� CO��H2�ڴ��������·�Ӧ���ɼ״���ƽ��������������ݻ�ѹ��Ϊԭ����һ�루�����������䣩����ƽ����ϵ������Ӱ����______������ĸ����
A��c( H2 )���� B��CH3OH �����ʵ������� C������ƽ��ʱ![]() ��С
��С
��3����֪6H2(g)��2CO2(g) ![]() CH3CH2OH(g)��3H2O(g) �����¶�ΪT�棬�ݻ�������ܱ������У���3mol H2��1mol CO2��ϣ��ﵽƽ��ʱCO2������������Ϊa��
CH3CH2OH(g)��3H2O(g) �����¶�ΪT�棬�ݻ�������ܱ������У���3mol H2��1mol CO2��ϣ��ﵽƽ��ʱCO2������������Ϊa��
�ٴﵽƽ��ʱ��ת������(H2)����(CO2) = ______��
�ں����£�����������г���2mol He����H2��ת����______������������ ������С�� ��������������
����T�棬�ݻ��ɱ���ܱ������н�3mol H2��1mol CO2��ϣ��ﵽƽ��ʱCO2������������_______a���������� �������� ����=������
���𰸡�CD D BC 1��1 ���� ��
��������
(1)�ٴﵽƽ��״̬ʱ�����淴Ӧ������ȣ������淴Ӧ���������ָ��ͬһ����������ʾ�ķ�Ӧ���ʣ���ͬ���ʱ�ʾ�ķ�Ӧ�����뻯ѧ�����������ȡ�
�ڷ�Ӧ��C�ǹ��壬�÷�Ӧ��һ�����������������ȷ�Ӧ��
��2���÷�Ӧ��һ�����������С�ķ�Ӧ��ƽ��������������ݻ�ѹ��Ϊԭ����һ�룬ѹǿ����ƽ��������Ӧ�����ƶ���
��3��������Ӧ����ʼ��֮���뻯ѧ������֮����ȣ���Ӧ���ת������ȣ�
�ں����£�����������г���2 mol He�������ʵ�Ũ�Ȳ��䣻
������ͬ�¶Ⱥ���ʼ����ͬ�������£��ݻ��ɱ���ܱ���������ں��������൱�ڸı�ѹǿ��
(1) ��A��v��(CO)��v��(H2)����������Ӧ���ʣ�����˵�����淴Ӧ������ȣ����ж��Ƿ�ﵽƽ��״̬���ʴ���
B��c(CO)=c(H2)�뷴Ӧ��ʼ���йأ�����˵��CO��H2Ũ�ȱ��ֲ��䣬���ж��Ƿ�ﵽƽ��״̬���ʴ���
C����Ӧ��C�ǹ��壬�������غ㶨�ɿ�֪��ƽ��ǰ���������������������У������ܶ������������ܶȲ����ܱ�����Ӧ�Ѵﵽƽ��״̬������ȷ��
D��÷�Ӧ��һ�������������ķ�Ӧ�����������У�����ѹǿ����������ѹǿ�����ܱ�����Ӧ�Ѵﵽƽ��״̬������ȷ��
CD��ȷ���ʴ�Ϊ��CD��
��A����Ӧ��C�ǹ��壬����̼�����ʵ�����ƽ�ⲻ�ƶ���ˮ������ת���ʲ��䣬�ʴ���
B������ˮ���������ʵ�����ˮ����Ũ������ƽ�������ƶ�����ƽ��ʱ��ˮ����Ũ������ת���ʼ�С���ʴ���
C���÷�Ӧ��һ�������������ķ�Ӧ������ѹǿ��ƽ�����淴Ӧ�����ƶ���ˮ����ת���ʼ�С���ʴ���
D���÷�Ӧ�����ȷ�Ӧ�������¶ȣ�ƽ��������Ӧ�����ƶ���ˮ����ת����������ȷ��
D��ȷ���ʴ�Ϊ��D��
��2���÷�Ӧ��һ�����������С�ķ�Ӧ��ƽ��������������ݻ�ѹ��Ϊԭ����һ�룬ѹǿ����ƽ��������Ӧ�����ƶ���
A����ƽ��ʱ���������ʵ�����С��Ũ�����ʴ���
B����ƽ��ʱ���״������ʵ������ӣ�Ũ��������ȷ��
C����ƽ��ʱ���������ʵ�����С���״������ʵ������ӣ���![]() ��С������ȷ��
��С������ȷ��
BC��ȷ���ʴ�Ϊ��BC��
��3�����ɻ�ѧ����ʽ��֪��H2��CO2���ʵ����ı仯��֮��Ϊ3:1����ʼ3mol H2��1mol CO2���ʵ���֮��Ϊ3:1����ת���ʹ�ʽ��֪���ﵽƽ��ʱ��ת������(H2)����(CO2)Ϊ1:1���ʴ�Ϊ��1:1��
�ں����£�����������г���2mol He�������ʵ�Ũ�Ȳ��䣬��ѧ��Ӧ���ʲ��䣬ƽ�ⲻ�ƶ�����H2��ת���ʲ��䣬�ʴ�Ϊ�����䣻
�۸÷�Ӧ����һ�����������С�ķ�Ӧ������ͬ�¶Ⱥ���ʼ����ͬ�������£��ݻ��ɱ���ܱ���������ں��������൱������ѹǿ������ѹǿ��ƽ��������Ӧ�����ƶ���CO2��������������С���ʴ�Ϊ������


 Сѧѧϰ�ð���ϵ�д�
Сѧѧϰ�ð���ϵ�д� Сѧͬ�����������ܾ�ϵ�д�
Сѧͬ�����������ܾ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС������ʵ����̽�����������ʼ�ģ�ҵ��ȡƯ�ۣ����������װ�ý���ʵ�顣
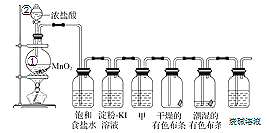
�밴Ҫ��ش��������⣺
��1�������ڵ�����___________�����з�Ӧ�����ӷ���ʽ__________
��2��Ũ���������_______��______________������ʳ��ˮ������__________
��3������KI��Һ�й۲쵽��������______________����Ӧ�����ӷ���ʽΪ________��
��4�����������ɫ��������ɫ��ʪ�����ɫ������ɫ�������ʢ�ŵ���________�������ƣ���
��5��Cl2���ռ���Һ��Ӧ��ȡ84����Һ�Ļ�ѧ����ʽΪ________��
��6������ȤС����0.2mol ����������������Ũ�����Ʊ��������������������Ƶ�������������______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������ȤС����Ҫ��18mol/L ��Ũ��������80mL3.0mol/L ϡ�����ʵ�鲽�����£��ټ�������Ũ�������� ����ȡһ�������Ũ���� ��ϡ�� �ܼ�©��ת�ơ�ϴ�� �ݶ��ݡ�ҡ�ȡ��ش��������⣺
��1������Ũ����������___mL����ȡŨ�������õ���Ͳ�Ĺ����___�������б����գ���
A��10 mL B��25mL C��50mL D��100mL
��2���ڢݲ�ʵ��IJ����Ǽ���������ƿ��ע������ˮ����̶���1-2cm��������___������ƿ�еμ�����ˮ����Һ��Ϳ̶�������Ϊֹ������ƿ������תҡ�Ȳ�װ�Լ�ƿ��
��3����������������Ƶ�ϡ����Ũ���к�Ӱ�죿������ƫ������ƫС��������Ӱ������
������ƿ������ˮϴ�Ӻ������������ˮ___��
����ת������ƿǰ�ձ�����Һδ��ȴ������___��
��ȡ��Ũ�����ϴ����Ͳ������ϴ��Һ�����ձ�___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������mgijX2���壬����Ħ������ΪM g/mol�������ӵ�������NA��ʾ����
��1������������ʵ���Ϊ________mol��
��2��һ��Xԭ�ӵ�����_________g��
��3���������ڱ�״���µ����Ϊ________L��
��4������������ˮ���γ�VL��Һ������Һ�����ʵ���Ũ��Ϊ________mol��L��1��
��5������������1Lˮ��(�����Ƿ�Ӧ)��������Һ���ܶ�Ϊ��g/cm3�������Һ�����ʵ���Ũ��Ϊ__________mol��L��1��
��6����ͬ״���£���X2�뵪���������1:4��ϣ��û��������������ܶ�Ϊ14.4��X2����Է�������Ϊ_______��
��7���������X2���ܶ�Ϊ1.25 g/L��Xԭ���������_____�����ӡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ɽ�洼[CH2OH(CHOH)4CH2OH]���������ࡢʳƷ��ˮ�ֱ��ּ���������·������ͼ��ʾ������˵���������
![]()
A.����̿��ɫ�Ĺ���Ϊ�����仯
B.��ѹ�⻯ʱ��������ȩ��ת��Ϊ�ǻ�
C.���ӽ���ʱ��ѡ�������ӽ�����֬
D.ɽ�洼����ˮ�ֱ��ּ�����Ϊ����ˮ�γ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ﮣ����������һ�ֿɳ�ŵ�أ���ط�ӦΪ2Li + O2 = Li2O2��ijﮣ�������صĹ���ԭ��ͼ���¡�����˵����ȷ����
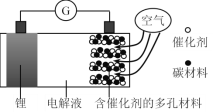
A.��ѡ���л����Һ��ˮ�Ե��Һ
B.�������Ķ�缫Ϊ��صĸ���
C.�ŵ�ʱ�����ĵ缫��ӦʽΪO2 + 2Li+ + 2e��= Li2O2
D.���ʱ﮵缫Ӧ������ӵ�Դ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�ϳ��õ�������CrO3����ˮ����H2Cr2O7��H2CrO4��ˮ��Һ�ķ����Ƹ������Һ������������Ĵ��������Ӽ�����ͨ������H2O2��͵��Һ��Cr���ĺ����������IJ��ַ�Ӧ�У�
��Cr2O72-+14H++6e=2Cr3++7H2O
��2H++2e=H2
��2CrO42-+2H+![]() Cr2O72-+H2O
Cr2O72-+H2O
��CrO42-+8H++6e=Cr+4H2O
��2H2O4e=O2+4H+
��2Cr3++7H2O6e=Cr2O72-+14H+
����˵��������ǣ�������
A.��Ӧ�٢��ڶƼ��Ϸ���
B.H2O2�����������������ֻ�ԭ��
C.���Ƽ�������52g���ʸ�ʱ����·��ת��6mol����
D.���һ��ʱ��缫������Һ��pH������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��Ԫ�����ڱ��е�ǰ�����ڣ��١���Ϊ��Ӧ��Ԫ�أ������ѡ����ʵ�Ԫ�ػش����⣺
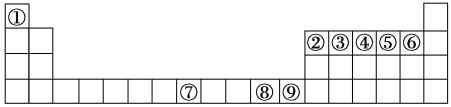
��1������Ԫ��ԭ�ӵ���Χ�����Ų�������Ԫ�����ڱ��ɻ���Ϊ�������Ԫ��λ�����ڱ���______________����
��2���ڡ�����Ԫ���γɵĻ�����Ŀռ乹��Ϊ______________��������ԭ�ӵ��ӻ��������Ϊ________��
��3��д��Ԫ�آ���Ԫ�آ��γɵ��ȶ�������Ľṹʽ_______________��
��4����Ķ���������������Ģܵ��⻯���ˮ�������õ����ӷ���ʽΪ��______��
��5��Ԫ�آ���CO���γ�X(CO)5�ͻ�����û����ﳣ���³�Һ̬���۵�Ϊ��20.5 �棬�е�Ϊ103 �棬�����ڷǼ����ܼ����ݴ˿��жϸû����ᄃ������________���壨������ͣ���
��6��Ԫ�آ�����ӵ��������ﲻ����ˮ���������ڰ�ˮ�У���������NH3���ϵ�������Ϊ________��
��7�������ߵľ����ڲ�ͬ�¶��������ֶѻ���ʽ�������ֱ���ͼ��ʾ��������������������������������ʵ�ʺ��е�ԭ�Ӹ���֮��Ϊ________��
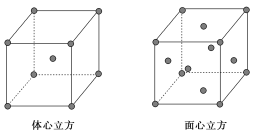
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)SO2 ���ŷ���Ҫ������ú��ȼ�գ���ҵ�ϳ��ð�ˮ���շ�����β���е� SO2����֪���չ�������ط�Ӧ���Ȼ�ѧ����ʽ���£�
��SO2(g)+NH3��H2O(aq)=NH4HSO3(aq) ��H1=a kJ/mol��
��NH3��H2O(aq)+ NH4HSO3(aq)=(NH4)2SO3(ag)+H2O(l) ��H2=b kJ/mol��
��2(NH4)2SO3(aq)+O2(g)=2(NH4)2SO4(aq) ��H3=c kJ/mol��
��Ӧ 2SO2(g)+4NH3��H2O(aq)+O2(g)=2(NH4)2SO4(aq)+2H2O(l)�� ��H=____kJ/mol��
(2)SO2���γ��������Ҫ��Ⱦ�ȼú����ԭ��Ϊ 2CaO(s)+2SO2(g)+O2(g)2CaSO4(s)���� 10L ���º����ܱ������м��� 3mol CaO����ͨ�� 2mol SO2 �� lmol O2 ����������Ӧ��2minʱ��ƽ�⣬��ʱ CaSO4 Ϊ1.8mol��02min �ڣ��� SO2 ��ʾ�ĸ÷�Ӧ������v(SO2)=____�������������ֲ��䣬��������Ӧ�ں�ѹ�����½��У��ﵽƽ��ʱ SO2 ��ת����____(����������������С������������)��
(3)NO ���ŷ���Ҫ����������β��������ԭ��Ϊ��2NO(g)+2CO(g)N2(g)+2CO2(g) ��H=746.8kJ/mol��ʵ���ã�v��=k����c2(NO)��c2(CO)��v ��=k����c(N2)��c2(CO2)(k ����k ��Ϊ���ʳ�����ֻ���¶��й�)��
�ٴﵽƽ��������¶ȣ�k������ı���____(����>����<������=��)k������ı�����
������ 1L ���ܱ������г��� 1molCO �� 1mol NO����һ���¶��´ﵽƽ��ʱ��CO ��ת����Ϊ 40%����k���Uk��=____��
(4)�����������(S2O42-)Ϊý�飬ʹ�ü�ӵ绯ѧ��Ҳ�ɴ���ȼú�����е�NO��װ����ͼ��ʾ��
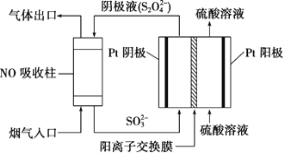
���������ĵ缫��ӦʽΪ____��
��NO ����ת�������Ҫ����Ϊ NH4+����ͨ��ʱ��·��ת���� 0.3mol e�������ͨ����������������յ� NO �ڱ�״���µ����Ϊ____mL��
(5)���� 5L Na2CO3 ��Һ�� 23.3g BaSO4 ����ȫ��ת��Ϊ BaCO3�������õ� Na2CO3 ��Һ�����ʵ���Ũ������Ϊ____��[��֪��������K(BaSO4)=1��107��K(BaCO3)=2.5��106]��(������Һ����ı仯)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com