
【题目】N2O、NO和NO2等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
(1) N2O的处理。N2O是硝酸生产中氨催化氧化的副产物,用特种催化剂能使N2O分解。NH3与O2在加热和催化剂作用下生成N2O的化学方程式为______。
(2)NO和NO2的处理。已除去N2O的硝酸尾气可用NaOH溶液吸收,主要反应为NO+NO2+2OH-=2NO2-+H2O;2NO2+2OH-=NO3-+NO2-+H2O;
①下列措施能提高尾气中NO和NO2去除率的有______(填字母)。
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
②吸收后的溶液经浓缩、结晶、过滤,得到NaNO2晶体,该晶体中的主要杂质是______(填化学式);吸收后排放的尾气中含量较高的氮氧化物是______(填化学式)。
【答案】2NH3+2O2 ![]() N2O+3H2O BC NaNO3 NO
N2O+3H2O BC NaNO3 NO
【解析】
(1)NH3与O2在加热和催化剂作用下生成N2O,类似于生成NO的反应,同时生成水;
(2)NO2与NaOH反应生成亚硝酸钠、硝酸钠和水,NO和NO2一起与氢氧化钠反应生成亚硝酸钠和水,据此书写方程式;
①提高尾气中NO和NO2去除率,应是气体与氢氧化钠溶液充分接触而反应;
②反应生成NaNO2和NaNO3;如NO的含量比NO2大,则尾气中含有NO。
(1)NH3与O2在加热和催化剂作用下发生氧化还原反应生成N2O,根据得失电子守恒和原子守恒可知反应有水生成,配平化学方程式,得反应的化学方程式为2NH3+2O2 ![]() N2O+3H2O;
N2O+3H2O;
(2)NO2与NaOH反应生成亚硝酸钠、硝酸钠和水,NO和NO2一起与氢氧化钠反应生成亚硝酸钠和水,反应离子方程式为:2NO2+2OH-=NO2-+NO3-+H2O、NO+NO2+2OH-=2NO2-+H2O;
①A. 加快通入尾气的速率,气体不能充分反应,不能提高尾气中NO和NO2的去除率,A不符合题意;
B. 采用气、液逆流的方式吸收尾气,可使气液充分接触,能提高尾气中NO和NO2的去除率,B符合题意;
C. 定期补充适量的NaOH溶液可增大反应物浓度,能提高尾气中NO和NO2的去除率,C符合题意;
故合理选项是BC;
②反应生成NaNO2和NaNO3,则含有的杂质为NaNO3,如NO的含量比NO2大,则尾气中含有NO。


科目:高中化学 来源: 题型:
【题目】N2O和CO是常见的环境污染气体。
(1)对于反应N2O(g)+CO(g)![]() CO2(g)+N2(g)来说,“Fe+”可作为此反应的催化剂。其总反应分两步进行:
CO2(g)+N2(g)来说,“Fe+”可作为此反应的催化剂。其总反应分两步进行:
第一步为Fe++N2O![]() FeO++N2;则第二步为____________________(写化学方程式)。
FeO++N2;则第二步为____________________(写化学方程式)。
已知第二步反应几乎不影响总反应达到平衡所用的时间,由此推知,第一步反应的活化能_________(填“大于”“小于”或“等于”)第二步反应的活化能。
(2)在四个不同容积的恒容密闭容器中按图甲充入相应的气体,发生反应:2N2O(g)![]() 2N2(g)+O2(g),容器I、II、III中N2O的平衡转化率如图乙所示:
2N2(g)+O2(g),容器I、II、III中N2O的平衡转化率如图乙所示:
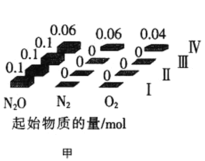
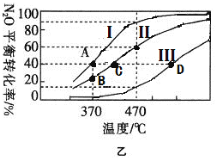
①该反应的△H_____0(填“>”或“<”)。
②若容器I的体积为2L,反应在370℃下进行,20s后达到平衡,则0~20s内容器I中用O2表示的反应速率为_________。B点对应的平衡常数k=________(保留两位有效数字)。
③图中A、C、D三点容器内气体密度由大到小的顺序是 _______________。
④若容器Ⅳ体积为1L,反应在370℃下进行,则起始时反应_________移动(填“向正反应方向”、“向逆反应方向”或“不”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )
A.1mol![]() 发生氧化还原反应时,转移的电子数目一定为2NA
发生氧化还原反应时,转移的电子数目一定为2NA
B.向含有1mol![]() 的溶液中通入足量的氯气完全反应时,转移的电子数目为2NA
的溶液中通入足量的氯气完全反应时,转移的电子数目为2NA
C.常温常压下,14g由![]() 与
与![]() 组成的混合气体含有的原子数目为NA
组成的混合气体含有的原子数目为NA
D.![]() 的浓硫酸与足量铜在加热条件下反应,生成
的浓硫酸与足量铜在加热条件下反应,生成![]() 分子的数目为0.46NA
分子的数目为0.46NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A(C2H2)是基本有机化工原料。由A制备高分子降解塑料(PVB)和IR的合成路线(部分反应条件略去)如图所示:
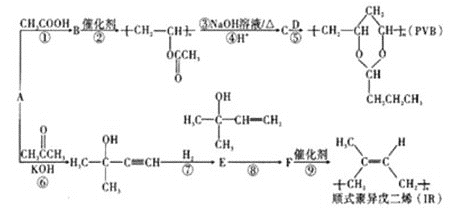
已知:①RCHO+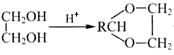 +H2O;
+H2O;
②RBr![]() RCOOH。
RCOOH。
试回答下列问题:
(1)过程①的反应类型为___,B中含氧官能团的名称是___。
(2)反应⑧的化学方程式为___。反应③的化学方程式为___。
(3)关于过程②,下列说法正确的是___(填序号)。
a.反应②属于缩聚反应
b.生成的高分子化合物还能与溴水反应而使其褪色
c.该高分子链节具有和其单体完全一样的结构
d.生成的高分子材料具有热塑性,且为混合物
e.通过质谱仪测得该高分子的平均相对分子质量为30444,可推知其n约为354
(4)F分子中最多有___个原子共平面,D的结构简式是___。
(5)G与E互为同分异构体,则G的所有同分异构体中含有碳碳双键的结构(包含E在内且不考虑顺反异构)共有___种。(已知碳碳双键与羟基直接相连不稳定,不考虑)
(6)利用题目信息,以乙烯为起始原料,选用必要的无机试剂合成丁二酸乙二酯,写出合成路线___(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】影响化学反应速率的因素很多,某课外兴趣小组用实验方法进行探究。
(1)取等物质的量浓度、等体积的H2O2溶液分别进行H2O2的分解实验,实验报告如下表所示(现象和结论略)。
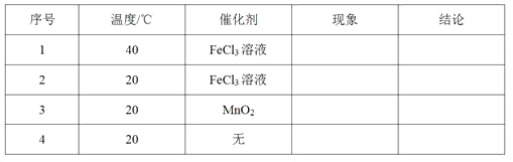
①实验1、2研究的是__________对H2O2分解速率的影响。
②实验2、3的目的是_______________对H2O2分解速率的影响。
(2)查文献可知,Cu2+对H2O2分解也有催化作用,为比较Fe3+、Cu2+对H2O2分解的催化效果,该小组的同学分别设计了如图甲、乙所示的实验。回答相关问题:
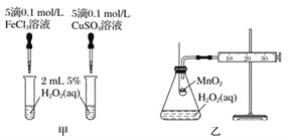
①定性如图甲可通过观察_______,定性比较得出结论。有同学提出将CuSO4溶液改为CuCl2溶液更合理,其理由是_________。
②定量如图乙所示,实验时以收集到40 mL气体为准,忽略其他可能影响实验的因素,实验中需要测量的数据是__________。
(3)酸性高锰酸钾溶液和草酸溶液可发生反应:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+8H2O+10CO2↑,实验时发现开始反应速率较慢,溶液褪色不明显,但一段时间后突然褪色,反应速率明显加快。对此展开讨论:
①某同学认为KMnO4与H2C2O4的反应是______热反应,导致_______________;
②从影响化学反应速率的因素看,你认为还可能是________的影响。要证明你的猜想,实验方案是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在-50℃时液氨中存在着下列平衡:2NH3(液)![]() NH4++NH2-,两种离子的平衡浓度均为1.0×10-15mol·L-1。以下有关-50℃时离子积的叙述中正确的是( )
NH4++NH2-,两种离子的平衡浓度均为1.0×10-15mol·L-1。以下有关-50℃时离子积的叙述中正确的是( )
A. 离子积为1.0×10-15
B. 离子积为1.0×10-30
C. 向液氨中加入氨基钠(NaNH2),液氨的离子积增大
D. 向液氨中加入NH4Cl,c(NH4+)增大,离子积的数值也随之增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数,下列说法错误的是 ( )
A.28克氮气所含的原子数目为2NA;
B.在标况下,0.5NA氯分子所占体积约是11.2L;
C.只有在标况下NA氧气分子的物质的量才是1mol;
D.在70℃、1×105Pa下,46克NO2与标况下46克四氧化二氮均含有3NA原子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组热化学方程式中,ΔH1>ΔH2的是( )
①C(s)+O2(g)=CO2(g) ΔH1;C(s)+![]() O2(g)=CO(g) ΔH2
O2(g)=CO(g) ΔH2
②S(g)+O2(g)==SO2(g) ΔH1;S(s)+O2(g)=SO2(g) ΔH2
③H2(g)+![]() O2(g)=H2O(l) ΔH1;2H2(g)+O2(g)=2H2O(l) ΔH2
O2(g)=H2O(l) ΔH1;2H2(g)+O2(g)=2H2O(l) ΔH2
④CaCO3(s)=CaO(s)+CO2(g) ΔH1;CaO(s)+H2O(l)=Ca(OH)2(s) ΔH2
A.①
B.②③④
C.③④
D.①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在酸性溶液中,碘酸钾(KIO3)和亚硫酸钠可发生如下反应:2IO3-+5SO32-+2H+=I2+5SO42-+H2O,生成的I2可以用淀粉溶液检验,根据反应溶液出现蓝色所需的时间来衡量该反应的速率。某同学设计实验如下表所示:
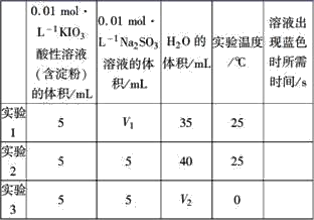
该实验的目的是_________;表中V2=_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com