
【题目】写出下列反应的离子方程式
(1)二氧化碳通入澄清石灰水_________________________________
(2)小苏打除胃酸___________________________________________
(3)硫酸和氢氧化钠反应_____________________________________
(4)金属铜和硝酸银溶液反应_________________________________
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源: 题型:
【题目】CH4—CO2催化重整不仅可以得到合成气(CO和H2),还对温室气体的减排具有重要意义。
(1)在标准状态下,由元素最稳定的单质生成1mol纯化合物时的反应热称为该化合物的标准摩尔生成焓。各物质的标准摩尔生成焓如表:

则制备合成气的反应CH4(g)+CO2(g)![]() 2CO(g)+2H2(g)在标准状态下的反应热ΔH=___kJ/mol。
2CO(g)+2H2(g)在标准状态下的反应热ΔH=___kJ/mol。
(2)在刚性容器中,当投料比![]() =1.0时,CO2的平衡转化率(α)与温度(T)、初始压强(p)的关系如图所示。
=1.0时,CO2的平衡转化率(α)与温度(T)、初始压强(p)的关系如图所示。
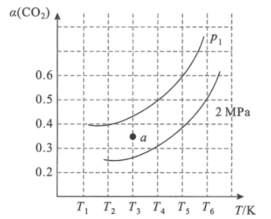
①由图可知:压强P1___2MPa(填“>”、“<”或“=”),理由是___。
②当温度为T3、压强为p1时,a点的v正___v逆(填“>”、“<”或“=”)。
③若起始时提高投料比![]() ,则CO2的平衡转化率将___(填“升高”或“降低”)。
,则CO2的平衡转化率将___(填“升高”或“降低”)。
④起始时向容器中加入1molCH4和1molCO2,在温度为T6。、初始压强为2MPa时反应,该反应的Kp=___(MPa)2。
(3)该催化重整过程中有副产物碳生成,碳的积累会严重影响催化剂的活性。某研究小组计算和模拟实验表明积碳量(催化剂表面碳的质量与催化剂的质量之比)与投料比、温度的关系如图。
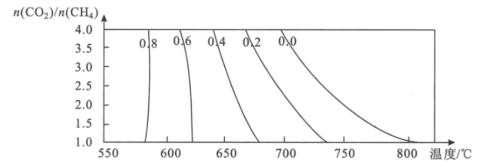
当投料比![]() =2.0时,要使积碳量最小,应调节温度为___℃。
=2.0时,要使积碳量最小,应调节温度为___℃。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 1mol任何气体的体积都是22.4L
B. 同温同压下两种气体,只要它们的分子数相同,所占体积也一定相同
C. 在标准状况下,体积为22.4L的物质都是1mol
D. 在非标准状况下,1mol任何气体的体积不可能是22.4L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用“银-Ferrozine”法测室内甲醛含量的原理为:

已知:吸光度与溶液中有色物质的浓度成正比
下列说法正确的是
A. 反应①中参与反应的HCHO为30g时转移电子2mol
B. 可用双氧水检验反应②后的溶液中是否存在Fe3+
C. 生成44.8 LCO2时反应②中参加反应的Ag一定为8mol
D. 理论上测得溶液吸光度越高,HCHO含量也越高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图某工厂用NO气体制取NH4NO3溶液,下列说法正确的是
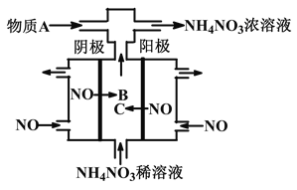
A. 阳极的电极反应式为:NO-3e-+2H2O=NO2-+4H+
B. 物质B与物质C是同一种物质
C. A物质可为氨气
D. 阴、阳两极转移的电子数之比为5∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏伽德罗常数,下列说法中正确的是( )
A.18g水含有电子数为9NA
B.常温常压下,71g氯气含有氯原子数为NA
C.标准状况下,22.4L氢气含有的氢原子数为2NA
D.1mol冰醋酸溶于水中,所得溶液中H+ 数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿比朵尔是抗击新型冠状病毒的潜在用药,其结构简式如图示,下列有关说法正确的是
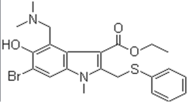
A.含氧官能团的名称:羟基、羧基
B.分子式:C22H25BrN2O3S
C.能使酸性高锰酸钾溶液、溴水褪色,且褪色原理相同
D.1mol该物质最多与6molH2发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室要配制0.40mol·L-1 Na2CO3溶液100mL。
⑴请将配制该溶液的实验步骤补充完整。
①计算,需Na2CO3固体的质量为__________g;
②把称量好的Na2CO3固体倒入小烧杯中,加入适量的蒸馏水溶解、冷却至室温;
③把②所得溶液小心引流到100mL容量瓶中;
④继续向容量瓶中加蒸馏水至液面接近容量瓶的刻度线1~2cm处,改用胶头滴管滴加蒸馏水至______________________________________________;
⑤用少量蒸馏水洗涤烧杯内壁和玻璃棒_________次,并将每次洗涤的溶液都注入容量瓶,轻轻摇匀;
⑥将容量瓶的瓶塞盖好,反复上下颠倒、摇匀。
⑵容量瓶使用前需____________________________________。
⑶配制该溶液的正确顺序是______________________________(填序号)。
⑷若出现如下情况,其中将引起所配溶液浓度偏低的是__________(填序号)。
①未洗涤烧杯内壁和玻璃棒
②定容时,俯视容量瓶的刻度线
③转移前,容量瓶中含有少量蒸馏水
④加水定容时不慎超过了刻度线,再用胶头滴管吸出多余的液体
⑸上述配制好的溶液导入试剂瓶后需贴上标签,请你填写如图标签的内容_______________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cl2和H2O2是高中阶段最常见的两种氧化剂,经查阅资料Cl2氧化能力强于H2O2,能将H2O2氧化。为了验证该结论,学生设计了如下图所示的实验装置进行实验(夹持装置略去)。请回答下列问题。
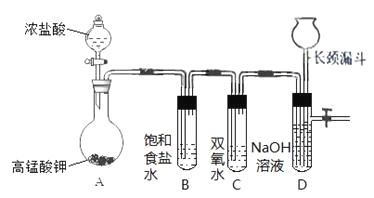
(1)A中的方程式为_____________________(用单线桥标电子转移方向与数目);
(2)试管B中饱和食盐水的作用__________________;
(3)试管C中加入5mL 30% 双氧水,发生反应的化学方程式____________________;
(4)试管D中充满10% NaOH溶液,NaOH溶液的作用是__________________;
(5)将浓盐酸注入圆底烧瓶A,当装置中的空气基本排尽后关闭止水夹,反应一段时间后试管D中的现象为_____________________________________________,试管D中的气体检验方法为____________;
(6)有的同学对上述实验中D试管中的气体来源产生质疑,你认为可能的来源有:_____________(用方程式回答)。对于质疑可以采用对比实验来解决。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com