
【题目】(I)无水CoCl2为深蓝色,吸水后变为粉红色的水合物,水合物受热后又变成无水CoCl2,故常在实验室中用作吸湿剂和空气湿度指示剂。

现有65g无水CoCl2,吸水后变成CoCl2·xH2O 119g。
(1)水合物中x=______;
(2)若该化合物中Co2+的配位数为6,而且经测定得知内界和外界占有Cl-的个数比为1:1,则其化学式可表示为:______
(Ⅱ)在极性分子中,正电荷中心同负电荷中心间的距离称为偶极长,通常用d表示。极性分子的极性强弱同偶极长和正(或负)电荷重心的电量(q)有关,一般用偶极矩(μ)来衡量。分子的偶极矩定义为偶极长和偶极上一端电荷电量的乘积,即μ=d·q。试回答以下问题:
(3)治癌药Pt(NH3)2Cl2具有平面四边形结构,Pt处在四边形中心,NH3和Cl分别处在四边形的4个角上。已知该化合物有两种异构体,棕黄色者μ>0,淡黄色者μ=0。
①试在方框中画出两种异构体的构型图:_________;___________________

②该化合物的两种异构体在水中溶解度较大的是___________________(填“棕黄色者”或“淡黄色者”)。
【答案】 6 [CoCl(H2O)5]Cl·H2O 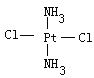
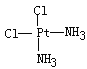 棕黄色者
棕黄色者
【解析】本题考查配位键及配位化合物,同分异构体等知识,必须审清题目信息,并与所学知识结合起来进行解答。
(1)xH2O+CoCl2=CoCl2·xH2O △m
131+18x 18x
119g (119-65)g
(131+18x):18x=119:(119-65),解得:x=6。
(2)该化合物CoCl2·6H2O中Co2+配位数为6,而且经定量测定得知内界和外界占有Cl-个数为1:1,即各有1个氯离子,则内界中含有1个氯离子和5个水分子,外界有1个氯离子,另外还有1个结晶水,所以化学式可表示为[CoCl(H2O)5]Cl·H2O。
(3)①根据题意,Pt(NH3)2Cl2具有平面四边形结构,若μ=0,则为非极性分子,NH3和Cl分别对称分布在四边形的4个角上,即正负电荷重心重合,所以淡黄色者是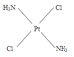 ;若μ>0,则为极性分子,NH3和Cl在四边形的4个角上的分布是不对称的,即正负电荷重心不重合,所以棕黄色者是
;若μ>0,则为极性分子,NH3和Cl在四边形的4个角上的分布是不对称的,即正负电荷重心不重合,所以棕黄色者是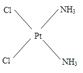 ;②根据“相似相溶”规律,水是极性分子,因此极性分子的溶质易溶解在水中,即在水中溶解度较大的是棕黄色者。
;②根据“相似相溶”规律,水是极性分子,因此极性分子的溶质易溶解在水中,即在水中溶解度较大的是棕黄色者。


科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 乙烯和丁烷都能发生加成反应 B. 乙醇和乙酸都能与NaHCO3反应
C. 糖类和蛋白质都属于生物高分子 D. 油脂和乙酸乙酯都能发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列反应的离子方程式:
(1)KOH溶液和HCl溶液反应____________________。
(2)Ba(OH)2溶液和H2SO4溶液反_____________________________________。
(3)Na2CO3溶液和HNO3溶液反应____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取一定质量的Cu2O和CuO混合粉末,将其均匀混合后分成两等份,取其中一份用足量的氢气还原,测得反应后固体质量减少6.40g,另一份中加入500mL稀硝酸,固体恰好完全溶解,且同时收集到标准状况下NO气体4.48L,则所用硝酸的物质的量浓度为
A. 3.6mol/L B. 3.2mol/L C. 2.8mol/L D. 2.4mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】3H、14C、14N、16O、32S等在科学研究中应用广泛,下列针对它们的说法正确的是
A. 14C和14N互为同位素
B. 3H的核外电子比2H多一个
C. 16O和32S原子核内的中子数相等
D. 等物质的量的14N216O和14C16O2所含质子数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸亚乙烯酯结构如右图所示。下列有关该物质的说法正确的是( )

A. 分子中含6个σ键
B. 分子式为C3H2O3
C. 分子中只有极性键
D. 8.6 g该物质完全燃烧得到6.72 L CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳有多种同素异形体,其中石墨烯与金刚石的晶体结构如图所示:

(1)金刚石、石墨、C60、碳纳米管等都是碳元素的单质形式,它们互为_____________。
(2)在石墨烯晶体中,每个C原子连接_____个六元环,每个六元环占有____个C原子。
(3)在金刚石晶体中,C原子所连接的最小环也为六元环,每个C原子连接________个六元环。
(4)金刚石晶胞含有________个碳原子。若碳原子半径为r,金刚石晶胞的边长为a,列式表示碳原子在晶胞中的空间占有率________(不要求计算结果)。
(5)德国和美国科学家首先制出由20个碳原子组成的空心笼状分子C20,该笼状结构是由许多正五边形构成(如右图)。请回答: C20分子共有_______个正五边形,共有______条棱边,C20晶体属于________晶体(填晶体类型)。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com