
����Ŀ����֪���̿���̽�˿����Ҫ�ɷ־�ΪMnO2���������̵��Ʊ�����������������ͻ�ѧʵ�����й㷺Ӧ�á�
�������̵��Ʊ�:
�̷۵���Ҫ�ɷ�ΪNH4Cl��C��MnO2,���̷۽�����ͼ��ʾ������,�ɵõ��������̹��塣

(1)ijͬѧ��Ϊ�Լ�aΪ����ˮ,����Ϊ______(��ܡ����ܡ�)ʵ��ʵ��Ŀ�ġ�
(2)����1��������______,���õ��IJ����������ձ�����������______��
(3)�ڿ����г�����յ�Ŀ����_________��
�������̵����ʼ���:
��.������
(4)ʵ������MnO2��Ũ���ᷴӦ�Ʊ�Cl2������ѡ�õ�װ����______(����ĸ)��
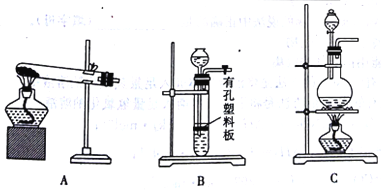
(5)��MnO2����NH3�����м��ȣ��ɵõ��غ�ɫ��Mn2O3��N2,�÷�Ӧ�Ļ�ѧ����ʽΪ_______��
��.��ԭ��
(6)���������������ķ�Ӧ�У��������뻹ԭ�������ʵ���֮��Ϊ______��
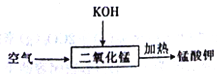
��.����
MnO2��ʵ������ȡO2�Ĵ�����ijͬѧ���ʵ��̽��˫��ˮ�ֽ��ʵ�鷽�����±���ʾ��
ʵ����� | w(H2O2)/% | ��״MnO2/g | �¶�/�� | �������� |
�� | 5 | 0 | 20 | |
�� | 5 | 1.0 | 20 |
(7)��ʵ��Ĵ���������___________��
(8)��ʵ��ٺ͢ڿɵó��Ľ�����______________________��
���𰸡� �� ���� (��ͨ)©�� ��ȥ������е�̼(C),�Եõ�������MnO2 C 6MnO2+2NH3=3Mn2O3+N2+3H2O 1:2 �ռ��������������Ҫ��ʱ��(����ͬʱ�������ռ������������) MnO2����˫��ˮ�ֽ�Ĵ���(������������)
��������(1) �̷۵���Ҫ�ɷ�ΪNH4Cl��C��MnO2,�Լ�aΪ����ˮ��NH4Cl����ˮ��C��MnO2������ˮ�����˷��룬����ʵ��ʵ��Ŀ�ģ�(2)����1�������ǹ���,���õ��IJ����������ձ�����������(��ͨ)©����(3)�ڿ����г�����յ�Ŀ���dz�ȥ������е�̼(C),�Եõ�������MnO2��(4)ʵ������MnO2��Ũ���ᷴӦ�Ʊ�Cl2��װ�ñ����ʺϡ���-Һ���������塱����ѡ�õ�װ����C��(5) MnO2��NH3��Ӧ����Mn2O3��N2��ˮ����Ӧ�Ļ�ѧ����ʽΪ6MnO2+2NH3=3Mn2O3+N2+3H2O��(6)�������̿�֪�����ķ�ӦΪ2MnO2+4KOH+O2![]() 2K2MnO4+2H2O�����ݷ�Ӧ��֪��������O2�뻹ԭ��MnO2�����ʵ���֮��Ϊ1��2��(7)���ݱ������ݿ��ƲⱾʵ��Ĵ����������ռ��������������Ҫ��ʱ��(����ͬʱ�������ռ������������)��(8)��ʵ��ٺ͢ڿɵó��Ľ�����MnO2����˫��ˮ�ֽ�Ĵ�����
2K2MnO4+2H2O�����ݷ�Ӧ��֪��������O2�뻹ԭ��MnO2�����ʵ���֮��Ϊ1��2��(7)���ݱ������ݿ��ƲⱾʵ��Ĵ����������ռ��������������Ҫ��ʱ��(����ͬʱ�������ռ������������)��(8)��ʵ��ٺ͢ڿɵó��Ľ�����MnO2����˫��ˮ�ֽ�Ĵ�����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����X��Y��Z��W��M���ֶ�����Ԫ�أ�����X��Y��Z��Wͬ���ڣ�Z��Mͬ���壻X����M2��������ͬ�ĵ��Ӳ�ṹ�����Ӱ뾶��Z2����W����Y�ĵ��ʾ����۵�ߡ�Ӳ�ȴ���һ����Ҫ�İ뵼����ϡ�������������⣺
��1��MԪ�صļ����ӵĽṹʾ��ͼΪ_______��
��2��Z�����ڱ��е�λ��Ϊ_____����ǽ����Ա�W�ķǽ�����____(�ǿ��������)��
��3��X��Z��W��ԭ�Ӱ뾶�ɴ�С˳��Ϊ_____________(��Ԫ�ط���)��
��4��Y���⻯�ﻯѧʽΪ______�����⻯���л�ѧ������Ϊ________________������Ӽ����������Թ��ۼ����Ǽ��Թ��ۼ�������
��5��W�ĵ�����X������������ˮ���ﷴӦ�����ӷ���ʽΪ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�л�����ҩ���������м��壬��ṹ��ʽ��ͼ�������й�������ȷ����( )

A. ���л���������ˮ�����ӳɷ�Ӧ
B. ���л�����Ũ�����ϼ��ȿɷ�����ȥ��Ӧ
C. 1 mol ���л���������NaOH��Һ��Ӧ�������3 mol NaOH
D. ���л��ᆳ���������ܷ���������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���мס������ָ߾�����������л��ܼ������ȿ����ڣ��Ҳ������κ��ܼ������Ȳ�����������ڣ������������д������ (����)
A. �߾�����ܾ��е��ԣ����߾�����һ��û�е���
B. �߾�����������߷��ӻ��������
C. �߾����һ�������߷��ӻ��������
D. �߾�����һ�������߷��ӻ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�˲ⶨijͭ���Ͻ����ɣ���30.0g�Ͻ�����80.0mL 13.5mol��L1��ŨHNO3�С����Ͻ���ȫ�ܽ���ռ�������6.72L(��״����)�����H+Ũ��Ϊ1mol��L1�����跴Ӧ����Һ�����Ϊ80.0mL���Լ��㣺
(1)����ԭ����������ʵ���___________��
(2)�Ͻ���������������___________��
(3)ȷ��6.72L�����и��ɷֵ����ʵ���___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ���ǣ� ��
A.1 mol�κδ����ﶼ������ͬ�ķ�����
B.1 mol������Լ����6.02��1023����ԭ��
C.1 molˮ�к���8mol����
D.1 molNa������Ϊ23 gmol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����(�� ��)
A. �ڻ�ѧ��Ӧ�з������ʱ仯��ͬʱ����һ�����������仯
B. ��H>0��ʾ���ȷ�Ӧ����H<0��ʾ���ȷ�Ӧ
C. ��H�Ĵ�С���Ȼ�ѧ����ʽ�л�ѧ��������
D. �������ͷŵ����������ڷ�Ӧ�����յ�������ʱ����H<0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ����
A. ![]() �е�����������������֮��Ϊ1:1
�е�����������������֮��Ϊ1:1
B. CO2��BCl3�����и�ԭ������㶼����8���ӽṹ
C. ![]() ��
��![]() ��Ӧ���ɵ������к���
��Ӧ���ɵ������к���![]()
D. ԭ����������������4��Ԫ�ؾ�Ϊ����Ԫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��̬��A��̼����������Ϊ92.3%��C��D��Ϊͬ���칹�壬F�����������Ҵ���ͬ�Ĺ����ţ��й����ʵ�ת����ϵ��ͼ��
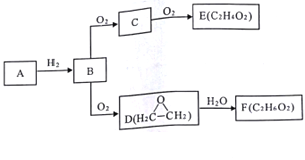
��ش�
��1��д��B�ĵ���ʽ___________________��
��2��C��E�ķ�Ӧ����___________________��
��3��D��F�Ļ�ѧ����ʽ___________________��
��4������˵����ȷ����___________________��
A. ����ȼ�շ�����A��B
B. C��һ�������¿�������������ԭ��Ӧ
C. E��F��Ũ���������¼��ȷ�Ӧ������ֻ��һ��
D. ��D�����ʽ��ͬ����Է�������Ϊ88�����ʿ�����E��ͬϵ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com