
【题目】化合物H具有类似龙涎香、琥珀香的气味,香气淡而持久,被广泛用作香精的稀释剂和定香剂。合成该化合物的某种途径如图所示。
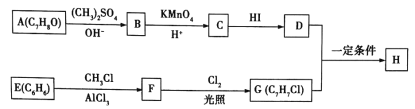
已知以下信息:
①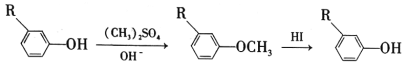 ;
;
②A的苯环上有四种化学环境不同的氢原子,且取代基的位置相邻;
③在D中滴加几滴FeCl3溶液,发生反应显出颜色;
④芳香烃F的相对分子质量介于90~100之间,0.1molF充分燃烧可生成7.2g水;
⑤R1COOH+RCH2C1![]() R1COOCH2R+HCl。
R1COOCH2R+HCl。
回答下列问题:
(1)A的化学名称是___________,由C生成D的反应的化学方程式为_______________。
(2)由F生成G的反应的化学方程式为____________________,反应类型为________________。
(3)H的结构简式为__________________。
(4)苯环上有三个取代基且其中两个与A中所含的官能团相同,同时又能发生银镜反应的C的同分异构体有___________(不考虑立体异构)种,其分子中有5种化学环境不同的氢原子,且氢原子个数之比为1:2:2:2:1的同分异构体的结构简式是_____________(任写一种即可)。
(5)苯酚经下图所示步骤可合成化合物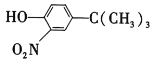 。
。
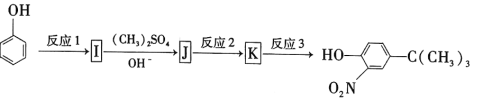
反应1所用的试剂为____________,K的结构简式为___________,反应3所用的试剂为_____________。
【答案】2-甲基苯酚(或邻甲基苯酚) ![]()
![]() 取代反应
取代反应 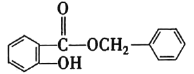 6
6 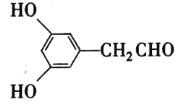 (或
(或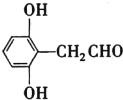 ) (CH3)3CCl和AlCl3
) (CH3)3CCl和AlCl3 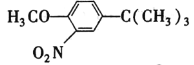 HI
HI
【解析】
根据A的分子式及已知信息②可知A结构简式为![]() ,由已知信息①可知A→B的过程发生取代反应,B是
,由已知信息①可知A→B的过程发生取代反应,B是![]() ,B→C是甲基被氧化为羧基的过程,C为
,B→C是甲基被氧化为羧基的过程,C为![]() ,C→D的过程发生的是取代反应,D是
,C→D的过程发生的是取代反应,D是![]() ;0.1mol F充分燃烧可生成7.2g水,即0.1mol F所含H为
;0.1mol F充分燃烧可生成7.2g水,即0.1mol F所含H为![]() ,结合G的分子式可知F是甲苯,E的分子式为C6H6,则E是苯,F→G的过程中F的甲基上的H被Cl取代,G为
,结合G的分子式可知F是甲苯,E的分子式为C6H6,则E是苯,F→G的过程中F的甲基上的H被Cl取代,G为![]() ;根据已知信息⑤可推出H为
;根据已知信息⑤可推出H为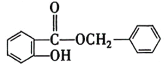 ;据此解答。
;据此解答。
(1)由分析可知, A的结构简式为![]() ,化学名称为2-甲基苯酚(或邻甲基苯酚),C→D的过程发生的是取代反应,化学方程式为
,化学名称为2-甲基苯酚(或邻甲基苯酚),C→D的过程发生的是取代反应,化学方程式为![]() ;
;
(2)由分析可知,F是甲苯,G为![]() ,F→G的过程中F的甲基上的H被Cl取代,化学方程式为
,F→G的过程中F的甲基上的H被Cl取代,化学方程式为![]() ;
;
(3)根据已知信息⑤可推出H为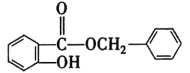 ;
;
(4)苯环上有三个取代基且其中两个与A中所含的官能团相同,同时又能发生银镜反应的C的同分异构体,说明该同分异构体含有两个酚羟基,一个醛基,且为三取代苯,故其除酚羟基外的一个取代基是—CH2CHO,因此符合要求的同分异构体有6种;分子中有5种化学环境不同的氢原子,且氢原子个数之比为1:2:2:2:1的同分异构体的结构简式是 或
或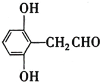 ;
;
(5)在苯环上引入—NO2,发生的是硝化反应,引入—C(CH3)3的反应原理与E→F的反应原理相同,I→J的转化过程是为了保护酚羟基,即苯酚→I的过程引入了—C(CH3)3,故反应1所用的试剂为(CH3)3CCl和AlCl3,硝酸有强氧化性,可氧化酚羟基,故在得到酚羟基之前应先进行硝化反应,故反应2所用的试剂是浓硝酸和浓硫酸,并加热生成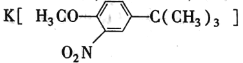 ,反应3所用的试剂是HI。
,反应3所用的试剂是HI。


科目:高中化学 来源: 题型:
【题目】工业生产中有实用价值的反应往往产物较纯净且容易分离,据此判断下列有机反应在工业上没有实用价值的是( )
A.![]() +3H2
+3H2![]()
B.nCH2=CH2![]()
C.CH3CH2CH3+Cl2![]() CH3CH2CH2Cl+HCl
CH3CH2CH2Cl+HCl
D.![]() +NaBr
+NaBr
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据某有机物的结构:
(1)测定实验式:某含碳、氢、氧三种元素的有机物,经燃烧分析实验测定其碳的质量分数是64.86%,氢的质量分数是13.51%,则其实验式是________。
(2)确定分子式:下图是该有机物的质谱图,则其相对分子质量为______,分子式为________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究NO2、SO2 、CO等大气污染气体的处理具有重要意义。
(1)一定条件下,将2molNO与2molO2置于恒容密闭容器中发生如下反应:2NO(g)+O2(g)![]() 2NO2(g),下列各项能说明反应达到平衡状态的是_____________。
2NO2(g),下列各项能说明反应达到平衡状态的是_____________。
A.体系压强保持不变
B.混合气体颜色保持不变
C.NO和O2的物质的量之比保持不变
D.每消耗1 molO2同时生成2 molNO
(2)CO可用于合成甲醇,一定温度下,向体积为2L的密闭容器中加入CO和H2,发生反应CO(g)+2H2(g)![]() CH3OH(g),达平衡后测得各组分浓度:
CH3OH(g),达平衡后测得各组分浓度:
物质 | CO | H2 | CH3OH |
浓度(mol/L) | 0.9 | 1.0 | 0.6 |
回答下列问题:
①混合气体的平均相对分子质量=_________________。
②平衡常数K=__________________。
③若将容器体积压缩为1L,不经计算,预测新平衡中c(H2)的取值范围是__________。
④若保持体积不变,再充入0.6molCO和0.4molCH3OH,此时v正______v逆(填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的分子式为C4HmO,下列说法错误的是( )
A.1 mol该有机物完全燃烧时,最多消耗6 mol O2
B.当m=6时,该有机物遇到FeCl3溶液发生显色反应
C.当m=8时,该有机物不一定能被新制氢氧化铜悬浊液氧化
D.当m=10时,该有机物不一定是丁醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】稀土元素是宝贵的战略资源,我国的蕴藏量居世界首位,但近年来对其进行了掠夺性开采。二氧化铈(CeO2)是一种重要的稀土化合物。以氟碳铈矿(主要含CeFCO3)为原料制备CeO2的一种工艺流程如图:
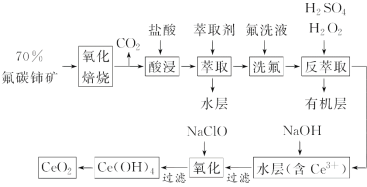
已知:①Ce4+能与F-结合成[CeFx](4-x)+,也能与SO42-结合成[CeSO4]2+;
②在硫酸体系中Ce4+能被萃取剂[(HA)2]萃取,而Ce3+不能。
回答下列问题:
(1)“氧化焙烧”中“氧化”的目的是__。
(2)“酸浸”中会产生大量黄绿色气体,写出CeO2与盐酸反应的离子方程式:__。为避免产生上述污染,请提出一种解决方案:__。
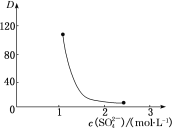
(3)“萃取”时存在反应:Ce4++n(HA)2![]() Ce·(H2n-4A2n)+4H+。如图中D是分配比,表示Ce(Ⅳ)分别在有机层中与水层中存在形式的物质的量浓度之比(D=
Ce·(H2n-4A2n)+4H+。如图中D是分配比,表示Ce(Ⅳ)分别在有机层中与水层中存在形式的物质的量浓度之比(D=![]() )。保持其他条件不变,D随起始料液中c(SO42-)变化的原因:__(用平衡移动原理解释)。
)。保持其他条件不变,D随起始料液中c(SO42-)变化的原因:__(用平衡移动原理解释)。
(4)若缺少“洗氟”,则所得产品的质量将__(填“偏大”“偏小”或“不变”)。
(5)“反萃取”中,H2O2作__(填“催化剂”“氧化剂”或“还原剂”)。
(6)“氧化”步骤的化学方程式为__。
(7)取上述流程中得到的CeO2产品0.4000g,加硫酸溶解后,用0.1000mol·L-1FeSO4标准溶液滴定至终点时(铈被还原为Ce3+,其他杂质均不反应),消耗20.00mL标准溶液。该产品中CeO2的质量分数为__。滴定过程中可能造成实验结果偏低的是__(填字母)。
A.使用久置的FeSO4标准溶液
B.滴定终点时仰视读数
C.锥形瓶中溶液变色后立刻停止滴定,进行读数
D.滴定管尖嘴内滴定前无气泡,滴定终点发现气泡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A是一种气态烃,相对分子质量是28,通常用作果实催熟剂,其年产量可用来衡量一个国家石油化工发展水平。D是厨房中某种调味品的成分之一, 各物质间的转化关系如下图(反应条件已省略)。回答下列问题:
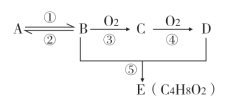
(1)B物质的名称________________.
(2)D分子中含有的官能团名称________________________.
(3)C物质的结构简式________________________
(4)反应⑤发生的条件________________________
(5)反应④的反应类型________________________
(6)反应①的化学方程式:________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物甲和A互为同分异构体,经测定它们的相对分子质量小于100;将1mol甲在O2中充分燃烧得到等物质的量的CO2和H2O (g) ,同时消耗112L O2(标准状况);在酸性条件下将1mol甲完全水解可以生成1mol乙和1mol丙;而且在一定条件下,丙可以被连续氧化成为乙。
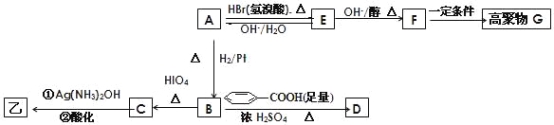
经红外光谱测定,在甲和A的结构中都存在C=O双键和C-O单键,B在HIO4存在并加热时只生成一种产物C,下列为各相关反应的信息和转化关系:
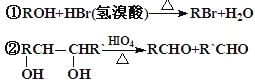
⑴ 请确定并写出甲的分子式_______;与甲属同类物质的同分异构体共有____种(包含甲)。
⑵ E→F 的反应类型为_________反应;
⑶ A的结构简式为_________;G 的结构简式为_________;
⑷ B→D的反应化学方程式为_______________________________;
⑸ 写出C在条件①下进行反应的化学方程式___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源开发、环境保护、资源利用等是当今社会的热门话题。请根据所学化学知识回答下列问题:
(1)汽车上安装催化转化器,可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)进行相互反应,生成无毒物质,减少汽车尾气污染。
已知:N2(g) + O2(g)=2NO(g) △H=+180.5 kJ · mol-1;
2C(s)+ O2(g)=2CO(g) △H=-221.0 kJ · mol-1;
C(s)+ O2(g)=CO2(g) △H=-393.5 kJ · mol-1;
则尾气转化反应2NO(g) +2CO(g)=N2(g)+2CO2(g)的△H=________________。
(2)汽车尾气分析仪对CO的含量分析是以燃料电池为工作原理,其装置如下图所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质中自由移动。

下列说法中正确的是_____________(填字母序号)。
A.负极的电极反应式为:CO + O2-―2e-=CO2
B.工作时电子由电极a通过传感器流向电极b
C.工作时电极b作正极,O2-由电极a通过固体介质向电极b迁移
D.传感器中通过的电流越大,尾气中CO的含量越高
(3)某硝酸厂利用甲醇处理废水。在一定条件下,向废水中加入CH3OH,将HNO3还原成N2。若该反应消耗32 g CH3OH转移6 mol电子,则参加反应的还原剂和氧化剂的物质的量之比为______________。
(4)煤的间接液化是先转化为CO和H2,再在催化剂作用下合成甲醇。若在一定温度下,向1 L密闭容器中加入CO和H2,发生反应CO(g)+2H2(g)![]() CH3OH(g),经10 min反应达到平衡时测得各组分的浓度如下:
CH3OH(g),经10 min反应达到平衡时测得各组分的浓度如下:
物 质 | CO | H2 | CH3OH |
浓度/(mol·L-1) | 1.2 | 1.0 | 0.6 |
①该反应的平衡常数表达式为:K=_____________________。
②该时间内反应速率υ(H2)=_________________。
③平衡时CO的转化率为_________________(保留1位小数)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com