
����Ŀ����ҵ�ϸߴ����ͨ�����з�Ӧ��ȡ��SiCl4(g)��2H2(g)![]() Si(s)��4HCl(g)���йػ�ѧ���ļ������������ʾ��
Si(s)��4HCl(g)���йػ�ѧ���ļ������������ʾ��
��ѧ�� | Si��Cl | H��H | H��Cl | Si��Si | Si��C |
����kJ/mol | 360 | 436 | 431 | 176 | 347 |
����˵����ȷ���ǣ� ��
A.��Ӧ�е������仯�����ʵ�״̬��
B.��������Ҫ���Ȳ��ܽ��еķ�Ӧ�������ȷ�Ӧ
C.������SiC���ȶ�
D.�÷�Ӧ��ÿ����1molSi(s)���յ�����Ϊ236kJ
���𰸡�D
��������
A����ѧ��Ӧ�е������仯�����ʵ�״̬�йأ���������̬>Һ̬>��̬��A����
B�����ȷ�Ӧ����ȷ�Ӧ�뷴Ӧ�����أ����������������Ȼ�麟����·�Ӧ���÷�ӦΪ���ȷ�Ӧ��B����
C��������SiC����ԭ�Ӿ��壬ͬ���壬���ϵ��£�ԭ�Ӱ뾶����ԭ�Ӱ뾶��Si>C�����̼֮��ļ���С�ڹ��֮��ļ���������Խ�̣�Խ�ȶ�������SiC�Ⱦ������ȶ���C����
D�� H=��Ӧ����ܼ���-��������ܼ��ܣ�����SiCl4(g)��2H2(g)![]() Si(s)��4HCl(g)��H=��360��4+436��2-176��2-431��4��kJ/mol=+236kJ/mol������ÿ����1molSi(s)���յ�����Ϊ236kJ��D��ȷ��
Si(s)��4HCl(g)��H=��360��4+436��2-176��2-431��4��kJ/mol=+236kJ/mol������ÿ����1molSi(s)���յ�����Ϊ236kJ��D��ȷ��
�ʴ�Ϊ��D��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����¶�298KʱpHΪ9��KOH��Һ��pHΪ9��![]() ��Һ����ˮ�������
��Һ����ˮ�������![]() �ıȽ��У���ȷ����
�ıȽ��У���ȷ����![]()
A.�������B.ǰ���Ǻ��ߵ�![]() ��
��
C.������ǰ�ߵ�![]() ��D.���Ƚ�
��D.���Ƚ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Na��Cu��O��Si��S��Cl�dz���������Ԫ�ء�
(1)Naλ��Ԫ�����ڱ���____���ڵ�____�壻S�Ļ�̬ԭ�Ӻ�����________��δ�ɶԵ��ӣ�Si�Ļ�̬ԭ�Ӻ�������Ų�ʽΪ__________��
(2)����>������<����գ�
��һ������ | ���Ӱ뾶 | �۵� | ���� |
Si____S | O2-____Na+ | NaCl____Si | H2SO4____HClO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ԫ��X��Y��Z��W��ԭ�������������ӡ�A��B��C��D��������ЩԪ����ɵĶ�Ԫ���������Y�Ĺ��嵥�ʣ�������0.05mol/L����Һ��pHΪ1��A����ɫ���壬����Ҫ�Ĵ�����Ⱦ��֮һ���������ʵ�ת����ϵ��ͼ��ʾ������˵��������ǣ� ��
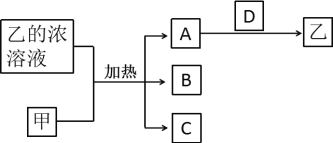
A.ԭ�Ӱ뾶��X<Z<W
B.D�д��ڼ��Լ��ͷǼ��Լ�
C.��ۺ���������ԣ�W>Y
D.������YZW�м���Ϊ120��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ�鷽���У��ܴﵽ��Ӧʵ��Ŀ�ĵ���
A.���������ڷ���I2��NH4I����
B.���������ڱȽ�CuSO4��MnO2�Ĵ�����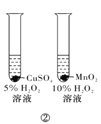
C.���������ڲⶨ�к���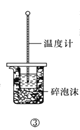
D.���������ڱȽϴ�������������ǿ��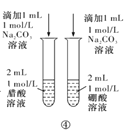
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������vtͼ������������ı�Կ��淴ӦA(g)��3B(g) ![]() 2C(g) ��H<0��Ӱ�졣�÷�Ӧ��������ʱ��Ĺ�ϵ��ͼ��ʾ��
2C(g) ��H<0��Ӱ�졣�÷�Ӧ��������ʱ��Ĺ�ϵ��ͼ��ʾ��
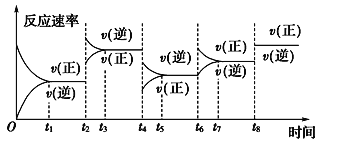
�ɼ���t1��t3��t5��t7ʱ��Ӧ���ﵽƽ�⣬���t2��t4��t6��t8ʱ��ֻ�ı���һ����Ӧ�����������ж�t2��t4��t6��t8ʱ�ı��������ж���ȷ����
A. ʹ���˴���������ѹǿ����С��Ӧ��Ũ�ȡ������¶�
B. �����¶ȡ���Сѹǿ����С��Ӧ��Ũ�ȡ�ʹ���˴���
C. ����Ӧ��Ũ�ȡ�ʹ���˴�������Сѹǿ�������¶�
D. �����¶ȡ���Сѹǿ������Ӧ��Ũ�ȡ�ʹ���˴���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ������������Ӧʵ��������ǣ� ��
ʵ������ | ���ӷ���ʽ | |
A | ��������þ����Һ�еμ��Ȼ����Һ�������ܽ� |
|
B | ���ˮ�еμӱ����Ȼ�����Һ�õ����ɫҺ�� |
|
C | ��������ʹ���Ը��������Һ��ɫ |
|
D | ������������ϡ���� |
|
A. AB. BC. CD. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������A��B��C��D��E���־�������ˮ�Ĺ������ʣ����������ṩ�ļ����������![]() ÿ������ֻ����һ��
ÿ������ֻ����һ��![]() ��
��
������ |
|
������ |
|
�ֱַ��������ʵ�飺
![]() ��D��E����Һ��ϼ��ȣ������д̼�����ζ������
��D��E����Һ��ϼ��ȣ������д̼�����ζ������
![]() ��B��E����Һ��ϣ�������ɫ��������ó����м���������ϡ���ᣬ���������ܽ�
��B��E����Һ��ϣ�������ɫ��������ó����м���������ϡ���ᣬ���������ܽ�
![]() �ڳ�������pH��ֽ�ⶨ��ҺA��
�ڳ�������pH��ֽ�ⶨ��ҺA��![]()
����˵������ȷ����![]()
A.����E�Ļ�ѧʽΪ![]() B.����D��һ������
B.����D��һ������![]()
C.����ȷ������A�����D.����C�Ļ�ѧʽ��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�������£���ӦN2+3H22NH3����2L�ܱ������н��У�5min�ڰ�������������1.7g����Ӧ����Ϊ�� ��
A.v(H2)=0.03mol/��L��min��
B.v(N2)=0.02mol/(L��min)
C.v(NH3)=0.17mol/(L��min )
D.v(NH3)=0.01mol/(L��min)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com