
【题目】(1)环境污染已成人类社会面临的重大威胁。下列名词与环境污染无关的是________(填:序号)。
①赤潮 ②温室效应 ③酸雨 ④光化学烟雾 ⑤水力发电 ⑥臭氧层空洞 ⑦潮汐 ⑧农药化肥的不当使用 ⑨地方性大脖子病 ⑩工业“三废”和生活污水的任意排放
(2)火箭推进器中装有强还原剂肼(N2H4)和强氧化剂(NO2),已知热化学方程式:
N2(g)+2O2(g)==2NO2(g) △H=+67.7kJ/mol; N2H4(g)+O2(g)==N2(g)+2H2O(g) △H=-534kJ/mol。请写出气态肼与NO2气体反应生成氮气和水蒸气的热化学方程式___________________________。该反应应用于火箭推进,除能释放大量热和快速产生大量气体外,还有一个很突出的优点是:________________________________________________。
(3)乙烯(C2H4)结构简式为CH2=CH2,且知:C-H键、C=C键、O=O键、C=O键、O-H键的键能分别是:413kJ/mol、615kJ/mol、496kJ/mol、745kJ/mol、463kJ/mol,则表达乙烯(C2H4)气体“燃烧热”的热化学方程式:C2H4(g) +3O2(g) =2CO2(g) +2H2O(l)中,△H=-______kJ/mol。
如果有2.4NA个电子发生转移,所放出的热量值是____________kJ。
(4)在微生物作用的条件下,NH4+经过两步反应被氧化成N3-。两步反应的能量变化如图:

①第一步是______反应(选填“放热”或“吸热”),判断依据是____________________。
【答案】⑤⑦⑨ N2H4(g)+2NO2(g)= 3N2(g)+4 H2O(g) △H =-1135.7 kJ/mol; 产物清洁无污染 1077 215.4 放热 因为△H =-273kJ/mol<0,反应物的总能量大于生成物的总能量,所以反应为放热反应
【解析】
(1) ①赤潮是水中的氮、磷元素浓度过大造成的水污染,会导致藻类疯长,引起水中缺氧,水生生物大量死亡,与环境污染有关;②温室效应是因为CO2等温室气体造成的全球气候变暖,与环境污染有关;③酸雨是大量排放SO2等酸性气体造成的大气污染,与环境污染有关;④光化学污染是氮的氧化物和有机烃类在光作用下的一系列复杂变化,与环境污染有关;⑤水力发电是将水能转化为电能,与环境污染无关;⑥臭氧空洞是氟里昂等排放到空气中形成的,与环境污染有关;⑦潮汐是海水在天体引力作用下产生的海面周期性涨落现象,与环境污染无关;⑧农药化肥的不当使用会造成环境污染;⑨地方性甲状腺肿是因为缺碘造成的甲状腺肿大,与环境污染无关; ⑩工业“三废”指废水废气和废物,生活污水的任意排放会造成环境污染;与环境污染无关,故 ⑤⑦⑨与环境污染无关。答案⑤⑦⑨。
(2) ①N2(g)+2O2(g)==2NO2(g)△H=+67.7kJ/mol②N2H4(g)+O2(g)==N2(g)+2H2O(g) △H=-534kJ/mol根据盖斯定律计算②![]() -①得到N2H4(g)+2NO2(g)= 3N2(g)+4H2O(g) △H =-1135.7 kJ/mol 。反应应用于火箭推进,除能释放大量热和快速产生大量气体外,还有一个很突出的优点是产物为氮气和水,清洁无污染,。因此,本题正确答案是: N2H4(g)+2NO2(g)= 3N2(g)+4 H2O(g) △H =-1135.7 kJ/mol;产物为氮气和水,清洁无污染。
-①得到N2H4(g)+2NO2(g)= 3N2(g)+4H2O(g) △H =-1135.7 kJ/mol 。反应应用于火箭推进,除能释放大量热和快速产生大量气体外,还有一个很突出的优点是产物为氮气和水,清洁无污染,。因此,本题正确答案是: N2H4(g)+2NO2(g)= 3N2(g)+4 H2O(g) △H =-1135.7 kJ/mol;产物为氮气和水,清洁无污染。
(3)乙烯(C2H4)结构简式为CH2=CH2,且知:C-H键、C=C键、O=O键、C=O键、O-H键的键能分别是:413kJ/mol、615kJ/mol、496kJ/mol、745kJ/mol、463kJ/mol,则表达乙烯(C2H4)气体“燃烧热”的热化学方程式:C2H4(g) +3O2(g) =2CO2(g) +2H2O(l)中, 413kJ/mol4+615kJ/mol+496kJ/mo![]() -745kJ/mol
-745kJ/mol![]() 4-463kJ/mol
4-463kJ/mol![]() 4=-1077kJ/mol。
4=-1077kJ/mol。
由C2H4(g) +3O2(g) =2CO2(g) +2H2O(l)知转移12NA电子时会放出1077kJ的热量,如果有2.4NA个电子发生转移,放出的热量为1077kJ![]() 2.4/12=2154 kJ。答案:1077、215.4
2.4/12=2154 kJ。答案:1077、215.4
(4) ① 因为△H =-273KJ/mol<0,反应物的总能量大于生成物的总能量,则反应为放热反应,因此,本题答案是:放热、因为△H =-273KJ/mol<0,反应物的总能量大于生成物的总能量,所以反应为放热反应。


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
【题目】下表中相关物质的信息都正确的一项是
选项 | 化学式 | 电子式或含有的化学键类型 | 物质的性质 | 与性质相对应的用途 |
A | NaClO | 离子键、共价键 | 强氧化性 | 消毒液 |
B | H2O2 |
| 不稳定,易分解 | 医用消毒剂 |
C | NH3 | 共价键 | 水溶液呈弱碱性 | 工业制硝酸 |
D | NaHCO3 | 离子键 | 受热易分解 | 泡沫灭火器 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用无机矿物资源生产部分材料的流程示意图如下。下列说法不正确的是( )

A. 在铝土矿制备较高纯度Al的过程中常用到NaOH溶液、CO2气体、冰晶石
B. 石灰石、纯碱、石英、玻璃都属于盐,都能与盐酸反应
C. 在制粗硅时,被氧化的物质与被还原的物质的物质的量之比为2∶1
D. 黄铜矿(CuFeS2)与O2反应产生的Cu2S、FeO均是还原产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列各溶液中,离子一定能大量共存的是( )
A.碱性溶液中:K+、HCO3-、Cl-、SO42-
B.酸性溶液中:Na+、Fe3+、NO3-、SO42-
C.含有0.1mol/LCa2+的溶液中:Na+、K+、CO32-、Cl-
D.使酚酞试液变红的溶液:Na+、Cl-、SO42-、Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解Na2SO4溶液产生H2SO4和烧碱的装置如下图所示,其中阴极和阳极均为惰性电极。测得同温同压下,气体甲与气体乙的体积比约为1∶2。以下说法正确的是(说明:阳离子交换膜只允许阳离子通过,阴离子交换膜只允许阴离子通过)
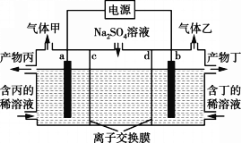
A. 产物丁为H2SO4
B. a电极反应式:2H2O+2e-=H2↑+2OH-
C. 离子交换膜d为阳离子交换膜
D. 每转移0.2 mol电子,产生1.12 L气体甲
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁被誉为“第一金属”,铁及其化合物在生活中有广泛应用。
(1)基态Fe3+的电子排布式为_________________。
(2)实验室用KSCN溶液、苯酚(![]() )检验Fe3+。N、O、S的第一电离能由大到小的顺序为______(用元素符号表示),苯酚中碳原子的杂化轨道类型为_______。
)检验Fe3+。N、O、S的第一电离能由大到小的顺序为______(用元素符号表示),苯酚中碳原子的杂化轨道类型为_______。
(3)FeCl3的熔点为306℃,沸点为315℃。FeCl3的晶体类型是________。FeSO4常作补铁剂,SO42-的立体构型是__________。
(4)羰基铁[Fe(CO)5]可用作催化剂、汽油抗暴剂等。1 mol Fe(CO)5分子中含________molσ键,与CO互为等电子体的离子是__________(填化学式,写一种)。
(5)氮化铁晶体的晶体结构示意图如图1所示。该晶体中铁、氮的微粒个数之比为_____。

(6)氧化亚铁晶体的晶胞如图2所示。已知:氧化亚铁晶体的密度为ρg·cm-3,NA代表阿伏加德罗常数的值。在该晶胞中,与Fe3+紧邻且等距离的Fe2+数目为_____;Fe2+与O2-的最短核间距为___________pm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D是常见的有机物,A是一种气态烃,标准状况下的密度1.25g/L,其产量是衡量一个国家石油化工发展水平的标志之一;C分子式为C2H4O2;B和C在浓硫酸和加热条件下发生反应,生成有果香味儿的油状液体D;A、B、C、D一定条件下的转化关系如图(条件省略):

(1)C中所含官能团的名称______________;
(2)丙烯酸![]()
![]() 可能发生的化学反应有:__________________;
可能发生的化学反应有:__________________;
①加成反应 ②取代反应 ③加聚反应 ④中和反应 ⑤氧化反应
(3)写出聚丙烯酸的结构简式__________________________;
(4)写出下列反应的化学方程式:
①A→B:___________________________________________________;
②丙烯酸+B→丙烯酸乙酯:_______________________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色透明的溶液中,能大量共存的离子组是( )
A. Ag+、K+、NO3﹣、Cl﹣ B. Ca2+、Fe3+、Cl﹣、NO3﹣
C. Mg2+、Na+、Cl﹣、SO42﹣ D. H+、NH4+、Na+、CH3COO﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 增大压强或升高温度,一定能使化学反应速率加快
B. 已知Ni(CO)4(g)=Ni(s)+4CO(g) ΔH=Q kJ/mol,则Ni(s)+4CO(g)=Ni(CO)4(g) ΔH=-Q kJ/mol
C. 500℃、30 MPa下,0.5 mol N2(g)和1.5 mol H2(g)反应生成NH3(g)放热Q kJ,其热化学方程式为N2(g)+3H2(g) ![]() 2NH3(g) ΔH=-2Q kJ/mol
2NH3(g) ΔH=-2Q kJ/mol
D. 已知两个平衡体系:2NiO(s) ![]() 2Ni(s)+O2 (g),2CO(g)+O2(g)
2Ni(s)+O2 (g),2CO(g)+O2(g) ![]() 2CO2(g)的平衡常数分别为K1和K2,可推知平衡NiO(s)+CO(g)
2CO2(g)的平衡常数分别为K1和K2,可推知平衡NiO(s)+CO(g) ![]() Ni(s)+CO2(g)的平衡常数为
Ni(s)+CO2(g)的平衡常数为![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com