
【题目】已知:AG=lgc(H+)/c(OH-),室温下用0.01mol·L1 NH3·H2O溶液滴定20.00mL 0.01mol·L1某一元酸HA,可得下图所示的结果,下列说法中错误的是

A. 该滴定实验最好选用甲基橙作指示剂
B. 整个过程中,C点时水的电离程度最大
C. 若x3=30,则有:3c(OH)=c(NH4+)+3c(H+)-2c(NH3·H2O)
D. A→C的过程中,可存在:c(A)>c(H+)>c(NH)>c(OH)
【答案】B
【解析】
A、由A点可知0.01mol·L1HA溶液中c(H+)=0.01mol·L1,所以HA为强酸,因为氨水是弱碱,所以滴定时应该选用甲基橙作指示剂,故A说法正确;
B、整个滴定过程中,当酸碱恰好反应生成盐时,水的电离程度最大,由于生成的盐是强酸弱碱盐,此时溶液显酸性,而C点为中性,故B说法错误;
C、若x3=30,根据电荷守恒有:c(OH)+c(A)=c(NH4+)+c(H+),根据物料守恒有3c(A)=2[c(NH)+c(NH3·H2O)],二者联合解得:3c(OH)=c(NH4+)+3c(H+)-2c(NH3·H2O),故C说法正确;
D、A→C的过程中,若加入的氨水的量很少时,溶液中H+和A较多,此时可存在:c(A)>c(H+)>c(NH4+)>c(OH),故D说法正确。


 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源: 题型:
【题目】乙酸乙酯是无色透明有刺激性气味的液体,制备的实验 装置如图所示。下列说法不正确的是

A. 先在试管a中加入乙醇,然后边振荡试管边缓慢加入浓硫酸和乙酸
B. 浓硫酸的作用主要是催化和吸水
C. b中的饱和Na2CO3溶液可用浓NaOH溶液代替
D. 实验原理为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中含有较大量的Cl﹣、![]() 、OH﹣等3种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次检验出来,下列实验操作顺序正确的是( )
、OH﹣等3种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次检验出来,下列实验操作顺序正确的是( )
①滴加Mg(NO3)2溶液;②过滤;③滴加AgNO3溶液;④滴加Ba(NO3)2溶液
A.①②④②③B.④②①②③C.①②③②④D.④②③②①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:

![]() 该浓盐酸的物质的量浓度为 ______
该浓盐酸的物质的量浓度为 ______ ![]() .
.
![]() 取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是 ______ .
取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是 ______ .
A.溶液中HCl的物质的量![]() 溶液的浓度
溶液的浓度
C.溶液中![]() 的数目
的数目![]() 溶液的密度
溶液的密度
![]() 某学生欲用上述浓盐酸和蒸馏水配制450mL物质的量浓度为
某学生欲用上述浓盐酸和蒸馏水配制450mL物质的量浓度为![]() 稀盐酸.
稀盐酸.
![]() 该学生需要量取 ______ mL上述浓盐酸进行配制.
该学生需要量取 ______ mL上述浓盐酸进行配制.
![]() 配制时,其正确的操作顺序是
配制时,其正确的操作顺序是![]() 用字母表示,每个字母只能用一次
用字母表示,每个字母只能用一次![]() ______ ;
______ ;
A.用30mL水洗涤烧杯![]() 次,洗涤液均注入容量瓶,振荡
次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需浓盐酸的体积,慢慢沿杯壁注入盛有少量水![]() 约
约![]() 的烧杯中,用玻璃棒慢慢搅动,使其混合均匀
的烧杯中,用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入500mL的容量瓶中
D.将容量瓶盖紧,颠倒摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线![]() 处
处
![]() 在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?
在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?![]() 填“偏高”或“偏低”或“无影响”
填“偏高”或“偏低”或“无影响”![]() .
.
I、用量筒量取浓盐酸时俯视观察凹液面 ______
II、用量筒量取浓盐酸后,洗涤量筒![]() 次,洗涤液也转移到容量瓶 ______
次,洗涤液也转移到容量瓶 ______
III、溶液注入容量瓶前没有恢复到室温就进行定容 ______
![]() 若在标准状况下,将VLHCl气体溶于1L水中,所得溶液密度为d
若在标准状况下,将VLHCl气体溶于1L水中,所得溶液密度为d![]() ,则此溶液的物质的量浓度为 ______
,则此溶液的物质的量浓度为 ______ ![]() 填字母
填字母![]()
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家预言,被称为“黑金”的“新材料之王”石墨烯将“彻底改变21世纪”。中国华为研发人员利用锂离子能在石墨烯表面和电极之间快速大量穿梭运动的特性,已在世界上率先开发出石墨烯电池,电池反应式为LixC6+Li1-xCoO2![]() C6+LiCoO2,其工作原理如图。下列关于该电池的说法正确的是
C6+LiCoO2,其工作原理如图。下列关于该电池的说法正确的是

A. 有设计师建议该电池采用隔膜效果更好,可选用质子交换膜
B. 放电时,LiCoO2极发生的电极反应为:LiCoO2-xe=Li1-xCoO2+xLi+
C. 石墨烯电池通过提高储锂容量进而提高能量密度,废旧的该电池进行“放电处理”让Li+嵌入LiCoO2中而有利于回收
D. 石墨烯电池充电时LiCoO2极与电源负极相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下,某反应达平衡,平衡常数K=![]() 。恒容时,温度升高,H2浓度减小。下列说法正确的是
。恒容时,温度升高,H2浓度减小。下列说法正确的是
A、该反应的焓变为正值
B、恒温恒容下,增大压强,H2浓度一定减小
C、升高温度,逆反应速率减小
D、该反应化学方程式为CO+H2O=CO2+H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】G是药物合成中的一种重要中间体,下面是G的一种合成路线:

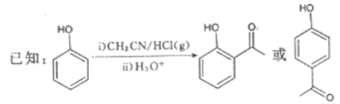
回答下列问题:
(1)B的结构简式为__________,其中所含官能团的名称为__________;B生成C的反应类型为__________。
(2)D的名称是__________。
(3)由C和E合成F的化学方程式为________________________________________。
(4)D的同分异构体中,能发生银镜反应且分子结构中含苯环的还有__________种,其中核磁共振氢谱上有6组峰,峰面积之比为1∶1∶1∶1∶1∶1的同分异构体的结构简式为______________________ (一种即可)。
(5)参照上述合成路线,以CH3CH2Cl为原料(其他试剂任选),设计制备巴豆醛(CH3CH=CH
CHO)的合成路线。_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验实验室配制500mL 0.1molL-1的碳酸钠溶液,请回答下列问题.
(1)应用托盘天平称取Na2CO310H2O晶体__________g.
(2)配置碳酸钠溶液时,需要的主要玻璃仪器除烧杯和胶头滴管以外还需要_________、____________.
(3)配置过程中,若遇到以下操作可能造成实验结果偏大,偏小还是不影响?
①容量瓶中原来有少量蒸馏水_____
②定容时,俯视液面_____
③有少量氢氧化钠溶液残留在烧杯中_____
④盖好瓶塞反复摇匀,发现液面低于标线,再加蒸馏水使液面达到刻度处_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸钡是一种比碳酸钡更难溶的物质。常温下-lgc(Ba2+)随-lgc(CO32-)或-lgc(SO42-)的变化趋势如图,下列说法正确的是

A. 趋势线A表示硫酸钡
B. 常温下,Ksp(BaCO3)=1×10-11
C. 将碳酸钡和硫酸钡固体置于水中,此时溶液中的![]() =10
=10
D. 在硫酸钡悬浊液中,若要使0.1mol的硫酸钡完全转化成碳酸钡,则需要加入碳酸钠的物质的量至少为0.1mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com