
����Ŀ��ij��ѧ��ȤС����ʵ������ͭ��Ũ����Ϊԭ�ϣ��������ַ�����ȡ�������Ʊ��������£�
����һ����ͭм����Ũ�����м���
��1��д���÷�Ӧ�Ļ�ѧ����ʽ______________��
��2��Ũ�����Լ�ƿ�����ı�ǩӦ����______________������ĸѡ���
��3��ͨ��������Ӧ����һϵ�в����������յõ���������25.0g����ԭ��H2SO4�����ʵ���Ϊ____________mol��
����������ͭм����ϡ�����У����Ȳ����Ϲ������,�÷�Ӧ�Ļ�ѧ����ʽΪ��2Cu+ H2SO4+O2![]() 2 CuSO4+2H2O
2 CuSO4+2H2O
��4��д���÷�Ӧ�����ӷ���ʽ��____________________________��
��5��������Ӧ���������ͻ�ԭ�������ʵ���֮��Ϊ___________��
��6����ַ�Ӧ���Ƶõ�����ͭ��Һ��������Ũ����___________�����ˣ����ɵõ��������塣
��7���Ա����ַ���������������ڷ���һ���������Ե��ŵ㣺
����ȡ�������ĵ������ĵ���������٣�
��__________________________________________________
���𰸡�Cu+2H2SO4(Ũ)![]() CuSO4+ SO2��+2H2O D 0.1 2Cu+4H++ O2
CuSO4+ SO2��+2H2O D 0.1 2Cu+4H++ O2![]() Cu2++2H2O 1��2 ��ȴ�ᾧ ��������Ⱦ����SO2
Cu2++2H2O 1��2 ��ȴ�ᾧ ��������Ⱦ����SO2
��������
����Ũ���������������д��ط�Ӧ����ʽ�����ݷ�Ӧ����ʽ�����ʵ����������ȵĹ�ϵ������ؼ��㣻�������ʵķ������ᴿ�ķ���������𣻸��ݷ�Ӧԭ�����Ƿ���Ⱦ�����Ͷ�ԭ��������ȷ���������
��1��Ũ�������ǿ�����ԣ����������¿�����ͭ��Ӧ��������ͭ�����������ˮ����Ӧ����ʽΪ��Cu+2H2SO4(Ũ)![]() CuSO4+ SO2��+2H2O���ʴ�Ϊ��Cu+2H2SO4(Ũ)
CuSO4+ SO2��+2H2O���ʴ�Ϊ��Cu+2H2SO4(Ũ)![]() CuSO4+ SO2��+2H2O��
CuSO4+ SO2��+2H2O��
��2��Ũ������и�ʴ�ԣ������Լ�ƿ�����ı�ǩӦ����D���ʴ�Ϊ��D��
��3�����ݷ�Ӧ����ʽ֪������ԭ��H2SO4�����ʵ����������ɶ�����������ʵ����������ɵ�����ͭ�����ʵ�����n(H2SO4)=n(SO2)=n(CuSO4)=n(CuSO4![]() H2O)=
H2O)=![]() ���ʴ�Ϊ��0.1��
���ʴ�Ϊ��0.1��
��4��ϡ������ͭ����Ӧ��ͨ������ʱ��ͭ������������������ͭ��ˮ�������ӷ���ʽΪ��2Cu+4H++ O2![]() Cu2++2H2O���ʴ�Ϊ��2Cu+4H++ O2
Cu2++2H2O���ʴ�Ϊ��2Cu+4H++ O2![]() Cu2++2H2O��
Cu2++2H2O��
��5��������Ӧ�У���������������ͭ����ԭ�������ʵ���֮��Ϊ1:2���ʴ�Ϊ��1:2��
��6������ͭ��Һ��������Ũ������ȴ�ᾧ�����ˣ����ɵõ��������壬�ʴ�Ϊ����ȴ�ᾧ��
��7��SO2���ڴ�����Ⱦ����ݷ�Ӧ�IJ�������ã��Ա����ַ���������������ڷ���һ�����Ե��ŵ��Dz�������Ⱦ����SO2���ʴ�Ϊ����������Ⱦ����SO2��


 ȫ�ܲ��һ���þ�ϵ�д�
ȫ�ܲ��һ���þ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪Ksp��AgCl��=1.56��10��10��Ksp��AgBr��=7.7��10��13 ��Ksp��Ag2CrO4��=9��10��11��ij��Һ�к���Cl����Br����CrO42����Ũ�Ⱦ�Ϊ0.010mol/L�������Һ����μ���0.010mol/L��AgNO3��Һʱ�����������Ӳ����������Ⱥ�˳��Ϊ( )
A. Cl����Br����CrO42��B. Br����Cl����CrO42��
C. CrO42����Br����Cl��D. Br����CrO42����Cl��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ��ʵ���ҽ����������������ת����ʵ��:

ʵ��I:��Fe3+ת��ΪFe2+
(1)Fe3+��Cu�۷�����Ӧ�����ӷ���ʽΪ��_________________��
(2)̽����ɫ����������ԭ������дʵ�鷽����
ʵ�鷽�� | ���� | ���� |
����1��ȡ4mL____mol/LCuSO4��Һ�����еμ�3��0.1mol/LKSCN��Һ | ������ɫ���� | CuSO4��KSCN��Ӧ�����˰�ɫ���� |
����2��ȡ______________�������еμ�3��0.1mol/LKSCN��Һ | ���������� |
�������ϣ���.SCN-�Ļ�ѧ������I-���ƣ���.2Cu2++4I-=2CuI��+I2
��Cu2+��SCN-��Ӧ�����ӷ���ʽΪ________________��
ʵ���Fe2+ת��ΪFe3+
ʵ�鷽�� | ���� |
��3mL0.1mol/LFeSO4��Һ�м���1mL8mol/Lϡ���� | ��Һ��Ϊ��ɫ������һ��ʱ�����ɫ ��ʧ����Һ��Ϊ��ɫ |
̽������������ֵ�ԭ��
�������ϣ�Fe2++NO![]() Fe(NO)2+����ɫ��
Fe(NO)2+����ɫ��
(3)�����ӷ���ʽ����NO������ԭ��____________��
(4)�ӻ�ѧ��Ӧ�������ȵĽǶȶ���ϵ�д��ڵķ�Ӧ���з�����
��Ӧ��Fe2+��HNO3��Ӧ����Ӧ��Fe2+��NO��Ӧ
������ʵ��������Ϊ��Ӧ������ʱȷ�Ӧ��_______(��족������)��
������Ϊ��Ӧ����һ�������淴Ӧ����ͨ��ʵ��֤����²���ȷ������Ƶ�ʵ�鷽����_________________________��
�����û�ѧƽ���ƶ�ԭ��������Һ����ɫ��Ϊ��ɫ��ԭ��____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����98����Ũ����(�ܶ�Ϊ1.84 g/cm3 )����100 mL l mol/L��ϡ���ᡣ�ָ�����������(���ƹ����п����õ�)����100 mL��Ͳ ��10 mL��Ͳ ��50 mL�ձ� ��������ƽ ��100 mL����ƿ ��ͷ�ι� �߲���������ʹ���������Ⱥ�˳��������ȷ����.( )
A.�ܢۢߢݢޣ�B.�ڢݢߢޣ�C.�٢ۢݢޢߣ�D.�ڢޢۢߢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ѧʵ����Ҫ��ѧ����ʵ���������£��ñ����ߡ���ѧ��ѧʵ���ҳ��õ�������ƽ������ͼ��ʾ������������ϡ����Ϳ��ȡ���Ⱦ��ȵĴ�þ����þ��ÿ������Ϊ2.5g���ң��ⶨ����Ħ�������
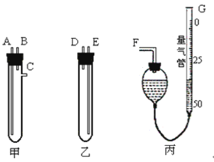
����ʵ�����ڱ�״���½��У��Իش��������⣺
��1��þ����ϡ����Ӧ�ֱ�����_________��_________�����У���������ţ���G�ܿ����û�ѧʵ�������һ�ֳ�����������װ������Ϊ����������������__________________��
��2������������������������ɣ���������Ƥ����ͨ����װ������ˮ�������ƶ����ܿ��Ե���Һ��ߵ͡��������Թܸ����������ܣ��������Ӷ�Ӧ�ӿں���ʢϡ������Թܣ�������Ӧ���ų����壬�ӿڵ����ӷ�ʽ���£�A����_________��B����_________��C����_________ ����д���ӿڵı�ţ���
��3��ʵ����Ҫȡ��һ��������þ����ƷͶ��ͼʾ�Թ��У�����Ϊ�ܷ�����ѧ��ѧʵ���ҳ��õ�������ƽ_________��������____________��
��4������Ϊ����ʲô����ȡþ����Ʒ_________�����ȡþ����l m������Ϊ m g����ȡþ����x cm�������������ΪV mL�����ñ��������Ħ�����Ӧ��ʾΪ��V��m��= _________Lmol-1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ����ͼ����ʵ�飬��A�зŵ��Ǹ���ĺ�ɫֽ����B�зŵ���ʪ��ĺ�ɫֽ����C��ʢ�ŵ�������������Һ����ش��������⡣
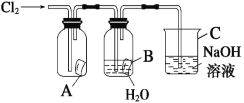
(1)ͨCl2һ��ʱ���A�й۲쵽��������_______________��B�й۲쵽��������_______________��д���йط�Ӧ�Ļ�ѧ����ʽ��_____________________________��
(2)Cװ�õ�������_____________________________��������_______________��д���йط�Ӧ�Ļ�ѧ����ʽ��_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ȼ���г���CaF2����ʽ���ڡ�
(1)���й���CaF2�ı�����ȷ����________��
a��Ca2����F��������ھ�����������
b��F�������Ӱ뾶С��Cl������CaF2���۵����CaCl2
c���������ӱ�Ϊ2��1�����ʣ�����CaF2���幹����ͬ
d��CaF2�еĻ�ѧ��Ϊ���Ӽ������CaF2������״̬���ܵ���
(2)CaF2������ˮ���������ں�Al3������Һ�У�ԭ����_______________(�����ӷ���ʽ��ʾ)����֪AlF![]() ����Һ�п��ȶ����ڡ�
����Һ�п��ȶ����ڡ�
(3)F2ͨ��ϡNaOH��Һ�п�����OF2��OF2���ӹ���Ϊ________��������ԭ�ӵ��ӻ���ʽΪ________��
(4)F2������±�ص��ʷ�Ӧ�����γ�±�ػ��������ClF3��BrF3�ȡ���֪��ӦCl2(g)��3F2(g)===2ClF3(g)����H����313 kJ��mol��1��F��F���ļ���Ϊ159 kJ��mol��1��Cl��Cl���ļ���Ϊ242 kJ��mol��1����ClF3��Cl��F����ƽ������Ϊ________kJ��mol��1��ClF3���ۡ��е��BrF3��________(��ߡ��͡�)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������ȡCl2�Ļ�ѧ����ʽΪMnO2+ 4HCl![]() MnCl2+ Cl2��+ 2H2O������146.0��HCl��ȫ�μӷ�Ӧʱ���ж���Ħ������������ԭ���ж���Ħ����ԭ������������ԭ����Ϊ���ٿˣ����ɵ����������ڱ�״���µ�����Ƕ���������ÿ��3 �֣�
MnCl2+ Cl2��+ 2H2O������146.0��HCl��ȫ�μӷ�Ӧʱ���ж���Ħ������������ԭ���ж���Ħ����ԭ������������ԭ����Ϊ���ٿˣ����ɵ����������ڱ�״���µ�����Ƕ���������ÿ��3 �֣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͭ�ǹ㷺Ӧ�������������Ԫ�������úϽ�ij����С���ij�Ⱦ���ͭԪ��(��25%BeO��71%CuS������FeS��SiO2)�л������ͭ���ֽ����Ĺ����������£�

��֪��I.�롢��Ԫ�ػ�ѧ�������ƣ�
��.�����²�����������ܶȻ��������±���

(1)��ҺA����Ҫ�ɷֳ�NaOH�⣬����_____________(�ѧʽ)��д����ӦI�к��뻯������������ᷴӦ�����ӷ���ʽ��_______________________________________________��
(2)����ҺC�к�NaCl��BeCl2������HCl��Ϊ�ᴿBeCl2���������ʵ�鲽��˳��Ϊ_______(����ĸ)
a.��������İ�ˮ b.ͨ�������CO2
c.���������NaOH d.����������HCl e.ϴ�� f.����
(3)MnO2�ܽ����������е���Ԫ������Ϊ���ʣ�д����Ӧ����CuS������Ӧ�Ļ�ѧ����ʽ��____________________________________________��
(4)��ҺD��c(Cu2+)=2.2mol��L��1��c(Fe3+)=0.008mol��L��1��c(Mn2+)=0.01mol��L��1����μ���ϡ��ˮ����pH�ɽ������η��룬���ȳ�������___________(�����ӷ���)��Ϊʹͭ���ӿ�ʼ������������Ӧ������Һ��pH����___________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com