
【题目】已知:有机物A的产量可以用来衡量一个国家的石油化工发展水平。现以A为主要原料合成F,其合成路线如下图所示。

(1)A分子中官能团的名称是____________,D中官能团的名称是________反应①的反应类型是___________反应。
(2)反应②的化学方程式是___________________________。
反应④的化学方程式是___________________________。
(3)E是常见的高分子材料,合成E的化学方程式是_____________________________。

(4)某同学用如右图所示的实验装置制取少量F。实验结束后,试管甲中上层为透明的、不溶于水的油状液体。
① 实验开始时,试管甲中的导管不伸入液面下的原因是______________。
②上述实验中饱和碳酸钠溶液的作用是(填字母) ________。
A.中和乙酸和乙醇
B.中和乙酸并吸收部分乙醇
C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出
D.加速酯的生成,提高其产率
③在实验室利用B和D制备F的实验中,若用1mol B和1mol D充分反应,__________(能/不能)生成1mol F,原因是 __________________。
【答案】碳碳双键 羧基 加成反应 2CH3CH2OH + O2![]() 2CH3CHO + 2H2O CH3COOH + CH3CH2OH
2CH3CHO + 2H2O CH3COOH + CH3CH2OH ![]() CH3COOCH2CH3 + H2O n CH2=CH2
CH3COOCH2CH3 + H2O n CH2=CH2 ![]()
![]() 防止倒吸 B C 不能 酯化反应为可逆反应
防止倒吸 B C 不能 酯化反应为可逆反应
【解析】
有机物A的产量可以用来衡量一个国家的石油化工发展水平,则A为CH2=CH2;结合图中转化可知,A和水发生加成反应生成B,B可发生连续氧化反应,则B为CH3CH2OH,C为CH3CHO,D为CH3COOH,CH3CH2OH和CH3COOH在浓硫酸作用下发生酯化反应生成CH3COOCH2CH3,E是常见的高分子材料,则乙烯发生加聚反应生成E为![]() ,以此来解答。
,以此来解答。
(1)A分子中官能团的名称是碳碳双键,D中官能团的名称是羧基;反应①为乙烯与水的加成反应,反应类型是加成反应;
(2)反应②为乙醇的催化氧化,反应的化学方程式是2CH3CH2OH + O2![]() 2CH3CHO + 2H2O,反应④为乙醇和乙酸的酯化反应,反应的化学方程式是CH3COOH + CH3CH2OH
2CH3CHO + 2H2O,反应④为乙醇和乙酸的酯化反应,反应的化学方程式是CH3COOH + CH3CH2OH ![]() CH3COOCH2CH3 + H2O;
CH3COOCH2CH3 + H2O;
(3)E是常见的高分子材料,合成E的化学方程式是nCH2=CH2 ![]()
![]() ;
;
(4)①因乙酸、乙醇易溶于水,实验开始时,试管甲中的导管不伸入液面下的目的是防止倒吸;
②上述实验中饱和碳酸钠溶液的作用是中和乙酸并吸收部分乙醇、降低乙酸乙酯在饱和碳酸钠溶液中的溶解度,有利于分层析出,故答案为BC;
③在实验室利用B和D制备乙酸乙酯的实验中,若用1mol B和1mol D充分反应,不能生成1mol乙酸乙酯,因为该反应是可逆反应,当反应达到一定限度时达到平衡状态。


科目:高中化学 来源: 题型:
【题目】在下列物质转化中,A是一种正盐,D的相对分子质量比C的相对分子质量大16,E是酸,当X无论是强酸还是强碱时,都有如下的转化关系:
![]()
当X是强酸时,A、B、C、D、E均含同一种元素;当X是强碱时,A、B、C、D、E都含另外同一种元素。请回答:
(1)A是__________,Y是__________,Z是__________。
(2)当X是强酸时,E是__________;B生成C的化学方程式是________________________。
(3)当X是强碱时,E是__________; B生成C的化学方程式是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y和Z为原子序数依次增大的四种短周期元素。X是短周期原子半径最大的元素,Y的最高化合价与最低价相加为0,Z是同周期非金属性最强的元素,W、X、Y三种元素形成的一种化合物结构如图所示。下列叙述正确的是
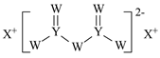
A.X单质的熔点高于Y单质
B.气态氢化物稳定性:Y<Z
C.Z的氧化物对应的水化物为强酸
D.X分别与W、Z形成的二元化合物溶于水显碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在有关限定条件下溶液中一定能大量共存的是( )
A. 由水电离产生的c(H+)=10-12mol/L的溶液中:K+、Na+、ClO-、I-
B. c(H+)=![]() mol/L的溶液中:K+、Fe3+、Cl-、CO32—
mol/L的溶液中:K+、Fe3+、Cl-、CO32—
C. 常温下,![]() =1×10-12的溶液:K+、AlO2—、CO32—、Na+
=1×10-12的溶液:K+、AlO2—、CO32—、Na+
D. pH=13的溶液中:AlO2—、Cl-、HCO3—、SO42—
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氧化还原反应的叙述中,正确的是( )
A.有单质参加的反应一定是氧化还原反应
B.燃烧反应必须有氧气作氧化剂
C.2Fe+3Cl2![]() 2FeCl3; Fe+S
2FeCl3; Fe+S![]() FeS 由此可以判断氧化性:Cl2>S
FeS 由此可以判断氧化性:Cl2>S
D.Mg在化学反应中失去2个电子,而Al在化学反应中失去3个电子,因此还原性Al>Mg
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】20℃时,在c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.100mol·L-1的H2C2O4、NaOH混合溶液中,含碳元素微粒的分布分数δ随溶液pH变化的关系如图所示。下列说法正确的是( )

A. 0.100 mol·L-1NaHC2O4溶液中:c(OH-)=c(H+)-2c(C2O42-)+c(H2C2O4)
B. Q点:c(H2C2O4)+c(C2O42-)>c(HC2O4-)
C. P点:c(Na+)+c(H2C2O4)<0.100mol·L-1+c(C2O42-)
D. 该温度下H2C2O4的电离常数Ka2=1×10-4.2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是四种原子序数依次增大的短周期元素,W、X两种元索可组成W2x和W2X2两种常见的无色液体化合物, Y2X2为淡黄色固体化合物,Z的原子序数是X的原子序数的两倍。请回答下列问题:
(1)Z元素的名称是___________ 。
(2)W、X、Y三种元素形成的化合物的电子式_____________
(3)写出Y2X2中所含化学键有:___________。
(4)写出Y2X2和W2X反应的化学方程式:_______________
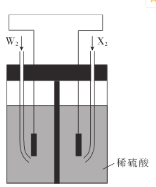
(5)W2和X2是组成某种燃料电池的两种常见物质,如图所示,通人X2的电极是___(填“正极”或“负极”),写出通人W2的电极的电极反应式:________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关物质的转化关系如下图所示。A为一种黄绿色的气体,B为常见的无色液体,H为一种助燃的气体,F为一种气体,它在A中燃烧产生苍白色火焰,E为一种能被磁铁吸引的金属。
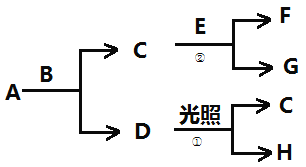
(1)B的化学式为____________。
(2)F的化学式为____________。
(3)写出反应②的化学方程式:_______________________________。
(4)写出反应①的化学方程式:_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知2KClO3 + H2C2O4 + H2SO4= K2SO4 + 2ClO2 + 2CO2 + 2H2O。
(1)用单线桥法表示该反应的电子转移的方向和数目_______。
(2)该反应的氧化剂是____,还原剂是_____,氧化产物是_____,还原产物是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com