
【题目】常温下,下列各组离子在有关限定条件下溶液中一定能大量共存的是( )
A. 由水电离产生的c(H+)=10-12mol/L的溶液中:K+、Na+、ClO-、I-
B. c(H+)=![]() mol/L的溶液中:K+、Fe3+、Cl-、CO32—
mol/L的溶液中:K+、Fe3+、Cl-、CO32—
C. 常温下,![]() =1×10-12的溶液:K+、AlO2—、CO32—、Na+
=1×10-12的溶液:K+、AlO2—、CO32—、Na+
D. pH=13的溶液中:AlO2—、Cl-、HCO3—、SO42—
 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源: 题型:
【题目】实验发现,298 K时,在氯化铁酸性溶液中加少量锌粒后,Fe3+立即被还原成Fe2+。某夏令营兴趣小组根据该实验事实设计了如图所示原电池装置。下列有关说法正确的是

A. 该原电池的正极反应是:Zn-2e-=Zn2+
B. 左烧杯中溶液的红色逐渐褪去
C. 该电池铂电极上立即有气泡出现
D. 该电池总反应为:3Zn+2Fe3+=2Fe+3Zn2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取 30.8g 甲酸铜[(HCOO)2Cu]在隔绝空气的条件下加热分解,会生成含两种红色固体的混合物 A 和混合气体 B;若相同质量的甲酸铜在空气中充分加热,则生成黑色固体 D 和 CO2、H2O。固体 A 和 D 质量相差 2.4g。则:
(1)红色固体 A 中 Cu 单质的物质的量为_________mol。
(2)将混合气体B 置于O2 中充分燃烧,消耗 O2 的体积是_________L (换算为标准状况)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一压强始终与外界大气压相同的密闭容器中,将适量硫粉和碳粉的混合物与一定量的O2完全反应,恢复到常温,放出504.875kJ的热量,反应后O2有剩余。在标准状况下测得反应后混合气体的体积为44.8L,已知反应后的混合气体中某种气体(A)的质量与物质的量均为另两种气体之和,且C(s)+O2(g) = CO2(g) ΔH=-393.5kJ/mol-1。
(1)投入O2的总体积在标准状况下的体积为____________L。
(2)A为_________。
A.SO2 B.CO2 C.O2 D.无法确定
(3)反应后混合气体的平均摩尔质量为__________________。
(4)混合气体中![]() =_____________。
=_____________。
(5)表示硫燃烧热的热化学方程式为_____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸是重要的化工原料,我国主要采用接触法生产硫酸,主要过程如下:
FeS2 ![]() SO2
SO2 ![]() SO3
SO3 ![]() H2SO4
H2SO4
回答下列问题:
(1)基态V原子的电子排布式为________,基态Fe原子核外未成对电子数为______。
(2)组成H2SO4的元素中,电负性由大到小的顺序是________,SO2分子的VSEPR模型为________。
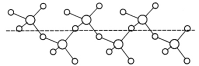
(3)固态SO3能以无限长链形式存在(如图所示)。其中S原子的杂化形式为______。长链结构中,连接2个S原子的O原子称为桥氧,连接1个S原子的O原子称为端基氧,则与S原子形成化学键键长更大的是________(填“桥氧”或“端基氧”),原因是______________。
(4)绿矾是一种重要的硫酸盐,其组成可写成[Fe(H2O)6]2+[SO4(H2O)]2-,水合阴离子中H2O通过氢键与SO42-中的O原子相联结,按图示画出含氢键的水合阴离子:______________。

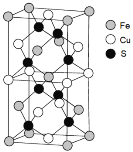
(5)一种含Fe、Cu、S三种元素的矿物晶胞如图所示,属于四方晶系(晶胞底面为正方形)。S2-的配位数为______。若晶胞的底面边长为a pm,高为b pm,晶体密度为ρ g/cm3,则阿伏加德罗常数可表示为____________(写出表达式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温时,将xmL pH=a的稀NaOH溶液与ymL pH=b的稀盐酸充分反应。下列关于反应后溶液pH的判断,正确的是( )
A. 若x=y,且a+b=14,则pH>7B. 若10x=y,且a+b=13,则pH=7
C. 若ax=by,且a+b=13,则pH=7D. 若x=10y,且a+b=14,则pH>7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:有机物A的产量可以用来衡量一个国家的石油化工发展水平。现以A为主要原料合成F,其合成路线如下图所示。

(1)A分子中官能团的名称是____________,D中官能团的名称是________反应①的反应类型是___________反应。
(2)反应②的化学方程式是___________________________。
反应④的化学方程式是___________________________。
(3)E是常见的高分子材料,合成E的化学方程式是_____________________________。

(4)某同学用如右图所示的实验装置制取少量F。实验结束后,试管甲中上层为透明的、不溶于水的油状液体。
① 实验开始时,试管甲中的导管不伸入液面下的原因是______________。
②上述实验中饱和碳酸钠溶液的作用是(填字母) ________。
A.中和乙酸和乙醇
B.中和乙酸并吸收部分乙醇
C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出
D.加速酯的生成,提高其产率
③在实验室利用B和D制备F的实验中,若用1mol B和1mol D充分反应,__________(能/不能)生成1mol F,原因是 __________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家合成出了一种用于分离镧系金属的化合物 A,其结构如下图所示。短周期元素 X、Y、Z原子序数依次增大,其中Z位于第三周期。Z与Y可以形成分子 ZY6,该分子常用作高压电气设备的绝缘介质。下列关于X、Y、Z的叙述,正确的是

A.化合物 A中,X、Y、Z最外层都达到8电子稳定结构
B.离子半径:Y>Z
C.最简单氢化物的沸点:Z>Y
D.最高价氧化物对应水化物的酸性:Z<X
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白藜芦醇是一种抗肿瘤的药物,合成它的一种路线如图:
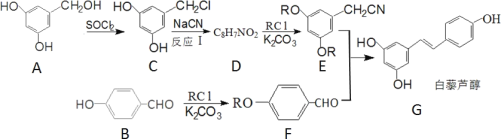
回答下列问题:
(1)B 的化学名称是_______;G 中含有的官能团名称是_________。
(2)反应I的反应类型为____________。
(3)D 的结构简式是______________。
(4)B的芳香类同分异构体中可以发生水解的结构简式为_____________;该有机物在 NaOH溶液作用下完全水解的化学反应方程式为______________。
(5)据已有知识并结合相关信息,写出以 ![]() 和 CH3OH 为原料制备
和 CH3OH 为原料制备 ![]() 的合成路线流程图______________(无机试剂任用)。 (已知 RCN
的合成路线流程图______________(无机试剂任用)。 (已知 RCN![]() RCOOH)合成路线流程图如下: (甲
RCOOH)合成路线流程图如下: (甲![]() 乙……
乙……![]() 目标产物)
目标产物)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com