
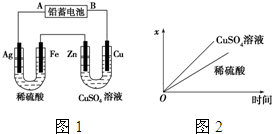
 已知铅蓄电池的工作原理为Pb+PbO2+2H2SO2
已知铅蓄电池的工作原理为Pb+PbO2+2H2SO2| 放电 |
| 充电 |
| 0.4mol |
| 2 |


科目:高中化学 来源: 题型:
| A、甲试管 | B、乙试管 |
| C、丙试管 | D、无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:
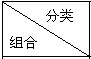 | 碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 |
| A | Na2CO3 | H2SO4 | NaHCO3 | SiO2 | CO2 |
| B | NaOH | HCl | NaCl | Na2O | CO |
| C | NaOH | CH3COOH | MgCl2 | CO2 | SO2 |
| D | KOH | HNO3 | CaCO3 | CaO | SO3 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
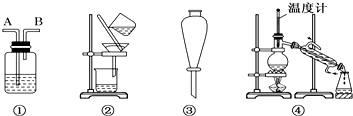
| 选项 | 物质 | 试剂 | 装置 |
| A | C2H6(C2H4) | ① | ① |
| B | 溴苯(溴) | ② | ③ |
| C | CH3COOC2H5(CH3COOH) | ③ | ② |
| D | 甲苯(二甲苯) | ① | ③ |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
 已知A、B、C是中学化学的常见物质,它们在一定条件下有如下转化关系:
已知A、B、C是中学化学的常见物质,它们在一定条件下有如下转化关系:查看答案和解析>>
科目:高中化学 来源: 题型:
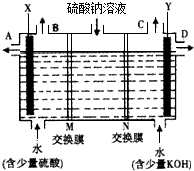
查看答案和解析>>
科目:高中化学 来源: 题型:
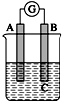 如图所示装置,检流计指针发生偏转,同时A极逐渐变粗,B极逐渐变细,C为电解质溶液,则A、B、C应是下列各组中的( )
如图所示装置,检流计指针发生偏转,同时A极逐渐变粗,B极逐渐变细,C为电解质溶液,则A、B、C应是下列各组中的( )| A、A是Zn,B是Cu,C为稀硫酸 |
| B、A是Ag,B是Fe,C为稀AgNO3溶液 |
| C、A是Fe,B是Ag,C为稀AgNO3溶液 |
| D、A是Cu,B是Zn,C为稀硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、石墨不如金刚石稳定 |
| B、等质量的石墨与金刚石相比,石墨具有的能量高 |
| C、等物质的量的石墨与金刚石完全燃烧,金刚石放出的能量多 |
| D、等物质的量的石墨与金刚石完全燃烧,石墨放出的能量多 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com