
 已知A、B、C是中学化学的常见物质,它们在一定条件下有如下转化关系:
已知A、B、C是中学化学的常见物质,它们在一定条件下有如下转化关系:| NaOH |
| NaOH |
| C |
| C |
| O2 |
| O2 |
| ||
| △ |
| ||
| △ |
| NaOH |
| NaOH |
| C |
| C |
| O2 |
| O2 |
| ||
| △ |
| ||
| △ |


科目:高中化学 来源: 题型:
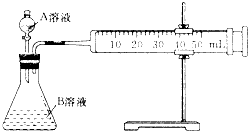
| 组别 | 10%硫酸体积/mL | 温度/℃ | 其他物质 |
| A | 2mL | 20 | |
| B | 2mL | 20 | 10滴饱和MnSO4溶液 |
| C | 2mL | 30 | |
| D | 1mL | 20 | V1 mL蒸馏水 |
| E | 0.5mL | 20 | V2 mL蒸馏水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 名称 | 托盘天平 | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
| 仪器 |  |  |  |  |  | |
| 序号 | a | b | c | d | e | f |
| 实验 次数 | 起始温度t1/℃ | 终止温度 t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、先装好药品,再检查装置的气密性 |
| B、先用双手捂紧试管,再将导管插入水中检查装置的气密性 |
| C、氢气还原氧化铜的实验,先通一段时间的氢气,后检验氢气纯度,再加热 |
| D、稀释浓硫酸时,先在烧杯里倒入浓硫酸,再小心倒入水并不断搅拌 |
查看答案和解析>>
科目:高中化学 来源: 题型:
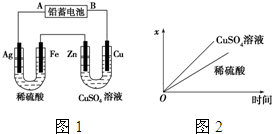 已知铅蓄电池的工作原理为Pb+PbO2+2H2SO2
已知铅蓄电池的工作原理为Pb+PbO2+2H2SO2| 放电 |
| 充电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 放电 |
| 充电 |
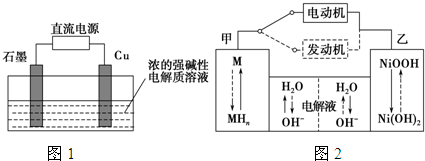
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图表示反应X(g)+Y(s)?Z(s)+R(g)(△H<0)的正、逆反应速率(v)与时间(t)的关系,t1时开始改变条件,则改变的条件符合曲线的是( )
如图表示反应X(g)+Y(s)?Z(s)+R(g)(△H<0)的正、逆反应速率(v)与时间(t)的关系,t1时开始改变条件,则改变的条件符合曲线的是( )| A、减少物质Z | B、升温 |
| C、减压 | D、用催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等于2cmol?L-1 |
| B、大于2cmol?L-1 |
| C、小于2cmol?L-1 |
| D、在c~2cmol?L-1之间 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com