
【题目】有Al2(SO4)3和Na2SO4的混合溶液V L,将它均分成两份。一份滴加氨水,使Al3+完全沉淀;另一份滴加BaCl2溶液,使SO![]() 完全沉淀。反应中消耗a mol NH3·H2O、b mol BaCl2。据此得知原混合溶液中的c(Na+)(mol·L-1)为( )
完全沉淀。反应中消耗a mol NH3·H2O、b mol BaCl2。据此得知原混合溶液中的c(Na+)(mol·L-1)为( )
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
【答案】D
【解析】
第一份发生的离子反应方程式为Al3++3NH3.H2O=Al(OH)3↓+3NH4+、第二份发生的离子反应方程式为Ba2++SO42-=BaSO4↓,再结合电荷守恒计算。
第一份发生的离子反应方程式为Al3++3NH3.H2O=Al(OH)3↓+3NH4+、第二份发生的离子反应方程式为Ba2++SO42-=BaSO4↓,根据Al3++3NH3.H2O=Al(OH)3↓+3NH4+得n(Al3+)=![]() n(NH3.H2O)=
n(NH3.H2O)=![]() mol,则混合溶液中c(Al3+)=
mol,则混合溶液中c(Al3+)=![]() =
=![]() mol/L;根据Ba2++SO42-=BaSO4↓得n(Ba2+)=n(SO42-)=bmol,则c(SO42-)=
mol/L;根据Ba2++SO42-=BaSO4↓得n(Ba2+)=n(SO42-)=bmol,则c(SO42-)=![]() =
=![]() mol/L,任何电解质溶液都呈电中性,根据电荷守恒得c(Na+)=2c(SO42-)-3c(Al3+)=
mol/L,任何电解质溶液都呈电中性,根据电荷守恒得c(Na+)=2c(SO42-)-3c(Al3+)=![]() mol/L-
mol/L-![]() mol/L=
mol/L=![]() mol/L。
mol/L。
答案选D。


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:
【题目】应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下"Fe与水蒸气反应的实验"。

请回答该实验中的问题。
(1)实验前必须对整套装置进行气密性的检查,操作方法是_____________。
(2)圆底烧瓶中盛装的是水,该装置受热后的主要作用是_______________;烧瓶底部放置了几片碎瓷片,碎瓷片的作用是_______________。
(3)酒精灯和酒精喷灯点燃的顺序是__________。
(4)干燥管中盛装的物质可以是_____________,作用是__________。
(5)如果要在A处玻璃管口处点燃该气体,则必须对该气体进行_________,这一操作的目的_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一恒温、恒容的密闭容器中充入一定量的N2O4气体,一段时间后容器中气体颜色逐渐变为红棕色:N2O4(g)![]() 2NO2(g)。下列结论不能说明该反应已经达到化学平衡状态的是( )
2NO2(g)。下列结论不能说明该反应已经达到化学平衡状态的是( )
A.v(N2O4):v(NO2)=1:2
B.容器内气体的压强不再变化
C.容器内气体的颜色不再变化
D.容器内气体的平均相对分子质量不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】—定条件下,向密闭容器中充入一定量的气体X,发生反应3X(g)![]() Y(g)+xZ(g),一段时间后反应达到平衡。12min时,将容器体积压缩至原来的一半,一段时间后反应再次达到平衡。反应中各时刻X物质的浓度如下表所示。下列说法中不正确的是( )
Y(g)+xZ(g),一段时间后反应达到平衡。12min时,将容器体积压缩至原来的一半,一段时间后反应再次达到平衡。反应中各时刻X物质的浓度如下表所示。下列说法中不正确的是( )
反应时间(min) | 0 | 5 | 12 | 17 | 20 |
X的浓度(mol·L-1) | 1.0 | 0.4 | 0.4 | 0.7 | 0.7 |
A.x=1
B.5min时该反应处于化学平衡状态
C.从反应开始到18min时,X的转化率为30%
D.05min内,该反应的平均速率为v(X)=0.12mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知 SO32ˉ+I2+H2O= SO42ˉ+2Iˉ+2H+,将 0.09molCl2通入 100mL 含 a molNaI与 a mol Na2SO4的混合溶液中,有 0.25a mol的 NaI 被氧化(不考虑 Cl2 与 I2 之间的反应),则下列说法正确的是
A.物质的还原性 Iˉ >SO32ˉ
B.NaI 与 Na2SO3 的物质的量浓度为 0.08mol/L
C.通入 0.09molCl2 发生反应的离子方程式为:8SO32ˉ+2Iˉ+9Cl2+8H2O=8SO42ˉ+I2+16H++18Clˉ
D.若再通入0.07molCl2,恰好能将 NaI与 Na2SO3 完全氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一瓶澄清的溶液,只可能含有 NH4+、Na+、Mg2+、Ba2+、Fe3+、Clˉ、Brˉ、Iˉ、CO32ˉ、SO42—中的几种,且浓度均为 0.1mol L—1。进行以下实验:
①取少量溶液,滴加盐酸至溶液呈酸性,无明显现象。
②取少量溶液,滴加少许新制氯水,再加淀粉溶液,溶液变蓝
③取少量溶液,向其中逐滴加入 NaOH 溶液至碱性,过程中均无沉淀产生。将此溶液分为两等份,第一份加热,有气体放出;第二份溶液中加入Na2CO3 溶液,有白色沉淀生成。下列结论不正确的是
A.肯定含有的阳离子是 NH4+、Ba2+
B.肯定含有的阴离子是Iˉ、Clˉ、Brˉ
C.肯定不含有的离子是 Fe3+、CO32ˉ、SO42ˉ
D.不能确定是否含有的离子是 Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知酸性:苯甲酸>碳酸>苯酚,现将![]() 转变为
转变为![]() 的方法为( )
的方法为( )
A.与稀H2SO4共热后,加入足量的Na2CO3
B.加入足量的NaOH溶液,再通入足量的HCl
C.与足量的NaOH溶液共热后,再通入CO2
D.与稀H2SO4共热后,加入足量的NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 烷烃的通式为CnH2n+2,随n值增大,碳元素的质量百分含量逐渐减小
B. 乙烯与溴加成反应的产物为溴乙烷
C. 1 mol苯恰好与3 mol氢气完全加成,说明苯分子中有三个碳碳双键
D. 当n=7,主链上有5个碳原子的烷烃共有5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金刚烷是一种重要的化工原料,如合成的金刚烷胺就是一种抗病毒药剂,对帕金森症、老年痴呆有良好的疗效.由环戊二烯合成金刚烷的路线如下:
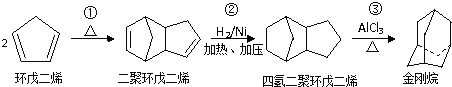
请回答下列问题:
(1)金刚烷的分子式为 ______ .
(2)反应①的反应类型是 ______ .
(3)金刚烷与四氢二聚环戊二烯的关系是 ______ .(填字母)
a 互为同系物 b 互为同分异构体 c 均为烷烃 d 均为环烃
(4)下面是以环戊烷为原料制备环戊二烯的合成路线:
![]()
其中,反应②的反应试剂和反应条件是 ______ ;X的名称是 ______ ;反应④的化学方程式是 ______ ;
(5)A是二聚环戊二烯的同分异构体,能使溴的四氯化碳溶液褪色,A经高锰酸钾酸性溶液加热氧化可以得到对苯二甲酸[提示:苯环上的烷基(-CH3、-CH2R、-CHR2)或烯基侧链经高锰酸钾酸性溶液氧化得羧基],则A的结构有 ______ 种(不考虑立体异构),其中核磁共振氢普为5组峰,且面积比为4:1:2:2:3的结构简式是 ______ .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com