
【题目】已知酸性:苯甲酸>碳酸>苯酚,现将![]() 转变为
转变为![]() 的方法为( )
的方法为( )
A.与稀H2SO4共热后,加入足量的Na2CO3
B.加入足量的NaOH溶液,再通入足量的HCl
C.与足量的NaOH溶液共热后,再通入CO2
D.与稀H2SO4共热后,加入足量的NaOH
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:高中化学 来源: 题型:
【题目】海藻中含有丰富的碘元素。如图是实验室从海藻里提取碘的流程的一部分。下列判断正确的是

A. 步骤④的操作是过滤
B. 可用淀粉溶液检验步骤②的反应是否进行完全
C. 步骤①、③的操作分别是过滤、萃取
D. 步骤③中加入的有机溶剂可能是酒精或四氯化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述与图象相对应的是
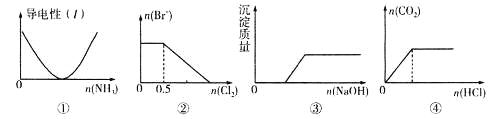
A.图①表示向乙酸溶液中通入氨气至过量的过程中溶液导电性的变化
B.图②表示向1 L l mol·L-1FeBr2溶液中通入Cl2时Br-物质的量的变化
C.图③表示向Ca(HCO3)2溶液中滴加NaOH溶液时沉淀质量的变化
D.图④表示向一定浓度的Na2CO3溶液中滴加盐酸,生成CO2的物质的量与滴加盐酸物质的量的关系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有Al2(SO4)3和Na2SO4的混合溶液V L,将它均分成两份。一份滴加氨水,使Al3+完全沉淀;另一份滴加BaCl2溶液,使SO![]() 完全沉淀。反应中消耗a mol NH3·H2O、b mol BaCl2。据此得知原混合溶液中的c(Na+)(mol·L-1)为( )
完全沉淀。反应中消耗a mol NH3·H2O、b mol BaCl2。据此得知原混合溶液中的c(Na+)(mol·L-1)为( )
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(化学---选修5有机化学基础)2005年诺贝尔化学奖授予了研究烯烃复分解反应的科学家,以表彰他们作出的卓越贡献。烯烃复分解反应原理如下:现以烯烃C5H10为原料,合成有机物M和N,合成路线如下:
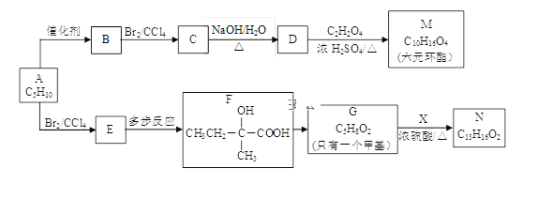
(1)按系统命名法,有机物A的名称是___________。
(2)B的结构简式是___________。
(3)写出D![]() M的化学方程式___________。
M的化学方程式___________。
(4)写出E![]() F合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)___________。
F合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)___________。
(5)已知X的苯环上只有一个取代基,且取代基无甲基,则N的结构简式为_________。
(6)满足下列条件的X的同分异构体共有_____种,写出任意一种的结构简式_____。
①遇FeCl3溶液显紫色 ②苯环上的一氯取代物只有两种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氰酸铵(NH4CNO)受热转化成尿素[CO(NH2)2]的反应在有机化学史上具有里程碑事件,打破了“有机物不能有无机物制得”的观念。在后来的实验中发现,尿素可以由氨气和二氧化碳反应生成,尿素也可以在一定条件下失去氨而缩合,如两分子尿素失去一分子氨,则形成二聚物--缩二脲。下列关于尿素及其缩合产物的说法中错误的是( )
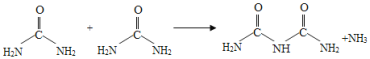
A.与尿素分子式相同的物质有不止一种
B.可以推测,尿素也可以缩合形成聚合产物
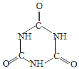
C.缩二脲中有肽键,因此缩二脲是一种二肽
D.若尿素生成三聚产物--缩三脲,则生成一分子缩三脲的同时,失去两分子氨
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某天然碱可以看作是CO2 和 NaOH 反应后的产物组成的一种物质。为了研究该物质的组成,进行如下实验:
ⅰ称取 3.98 g 天然碱样品,加入 50mL 稀盐酸(足量),产生 CO2 896mL(标准状况)。
ⅱ称取 3.98g 天然碱样品,加热至分解完全,产生 CO2 224mL(标准状况)和 0.36g 水。
①该稀盐酸的物质的量浓度最小是_____________。
②天然碱的化学式是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】扁桃酸衍生物是重要的医药中间体,以A和B为原料合成扁桃酸衍生物F路线如下:
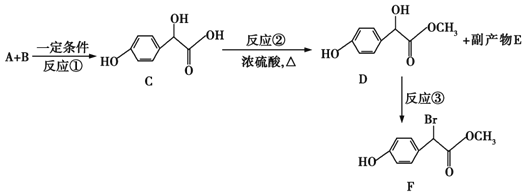
(1)A的分子式为C2H2O3,1molA能消耗含有2.5molCu(OH)2的新制悬浊液,写出A的结构简式______,B的结构简式______。
(2)反应②的反应类型为______反应;请写出反应②的化学方程式_________。
(3)在一定条件下F与足量NaOH溶液反应,1molF最多消耗NaOH的物质的量为______mol。
(4)符合下列条件的F的所有同分异构体(不考虑立体异构)有______种,其中核磁共振氢谱有五组峰的结构简式为______。
①属于一元酸类化合物 ②苯环上只有2个取代基 ③遇FeCl3溶液显紫色
(5)参照上述合成路线,以冰醋酸为原料(无机试剂任选),设计制备A的合成路线:__________。
[已知:RCH2COOH![]() RCH(Cl)COOH]
RCH(Cl)COOH]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)Cu+基态核外电子排布式为__________。
(2)基态Fe原子有______个未成对电子,Fe3+的电子排布式为__________。
(3)S的基态原子核外有_____个未成对电子;Si的基态原子核外电子排布式为_______________。
(4)Cu的价层电子轨道示意图为_____。
(5)基态Si原子中,电子占据的最高能层符号为_____,该能层具有的原子轨道数为_____,电子数为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com