
【题目】实验室用苯、浓H2SO4和浓HNO3 制备硝基苯的实验装置如图所示,发生反应方程式:![]() +HO-NO2→
+HO-NO2→![]() +H2O,下列说法错误的是
+H2O,下列说法错误的是
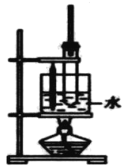
A.反应中浓H2SO4 的作用是催化剂、脱水剂
B.温度计的作用是测水浴的温度,长导管的主要作用是平衡气压
C.实验制得的硝基苯处于混合液的下层
D.从试管内混合物中分离出硝基苯可将反应后的混合物倒入水中,再分液
科目:高中化学 来源: 题型:
【题目】为了研究化学反应A+B===C+D的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升。试回答下列问题:
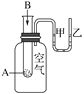
(1)该反应________(填“放出”或“吸收”)热量。
(2)如图能正确表示该反应中能量变化的是___________。
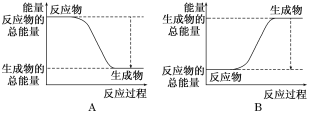
(3)写出一个符合题中条件的化学方程式:_______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D和E五种分子所含原子的数目依次为1、2、3、4和6,且都含有18个电子,又知B、C和D是由两种元素的原子组成,且D分子中两种原子个数比为1:1。请回答:
(1)组成A分子的原子的核外电子排布式是________________;
(2)B的分子式分别是 ___________;C分子的立体结构呈_________ 形,该分子属于_____________分子(填“极性”或“非极性”);
(3)向D的稀溶液中加入少量氯化铁溶液,反应的化学方程式为_____________________________
(4) 若将1molE在氧气中完全燃烧,只生成1molCO2和2molH2O,则E的分子式是 __________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,A是制取溴苯的实验装置,B、C是改进后的装置。请仔细分析,对比三个装置,回答下列问题:


(1)写出三个装置中发生反应的主要化学方程式:________________。写出B中右边试管中所发生反应的化学方程式:__________________。
(2)装置A和C均采用了长玻璃导管,其作用是_______、____________。
(3)在实验B、C装好仪器及药品后要使反应开始,应对装置B进行的操作是________________;应对装置C进行的操作是_______________________。
(4)装置B、C较好地解决了A中加装药品和使装置及时密封的矛盾,方便了操作。A装置中这一问题在实验中造成的后果是_________________。
(5)B中采用了洗气瓶吸收装置,其作用是______________________,反应后洗气瓶中可能出现的现象是_______________。
(6)B装置也存在两个明显的缺点,使实验的效果不好或不能正常进行。这两个缺点是_____________________;_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E均为有机物,其中A是化学实验中常见的有机物,它易溶于水并有特殊香味;B的产量可衡量一个国家石油化工发展的水平,有关物质的转化关系如图甲所示:
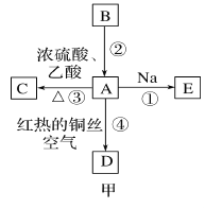
(1)写出B的结构简式________;A中官能团的名称为________。
(2)验证有机物乙酸中含有![]() 所用的试剂是_______,实验现象是_______。
所用的试剂是_______,实验现象是_______。
(3)写出下列反应的化学方程式:
反应①______________;
反应④______________。
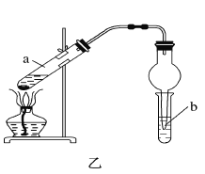
(4)实验室利用反应③制取C,常用上图乙装置:
①a试管中主要反应的化学方程式为_________。反应类型是________。
②在实验中球形干燥管除起冷凝作用外,另一个重要作用是__________。
③试管b中观察到的现象是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法不正确的是( )
A. 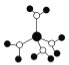 水合铜离子的模型如图所示,1个水合铜离子中有4个配位键
水合铜离子的模型如图所示,1个水合铜离子中有4个配位键
B. 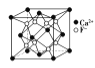 CaF2晶体的晶胞如图所示,每个CaF2晶胞平均占有4个Ca2+
CaF2晶体的晶胞如图所示,每个CaF2晶胞平均占有4个Ca2+
C.  H原子的电子云图如图所示,H原子核外的大多数电子在原子核附近运动
H原子的电子云图如图所示,H原子核外的大多数电子在原子核附近运动
D.  金属Cu中Cu原子堆积模型如图所示,该金属晶体为最密堆积,每个Cu原子的配位数均为12
金属Cu中Cu原子堆积模型如图所示,该金属晶体为最密堆积,每个Cu原子的配位数均为12
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羟氨(NH2OH )为一元弱碱 (25℃时 ,电离常数 Kb=9.0×l0-9), 其电离方程式为:NH2OH+H2O![]() NH3OH+ +OH-。用 0.lmol/L 盐酸滴定 20mL0.l mol/L NH2OH 溶液,恒定 25℃时, 滴定过程中由水电离出来OH-浓度的负对数与盐酸体积的关系如图所示(已知:lg3=0.5) 。 下列说法正确的是
NH3OH+ +OH-。用 0.lmol/L 盐酸滴定 20mL0.l mol/L NH2OH 溶液,恒定 25℃时, 滴定过程中由水电离出来OH-浓度的负对数与盐酸体积的关系如图所示(已知:lg3=0.5) 。 下列说法正确的是
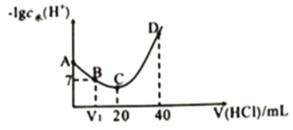
A.A、B、C、D 四点对应的溶液中 NH2OH 电离常数不相等
B.A 点对应溶液的 pH=8.5
C.D点对应溶液中存在:c(H+)=c(OH-)+c(NH3OH+)+c(NH2OH)
D.B点时溶液呈中性,C 点时溶液呈酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学用图所示装置制取氨,并探究其性质。
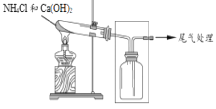
(1)制取氨气的化学方程式是______。
(2)采用图示的方法收集氨气,是因为氨气的密度比空气 ______(填“大”或“小”)。
(3)将蘸有浓盐酸的棉球放在玻璃片上,用集满NH3的集气瓶扣住棉球,可观察到的现象是______。
(4)甲同学设计了下图所示的装置进行尾气处理,乙同学认为该设计不合理,请画出正确的尾气吸收图______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯(ClO2)是一种黄绿色气体,易溶于水,在混合气体中的体积分数大于10%就可能发生爆炸,在工业上常用作水处理剂、漂白剂。回答下列问题:
(1)在处理废水时,ClO2可将废水中的CN-氧化成CO2和N2,该反应的离子方程式是_______。
(2)某小组按照文献中制备ClO2的方法设计了如图所示的实验装置用于制备ClO2。
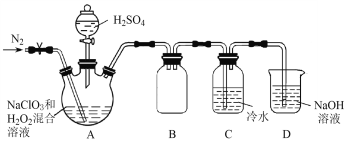
①通入氮气的主要作用有2个,一是可以起到搅拌作用,二是____________________。
②装置B的作用是__________________。
③装置A用于生成ClO2气体,该反应的化学方程式是_______________________________。
(3)测定装置C中ClO2溶液的浓度:取10.00 mL C中溶液于锥形瓶中,加入足量的KI溶液和H2SO4酸化,然后加入___________________作指示剂,用0.100 0 mol![]() L-1的Na2S2O3标准液滴定锥形瓶中的溶液(I2 + 2S2O32-=2I-+ S4O62-),消耗标准溶液的体积为20.00 mL。滴定终点的现象是______________________________,C中ClO2溶液的浓度是__________mol
L-1的Na2S2O3标准液滴定锥形瓶中的溶液(I2 + 2S2O32-=2I-+ S4O62-),消耗标准溶液的体积为20.00 mL。滴定终点的现象是______________________________,C中ClO2溶液的浓度是__________mol![]() L-1。
L-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com