
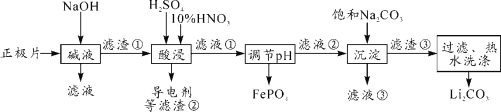
【题目】2019年诺贝尔化学奖授予对锂离子电池研究的贡献。磷酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一。采用湿法冶金工艺回收废旧磷酸亚铁锂电池正极片(除LiFePO4外,还含有Al箔、少量不溶于酸碱的导电剂)中的资源,部分流程如图:
(1)“碱溶”时Al箔溶解过程中,氧化剂是______________。
(2)“酸浸”时生成NO的离子方程式是_________。(其他杂质不与HNO3反应)
(3)实验测得滤液②中c(Li+)=4 mol·L-1,加入等体积的Na2CO3溶液后,Li+的沉降率为90%,则加入饱Na2CO3 溶液中c(Na2CO3)=______ mol·L-1。[Ksp(Li2CO3)=1.6×10-3]
(4)磷酸亚铁锂电池总反应为:LiFePO4+6C![]() Li1-xFePO4+LixC6,电池中的固体电解质可传导Li+。充电时,该电池的负极接电源的_____(填“正极”或“负极”);放电时,正极反应式为_______。
Li1-xFePO4+LixC6,电池中的固体电解质可传导Li+。充电时,该电池的负极接电源的_____(填“正极”或“负极”);放电时,正极反应式为_______。
(5)磷酸亚铁锂电池中铁的含量可通过如下方法测定:称取1.20g试样用盐酸溶解,在溶液中加入稍过量的SnCl2溶液,再加入HgCl2饱和溶液,用二苯胺磺酸钠作指示剂,用0.020mol·L-1重铬酸钾溶液滴定至溶液由浅绿色变为蓝紫色,消耗重铬酸钾溶液40.00mL。
已知:2Fe3++Sn2++6Cl-=SnCl62-+2Fe2+
4Cl-+Sn2++2HgCl2=SnCl62-+Hg2Cl2
6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O
①实验中加入HgCl2饱和溶液的目的是_________。
②磷酸亚铁锂电池中铁的含量为________%。
【答案】H2O 3LiFePO4+NO3-+4H+=3Li++NO↑+3PO43-+2H2O+3Fe3+ 1.88 负极 Li1-xFePO4+xLi++xe-=LiFePO4 将溶液中过量Sn2+转化为稳定的SnCl62-,防止其干扰Fe2+的测定 22.4
【解析】
分析流程图,磷酸亚铁锂电池正极片碱溶时,Al转化为NaAlO2,过滤后,滤渣中含有磷酸亚铁锂,向其中加入硫酸和硝酸进行酸浸,得到含Li+、Fe3+、H+、SO42-、NO3-和PO43-的滤液,调节溶液的pH,使得Fe3+以FePO4的形式除去,过滤后得到含Li+、H+、SO42-和NO3-的滤液,加入饱和Na2CO3溶液,将Li+转化为Li2CO3,通过过滤、热水洗涤等操作得到最终产物。据此进行分析。
(1)“碱溶”时Al箔溶解过程中发生的反应方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,反应实质为2Al+6H2O=2Al(OH)3+3H2↑,Al(OH)3+NaOH=NaAlO2+2H2O,根据氧化还原原理,化合价降低是H2O中的H,因此氧化剂为:H2O;
(2)酸浸时,磷酸亚铁锂电池正极片上的Fe2+与HNO3反应,生成Fe3+和NO,反应的离子反应方程式为:3LiFePO4+NO3-+4H+=3Li++NO↑+3PO43-+2H2O+3Fe3+;
(3)滤液②中c(Li+)=4mol·L-1,加入等体积的Na2CO3溶液后,Li+的沉降率为90%,则Li+的转化浓度为![]() ,由关系式:2Li+~CO32-可知,CO32-的转化浓度为
,由关系式:2Li+~CO32-可知,CO32-的转化浓度为![]() 。滤液②中加入等体积的Na2CO3溶液后,c(Li+)=
。滤液②中加入等体积的Na2CO3溶液后,c(Li+)=![]() ,由碳酸锂溶度积Ksp(Li2CO3)=
,由碳酸锂溶度积Ksp(Li2CO3)=![]() ,可得c(CO32-)=
,可得c(CO32-)=![]() ,则原饱和Na2CO3溶液中c(Na2CO3)=
,则原饱和Na2CO3溶液中c(Na2CO3)=![]() ;
;
(4)根据电池总反应:LiFePO4+6C![]() Li1-xFePO4+LixC6,放点过程中,C6x-中的C的化合价升高生成C单质,失去电子,作负极,可知,LixC6极为原电池的负极,充电时为阴极,发生还原反应,则应与电源的负极相连。放电时,原电池的正极发生还原反应,则反应方程式为:Li1-xFePO4+xLi++xe-=LiFePO4;
Li1-xFePO4+LixC6,放点过程中,C6x-中的C的化合价升高生成C单质,失去电子,作负极,可知,LixC6极为原电池的负极,充电时为阴极,发生还原反应,则应与电源的负极相连。放电时,原电池的正极发生还原反应,则反应方程式为:Li1-xFePO4+xLi++xe-=LiFePO4;
(5)①根据题给信息,SnCl2溶液稍过量,为了排除溶液中过量Sn2+干扰Fe2+的测定,故用HgCl2饱和溶液将其转化为稳定的SnCl62-。
②由题给已知条件,可得关系式:6Fe3+~Cr2O72-,则有:

解得:![]() ;则磷酸亚铁锂电池中铁的含量为
;则磷酸亚铁锂电池中铁的含量为![]() 。
。


科目:高中化学 来源: 题型:
【题目】密闭容器中发生可逆反应:H2(g)+I2(g)![]() 2HI(g)达到平衡状态时的标志是
2HI(g)达到平衡状态时的标志是
A.容器的压强恒定不变
B.混合气体的颜色不再改变
C.H2、I2、HI的浓度相等
D.I2在混合气体中的体积分数与H2在混合气体中的体积分数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温下D为生活中常见的无色无味的液体,F为淡黄色粉末(反应条件均已省略),请根据下列要求回答有关问题:
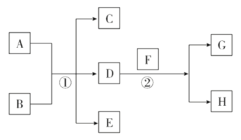
(1)写出②的化学方程式________________________ ,当生成5.6 L气体G(标准状况)时,此时反应转移的电子数目为(阿伏加德罗常数为NA)________。
(2)若A,C,E均含有氯元素,且A为单质,B为强碱溶液,写出该条件下反应①的离子方程式:__________________________________。
(3)若C,E均为气体且都能使澄清石灰水变浑浊,A为固体单质,写出该条件下反应①的化学方程式:_______________________________。
(4)若A与B均为固体化合物,E是能使湿润的红色石蕊试纸变蓝的气体,反应①常用于实验室制取气体E,写出该反应的化学方程式:_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是一种常见的单质,B、C为常见的化合物,A、B、C均含有元素x,它们有如图所示的转化关系(部分产物及反应条件已略去)。下列说法中正确的是( )
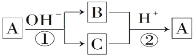
A. 反应①和②一定为氧化还原反应
B. 反应①和②互为可逆反应
C. X元素可能是金属,也可能是非金属
D. X元素可能为铝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】贝诺酯是由阿司匹林、扑热息痛经化学法拼合制备的解热镇痛抗炎药,其合成反应式(反应条件略去)如下:
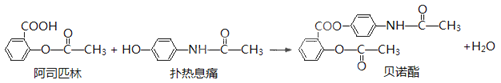
下列叙述错误的是
A. FeCl3溶液可区别阿司匹林和扑热息痛
B. 1mol阿司匹林最多可消耗2mol NaOH
C. 常温下贝诺酯在水中的溶解度小于扑热息痛
D. C6H7NO是扑热息痛发生类似酯水解反应的产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】植物在冬季来临过程中,随着气温的逐渐降低,体内发生了一系列适应低温的生理生化变化,抗寒力逐渐增强。下图为冬小麦在不同时期含水量和呼吸速率变化关系图,据图推断错误的是

A. 结合水与自由水含量的比值,与小麦的抗寒性呈正相关
B. 总含水量下降是因为细胞呼吸增强,需要消耗更多的水
C. 随着气温和土壤温度的下降,小麦的含水量下降
D. 11月时,小麦细胞中含量最多的化合物仍是水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨既是一种重要的化工产品,又是一种重要的化工原料。下图为合成氨以及氨氧化制硝酸的流程示意图。
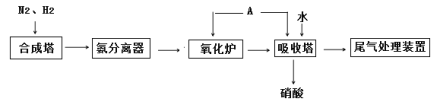
(1)写出合成塔中发生反应的化学方程式____________________,
(2)写出氧化炉中发生反应的化学方程式____________________
(3)A物质为______,向吸收塔中通入A的作用__________
(4)工业生产中为了盛装大量浓硝酸,可选择___作为罐体材料
A. 铜 B.铂 C.铝 D.镁
(5)为避免尾气氮氧化物污染环境,人们开发了溶液吸收、催化还原等尾气处理方法。前者使用具有碱性的Na2CO3溶液等吸收尾气,后者在催化下使用NH3或其他物质将氮氧化物还原为N2。请以尾气中的NO2处理为例,写出相关反应的化学方程式____________、_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种化合物的结构如图所示,其中X、Y、Z、Q、W为原子序数依次增大的五种短周期主族元素,Q核外最外层电子数与Y核外电子总数相同,X的原子半径是元素周期表中最小的。下列叙述正确的是( )

A.WX的水溶液呈碱性
B.元素非金属性的顺序为:Y>Z>Q
C.由X、Y、Q、W四种元素形成的化合物的水溶液一定呈碱性
D.该化合物中与Y单键相连的Q满足8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用 AgNO3 溶液分别滴定浓度均为 0.01 mol/L 的KCl、K2C2O4 溶液,所得的沉淀溶解平衡图像如图所示(不考虑 C2O42-的水解)。已知 Ksp(AgCl) 数量级为 10-10。下列叙述正确的是

A.图中 Y 线代表的 AgCl
B.n 点表示 Ag2C2O4 的过饱和溶液
C.向 c(Cl-)=c(C2O42-)的混合液中滴入 AgNO3溶液时,先生成 AgCl 沉淀
D.Ag2C2O4+2Cl-=2AgCl+C2O42-的平衡常数为 10-0.71
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com