
| A、NH3、HCl的水溶液都能导电,但NH3不是电解质 |
| B、Na2O、Na2O2组成元素相同,与CO2反应产物也相同 |
| C、CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 |
| D、新制氯水和SO2都具有漂白性,都能使紫色石蕊试液褪色 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
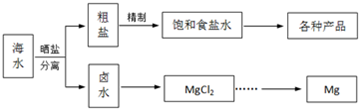
| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Mn(OH)2 | 8.3 | 9.5 |
| Mg(OH)2 | 10.0 | 11.1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、含5个碳原子的有机物,每个分子中最多可形成4个C-C单键 |
| B、油脂都不能使溴的四氯化碳溶液褪色 |
| C、可用新制的氢氧化铜悬浊液检验淀粉是否水解完全 |
| D、煤油可由石油分馏获得,可用作燃料和保存少量金属钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、元素的非金属性越强,单质的活泼性一定越强 |
| B、分子晶体中分子间的作用力越大,分子越稳定 |
| C、离子晶体发生状态变化时,一定会破坏离子键 |
| D、分子中含有两个氢原子的酸,一定就是二元酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c1=c2 |
| B、c1>c2 |
| C、c1≥c2 |
| D、c1<c2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、煤炭经气化,液化和干馏等过程,可获得清洁能源和重要的化工原料 |
| B、漂白粉和漂粉精不仅可以漂白棉,麻,纸张,还可做环境消毒剂 |
| C、Fe3O4俗称铁红,常做红色油漆和涂料 |
| D、蛋白质、淀粉、纤维素均属于天然有机高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 微热 |
A、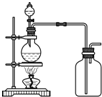 |
B、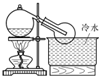 |
C、 |
D、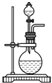 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钢柱在水下部分比在空气与水交界处更容易腐蚀 |
| B、与铜质水龙头连接处的钢质水管不易发生腐蚀 |
| C、可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 |
| D、在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com