
����Ŀ����˾ƥ��(��ѧ����Ϊ����ˮ����)�Ǿ��нⶾ����ʹ�ȹ�Ч�ļ�ͥ����ҩ����ѧ�����������ڸ߷����������Ƴɻ��ͳ�Ч��˾ƥ�֣��䲿�ֺϳɹ������£�
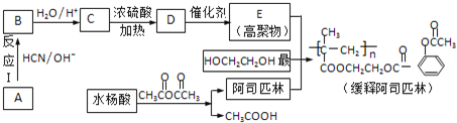
��֪��ȩ��ͪ���ɷ������з�Ӧ��CH3CHO ![]()
(1)ˮ����Ļ�ѧ����Ϊ���ǻ������ᣬ��ˮ����Ľṹ��ʽΪ__��
(2)��Ӧ��ķ�Ӧ������__��Ӧ��HOCH2CH2OH����1��2�����������Ʊ���ʵ�ָ��Ʊ�����ķ�Ӧ�Լ���__��
(3)д��C��D�ķ�Ӧ����ʽ______��
(4)C�ɷ������۷�Ӧ���ɸ߾���ø߾���Ľṹ��ʽΪ____��
(5)��˾ƥ����״������IJ���������������Һ�г�ַ�Ӧ�Ļ�ѧ����ʽΪ______��
(6)����˵����ȷ����__��
a�����ð�˾ƥ�ֳ���ˮ�����ж���Ӧ����ͣҩ��������ע��NaHCO3��Һ
b��1mol HOCH2CH2OH�Ĵ�����������������Һ��Ӧ���������������2mol��
c��A�ĺ˴Ź�������ֻ��һ���
d��������C����������Ӧ������8Ԫ��״��
(7)д�����Ͱ�˾ƥ��������ˮ�����ɰ�˾ƥ�֡��߾���E�����ʵķ�Ӧ����ʽ__��
(8)ˮ�����ж���ͬ���칹�壬�������ڷ������ܷ���������Ӧ��ͬ���칹����__�֡�
���𰸡�![]() �ӳɷ�Ӧ ����������Һ
�ӳɷ�Ӧ ����������Һ ![]() +H2O
+H2O ![]()
![]() +3NaOH
+3NaOH ![]() CH3COONa+CH3OH+H2O ac
CH3COONa+CH3OH+H2O ac  9
9
��������
���ݻ��Ͱ�˾ƥ�ּ���˾ƥ�֡��Ҷ����Ľṹ��ʽ֪��E�Ǿ��춡ϩ�ᣬD�ڴ�������������E����D���춡ϩ�ᣬB�ữ����C��C������ȥ��Ӧ�����춡ϩ�ᣬ���������Ϣ֪��A�DZ�ͪ��B�Ľṹ��ʽΪ��CH3C��OH����CN��CH3��C�Ľṹ��ʽΪ��HOC��CH3��2COOH��ˮ����Ļ�ѧ����Ϊ���ǻ������ᣬ��ˮ����Ľṹ��ʽΪ![]() ��
��
(1)ˮ����Ļ�ѧ����Ϊ���ǻ������ᣬ��ˮ����Ľṹ��ʽΪ![]() ��
��
(2)��ͪ�������ᷢ���ӳɷ�Ӧ����B����Ӧ��ķ�Ӧ�����Ǽӳɷ�Ӧ��HOCH2CH2OH����1��2����������ͨ��ȡ����Ӧ�Ʊ����ڼ��������£�1��2-����������������Ƶ�ˮ��Һ����ȡ����Ӧ�����Ҷ���������ʵ�ָ��Ʊ�����ķ�Ӧ�Լ����������Ƶ�ˮ��Һ��
(3)C�Ľṹ��ʽΪ��HOC��CH3��2COOH��D���춡�ᣬ��C��D�ķ�Ӧ����ʽΪ��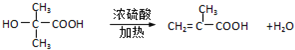 ��
��
(4)C�Ľṹ��ʽΪ��HOC��CH3��2COOH��C�ɷ������۷�Ӧ���ɸ߾���ø߾���Ľṹ��ʽΪ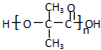 ��
��
(5)��˾ƥ����״������IJ���������������Һ�г�ַ�Ӧ�Ļ�ѧ����ʽΪ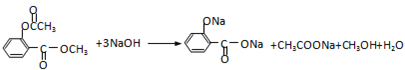 ��
��
(6)a�����ð�˾ƥ�ֳ���ˮ�����ж���Ӧ����ͣҩ��������ע��NaHCO3��Һ�кͣ�����ȷ��
b��1mol HOCH2CH2OH�Ĵ�����������Ժ���2��ȩ������������Һ��Ӧ���������������4mol�����ʴ���
c��A�DZ�ͪ����ͪ��ֻ��һ����ԭ�ӣ�A�ĺ˴Ź�������ֻ��һ��壬����ȷ��
d��C�Ľṹ��ʽΪ��HOC��CH3��2COOH��������C����������Ӧ������6Ԫ��״�����ʴ���
��ѡac��
(7)���Ͱ�˾ƥ��������ˮ�����ɰ�˾ƥ�֡��߾���E�����ʵķ�Ӧ����ʽ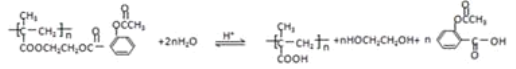 ��
��
(8)ˮ�����ж���ͬ���칹�壬�������ڷ������ܷ���������Ӧ��˵�����з��ǻ���ȩ������ˮ�����ͬ���칹���к���HCOO����-OHʹ��3�ֽṹ������������-OH��һ��-CHOʱ�������ǻ�������λ��2�ֽṹ�������ǻ����ڼ�λʱ��3�ֽṹ�������ǻ����ڶ�λʱ��1�ֽṹ�����Է���������ˮ�����ͬ���칹����9�֡�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����л����������ʶ����ȷ����
A. ��֬�ڿ�������ȫȼ��ת��Ϊˮ�Ͷ�����̼
B. ���ǡ���ѿ�ǵķ���ʽ����C12H22O11������Ϊͬ���칹��
C. ��ˮ��Һ���������е���CH3���Ե����H+
D. ��Ũ��������£�����Ũ���Ṳ�������������ķ�Ӧ����ȡ����Ӧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�����ñ�������Һ�ⶨijNaOH��Һ��Ũ�ȣ��ü�����ָʾ�������в����п���ʹ�ⶨ���ƫ�͵��ǣ� ��
A.��ʽ�ζ�����װ��Һǰδ�ñ�������Һ��ϴ2��3��
B.��ʼʵ��ʱ��ʽ�ζ��ܼ��첿�������ݣ��ڵζ�������������ʧ
C.��ƿ����Һ��ɫ�仯�ɻ�ɫ���ɫ���������µζ���Һ�����ڿ̶�
D.ʢNaOH��Һ����ƿ�ζ�ǰ��NaOH��Һ��ϴ2��3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ӧ��������Ⱦ�����ƿ���������Ҫ�Ӷ�����֣��翪�����������Դ���״���һ�ֿ������������Դ�����й����Ŀ�����Ӧ��ǰ�����ش��������⣺
(1)![]() ��
��![]() �ϳɼ״���
�ϳɼ״���![]() �����ҵ����ʵĴ�������Լ�÷�����ƿ����Ŀǰ��Ҫʹ�ù�������������ǹ��������ϡ�٣��ɱ��߰������Դ��ģӦ�ã���ʹ���д��ڻ�����Ⱦ�ķ��գ����������շ�ܷ��Ʊ��������������ڷ�չ�ǽ�������ʵ��
�����ҵ����ʵĴ�������Լ�÷�����ƿ����Ŀǰ��Ҫʹ�ù�������������ǹ��������ϡ�٣��ɱ��߰������Դ��ģӦ�ã���ʹ���д��ڻ�����Ⱦ�ķ��գ����������շ�ܷ��Ʊ��������������ڷ�չ�ǽ�������ʵ��![]() �����ԭ�Ʊ��״�����ȡ����Ҫ��չ���÷�Ӧ������ͼ��ʾ��
�����ԭ�Ʊ��״�����ȡ����Ҫ��չ���÷�Ӧ������ͼ��ʾ��

���õ��ĸ�������CO��![]() ��������Խ϶�ĸ�����Ϊ________________�������ϳɼ״��ķ�Ӧ���ʽ�����Ҫʹ��Ӧ���ʼӿ죬��Ҫ�������б仯��________
��������Խ϶�ĸ�����Ϊ________________�������ϳɼ״��ķ�Ӧ���ʽ�����Ҫʹ��Ӧ���ʼӿ죬��Ҫ�������б仯��________![]() ����ĸ
����ĸ![]() �������仯��
�������仯��
A.![]() B��
B��![]()
C.![]() D��
D��![]()
(2)��ѹ![]() �������ݻ��ɱ�
�������ݻ��ɱ�![]() �£�
�£�![]() ��
��![]() �ڴ��������·�����Ӧ
�ڴ��������·�����Ӧ![]()
![]() ��
��![]() ��ƽ��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��
��ƽ��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��

��ѹǿ![]() ________
________![]() ����
����![]() ������
������![]() ��
��![]() ��
��
����![]() ��
��![]() �����£�b��ʱ
�����£�b��ʱ![]() ________
________![]() ����
����![]() ������
������![]() ��
��![]() ��
��
����֪����Ӧ����![]() ��
��![]() ��
��![]() �ֱ�Ϊ�����淴Ӧ���ʳ�����xΪ���ʵ�����������b���Ӧ���������Ϊ
�ֱ�Ϊ�����淴Ӧ���ʳ�����xΪ���ʵ�����������b���Ӧ���������Ϊ![]() ������b����
������b����![]() ________
________![]() ����3λ��Ч����
����3λ��Ч����![]() ��
��
(3)��̿��ˮ�����ں����ܱ������з�Ӧ�ƺϳ�������Ҫ��Ӧ![]() ��
��![]() ��
��![]() ��
��![]() ��
��![]() Ϊ�Է�ѹ��ʾ��ƽ�ⳣ��
Ϊ�Է�ѹ��ʾ��ƽ�ⳣ��![]() ��T�Ĺ�ϵ����ͼ��ʾ��
��T�Ĺ�ϵ����ͼ��ʾ��

�ٷ�Ӧ![]() ��
��![]() ��
��![]() ________
________![]() ��������������������������
��������������������������![]() ��
��
��![]() ��ʱ����Ӧ
��ʱ����Ӧ![]() ��
��![]() ________
________![]() ����ֵ
����ֵ![]() ��
��
���ں����ܱ������г���![]() ��
��![]() ֻ������Ӧ
ֻ������Ӧ![]() ��
��![]() ��ͼ��d�㴦�ﵽƽ��ʱ��CO��ת����Ϊ________���ﵽƽ��ʱ�����������ٳ���
��ͼ��d�㴦�ﵽƽ��ʱ��CO��ת����Ϊ________���ﵽƽ��ʱ�����������ٳ���![]() ��
��![]() �����´ﵽƽ��ʱ��CO��ƽ��ת����________
�����´ﵽƽ��ʱ��CO��ƽ��ת����________![]() ��������������С������������
��������������������������![]() ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��  �dz���ָʾ����̪��д���û������к��������ŵ����ƣ�______��______��
�dz���ָʾ����̪��д���û������к��������ŵ����ƣ�______��______��
��2��д��3��1��ϩ�Ľṹ��ʽ____________��д���л��� ������____________��
������____________��
��3��  ��һ�ȴ�����____________�֣����ȴ�����____________�֣�
��һ�ȴ�����____________�֣����ȴ�����____________�֣�
��4���л���K���ںϳɸ߷��Ӳ��ϣ�K����![]() ˮ���Ƶã�д��K��Ũ�������������ɵľۺ���Ľṹ��ʽ__________��
ˮ���Ƶã�д��K��Ũ�������������ɵľۺ���Ľṹ��ʽ__________��
��5�� ��һ��ͬ���칹������������ʣ���������ˮ��������NaOH��Һ�����ܷ���������Ӧ���ۺ˴Ź�������������壬�ҷ����֮��Ϊ1��1��1��д���������������������Ʒ�Ӧ�Ļ�ѧ����ʽ___________________________��
��һ��ͬ���칹������������ʣ���������ˮ��������NaOH��Һ�����ܷ���������Ӧ���ۺ˴Ź�������������壬�ҷ����֮��Ϊ1��1��1��д���������������������Ʒ�Ӧ�Ļ�ѧ����ʽ___________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�������Һ����ˮ�����������Ũ��Ϊ1��10-5���� �� ��
A.pH=5��HClO ��ҺB.pH=9�İ�ˮ
C.pH=5��AlCl3��ҺD.pH=5��NaHSO4��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͨ�����SO2�����Ƿ�ﵽ�ŷű��ķ�Ӧԭ����SO2 +H2O2 + BaCl2 ===BaSO4��+ 2HCl��NA��ʾ����٤������������˵����ȷ���ǣ� ��
A. 0.1 mol BaCl2����������������Ϊ0.1NA
B. 25 ��ʱ��pH =1��HCl��Һ�к���H+����ĿΪ0.1NA
C. 17 g H2O2�к��зǼ��Լ���ĿΪ0.5NA
D. ����2.33 g BaSO4����ʱ��ת�Ƶ�����ĿΪ0.01NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ����c(HA)+c(A-)=0.1mol/L��һ��HA��KA�����Һ����Һ��c(HA)��c(A-)��pH�Ĺ�ϵ����ͼ��ʾ��������������ȷ���� �� ��
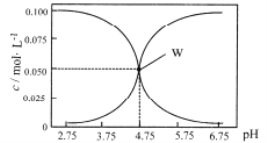
A.pH=5.75����Һ�У�c(K+)>c(A-)>c(HA)> c (H+)>c(OH-)
B.����W����ʾ��Һ����ʼ������ҺӦ����c(HA)+c(A-)=0.1mol/L��c(KA)<c(HA)
C.pH=3.75����Һ�У�c(K+)+c(H+)-c(OH-)+c(HA)=0.1mol/L
D.��A-��ˮ�ⳣ��ΪKh����lgKh=-9.25
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ݻ�Ϊ2 L���ܱ������У��з�ӦmA(g)��nB(g)![]() pC(g)��qD(g)������5 min�ﵽƽ�⣬��ʱ�����ʵı仯ΪA���ʵ���Ũ�ȼ���amol��L��1��B��ƽ����Ӧ����v(B)��a/15 mol��L��1��min��1��C���ʵ���Ũ������2a/3 mol��L��1����ʱ������ϵͳѹǿ������A��C�İٷֺ������䣬��m��n��p��qΪ(����)
pC(g)��qD(g)������5 min�ﵽƽ�⣬��ʱ�����ʵı仯ΪA���ʵ���Ũ�ȼ���amol��L��1��B��ƽ����Ӧ����v(B)��a/15 mol��L��1��min��1��C���ʵ���Ũ������2a/3 mol��L��1����ʱ������ϵͳѹǿ������A��C�İٷֺ������䣬��m��n��p��qΪ(����)
A.3��1��2��2B.1��3��2��2C.3��1��2��1D.1��1��1��1
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com