
����Ŀ������ֲ���纣���������к��зḻ�ĵ�Ԫ�أ���Ҫ�Ե⻯����ʽ���ڡ���һ��ѧ����С���ú���Ϊԭ����ȡ�����ⵥ�ʣ����ǽ��������ճɻң���ˮ����һ��ʱ��(�õ⻯�����ܽ���ˮ��)���õ�����������Һ��Ȼ������ʵ��������ȡ���ʵ⣺

��1��ָ����ȡ��Ĺ������йص�ʵ��������ƣ���_________��_________
��2�������������õ��л��Լ�������CCl4������ѡ������_________________________________��
��3���������̢۰������¼�����
A�������Һ©���������ϿڵIJ������Ƿ�©Һ�� B����ʢ����Һ�ķ�Һ©����������̨����Ȧ�У� C����50 mL��ˮ��15 mL�л��ܼ�(����ѡ��)�����Һ©���У����Ǻò������� D����ת©������������ʱ�����������������رջ������ѷ�Һ©�������� E�����á��ֲ㣻 F����©���ϿڵIJ�������ʹ���ϵİ�����©���Ͽڵ�С���� G���������������ձ�������Һ�� H���ӷ�Һ©���Ͽڵ����ϲ�Һ�塣
a������F��������Ŀ���ǣ�_____________________________
b�������CCl4��Һ��ͨ��_____________________���(����©���Ͽ�������©���¿���)��
��4���Ӻ�����л���Һ����ȡ��ͻ����л���ҺCCl4������Ҫ�������۲���ͼ��ʾʵ��װ�ã�ָ����������b__________����ȴˮ��____���루��A��B��,��������_________________������������ƣ�

���𰸡����� ��ȡ��Һ ������ˮ���ܽ�������Զ����ˮ ƽ��ѹǿ����Һ������ ©���¿� ������ B ������ƿ
��������
������ȡ�������ʵ��װ����ʵ�鲽���ʵ��ԭ������������⡣
��1������Һ�Ͳ����Թ������ķ����ǹ��ˣ��ӵ�ˮ�л�ȡ�ⵥ�ʲ�����ȡ��Һ�ķ�����
�ʴ�Ϊ�����ˣ���ȡ��
��2����������ȡ���е��ܽ�ȴ�����ԭ�ܼ��е��ܽ�ȣ����ʺ���ȡ������Ӧ����ȡ����ԭ���ܼ����ܻ��ܣ�CCl4������ȡ����ѡȡ�������Կ�����CCl4����ȡ����
��3��a��Ϊ��ʹ©���ڵ�ѹǿ����������ѹ��ƽ��ѹ��ʱҺ��˳��������
b��CCl4���ܶȴ���ˮ���ܶȣ�����CCl4���²㣬��©���¿�������
��4��ʵ��װ��������װ�ã�����b�������ܣ���ȴˮ��B���룬A������CCl4�ķе�ͣ�ˮԡ�����CCl4����������������ƿ�С�


 �����������Ů��ͯ������ϵ�д�
�����������Ů��ͯ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ɢ������ֱ����1nm��100nm ֮��ķ�ɢϵ�ǣ�������
A.��Һ
B.����Һ
C.����
D.����Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ�����ר�Һ�°���������Ƽ����Ϊ�����Ƽҵ������ͻ�����ס�����NaCl��NH3��CO2��Ϊԭ�����Ƶ�NaHCO3����������������йػ�ѧ����ʽ��NH3��CO2��H2O===NH4HCO3NH4HCO3��NaCl===NaHCO3����NH4Cl��2NaHCO3![]() Na2CO3��CO2����H2O��
Na2CO3��CO2����H2O��
(1)̼������뱥��ʳ��ˮ��Ӧ��������̼�����ƾ����ԭ������____��
a��̼������������ˮ
b��̼�����������ֽ�
c��̼�����Ƶ��ܽ����Խ�С����������Һ�����Ƚᾧ����
(2)ij̽���С����������Ƽ�ԭ��������̼�����Ƶ��Ʊ�ʵ�飬ͬѧ������˸��ַ�����
Aͬѧ��������̼����ͨ�뺬���ı���ʳ��ˮ���Ʊ�̼�����ƣ�ʵ��װ������ͼ��ʾ(ͼ�мг֡��̶��õ�����δ����)���Իش������й����⣺


����װ���е��Լ���____________��
�ڶ�װ����ϡ�����������______________________��
��ʵ����������NaHCO3����IJ�����________(��������������)��
Bͬѧ��ͼ����װ��(����װ��δ����)����ʵ�飺
�� ʵ��ʱ�����ȴ�________��ͨ��________ ���壬�ٴ�________����ͨ��________���壻
����ͬѧ��������װ�õ�b���¶����Ӽ�װ�ã�������_____________________________��
(3)������д��һ��ʵ������ȡ����̼�����Ƶķ�����________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ع���ԭ����ͼ��ʾ�������й�˵���������

A. ���·�ĵ�����������a��b
B. �����ĵ缫��ӦΪ��O2+4e-+4H+=2H2O
C. 1molC6H12O6��ȫ��Ӧ����CO2��ת��24mol����
D. ��Ӧһ��ʱ�����ڲ������������ʵ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ȵ�ƽ���������Ƹ�Ѫѹ���Ľ�ʹ�����м���F�ĺϳ�·������ͼ���£�

��1��F�еĺ�������������Ϊ��������________��________�ȡ�
��2��D![]() E�ķ�Ӧ����Ϊ___________
E�ķ�Ӧ����Ϊ___________
��3��X�ķ���ʽΪC7H5Ocl��д��X�Ľṹ��ʽ��___________
��4��д��ͬʱ��������������E��һ��ͬ���칹��Ľṹ��ʽ��___________
�ٺ�������������-�����������FeCl3��Һ������ɫ��Ӧ�۷�����ֻ��5�ֲ�ͬ��ѧ��������
��5����֪��CH3CH2CN![]() CH3CH2COOH����д����CH3CH2OH��NCCH2CN��
CH3CH2COOH����д����CH3CH2OH��NCCH2CN��![]() Ϊԭ���Ʊ�
Ϊԭ���Ʊ� �ĺϳ�·������ͼ(���Լ����ã��ϳ�·������ͼʾ�����������)��____________
�ĺϳ�·������ͼ(���Լ����ã��ϳ�·������ͼʾ�����������)��____________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ����������Ӿۺ������͵�����������Ͼ����ֳ��Ͽ�ĵ缫��Ӧ����ѧ��ʹ�õ�ر��ֳ����Ƶ������ĸ߹������ܡ�����ѭ����ŵ�ߴ�50000�Σ���ԶԶ�����˴�ͳ�ɳ���ص�ѭ������(<10000��)����ŵ�ʱ�Ĺ���ԭ����ͼ������˵������ȷ����
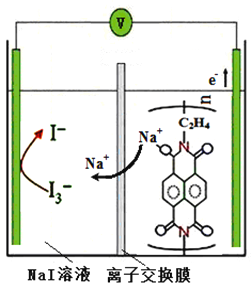
A. ���ʱ�������ĵ缫��ӦʽΪ3I-��2e-=I3-
B. ���ӽ���Ĥֻ����������ͨ����������������ͨ��
C. �ŵ�ʱ����ת��0.5mol����ʱ��NaI��Һ������NA��Na+
D. �ŵ�ʱ���߾����������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��NaCl��NH4Cl��NaHCO3���ܽ�����ߣ�����˵������ȷ������ ��

A. t1��ʱ������NaCl��NH4Cl��Һ������������ͬ
B. ��ͬ�¶��£�NaHCO3��ˮ�е��ܽ�ȱ�NaCl��NH4ClС�ܶ�
C. NH4Cl�ܽ�����¶ȱ仯�ϴ�
D. t1��������NaCl��NH4Cl��Һ�����ʵ���Ũ����ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������C9H10O2������ˮ����ζ������������ˮ�㾫�����쾫�ͣ���������ʳƷ��ҵ�У�Ҳ�������л��ϳ��м��塢�ܼ��ȡ����Ʊ�����Ϊ��
��֪��

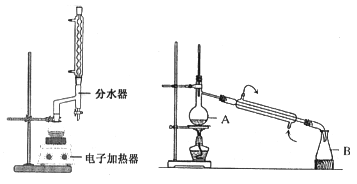
ʵ�鲽�����£�����100 mLԲ����ƿ�м���12.20 g�����ᡢ25mL�Ҵ�����������20mL�����飬�Լ�4mLŨ���ᣬ��Ͼ��Ȳ������ʯ��������ͼ��ʾװ�������������¶���65��70����Ȼ���2h����Ӧʱ������-�Ҵ�-ˮ���γɡ���������е�62.6�棩��������������÷�ˮ�����Ϸ����ȥ��Ӧ���ɵ�ˮ��������������Ҵ���
�ڷ�Ӧ�������������ų���ˮ����Һ��ر��������������ȣ�����ˮ�����ռ�����Һ�岻���������ӣ�ֹͣ���ȡ�
�۽���ƿ�ڷ�ӦҺ����ʢ������ˮ���ձ��У���������Na2CO3����Һ�����ԡ�
���÷�Һ©���ֳ��л��㣬ˮ����25mL������ȡ��Һ��Ȼ��ϲ��л��㡣�����Ȼ��ƣ��Դֲ�Ʒ��������װ����ͼ��ʾ���������������Ѻ�������£�����210��213�����֡�
�ݼ���ϸ�ò�Ʒ���Ϊ12.86mL.
(1)�������ʹ�÷�ˮ�����Ϸ����ȥˮ��Ŀ����_________________��
(2)�������Ӧ������ֵ��¶���___________________��
A��65��70�� B��78��80�� C��85��90�� D��215��220��
(3)���������Na2CO3���벻�㣬�ڲ��������ʱ��������ƿ�пɼ����������ɣ������������ԭ����_____________��
(4)������з�Һ����������ȷ����__________��
A.ˮ��Һ�м������ѣ�ת������Һ©���У����ϲ�����������Һ©����ת������ҡ
B.��ҡ���κ����Һ©���¿ڵIJ���������
C.��������ҡ���������ֳַ�Һ©�����ô�Һ��ֲ�
D.��Һ����ʱ����Һ©���е��²�Һ�����¿ڷų���Ȼ���ٽ��ϲ�Һ�����¿ڷų�
����װ��ͼ������A��������___________���ڲ�����м����Ȼ��Ƶ�������_________��
(5)��ʵ���Ʒ�IJ���Ϊ____________��
���𰸡� ������ƽ�ⲻ�����������ƶ�����߱������������� C �����������л��б����ᣬ��������100��ʱ�������� AB ������ƿ ��ˮ�� 90.02%
��������������������⿼�鱽�����������Ʊ���
��1����Ӧ![]() +CH3CH2OH
+CH3CH2OH![]()
![]() +H2OΪ���淴Ӧ��ʹ�÷�ˮ�����Ϸ����ȥˮ����С������Ũ�ȣ�������ƽ�ⲻ��������Ӧ�����ƶ�����߱����������IJ��ʡ�
+H2OΪ���淴Ӧ��ʹ�÷�ˮ�����Ϸ����ȥˮ����С������Ũ�ȣ�������ƽ�ⲻ��������Ӧ�����ƶ�����߱����������IJ��ʡ�
��2���������⣬��Ӧʱ������-�Ҵ�-ˮ���γ����������������������ƿ�ڵı����������л����Ҵ��������顢������������������������������������������е��Ҵ��������飬�Ҵ��ķе�Ϊ78.3����������ķе�Ϊ80.8���������������ķе�Ϊ212.6�������Բ�����Ӧ������ֵ��¶���85~90������ѡC��
��3���������м���Na2CO3��ȥ�����������л��еı���������ᣬ��Na2CO3���벻�㣬������û����ȫ��ȥ������������ʱ������ƿ�пɼ����̵�ԭ���ǣ������������л��б���������������������100��ʱ����������
��4��A��Ϊ��ʹ���Ѻ�ˮ��Һ��ֽӴ���ˮ��Һ�м�������ת������Һ©���к������ϲ�����������Һ©����ת������ҡ��A����ȷ��B��Ϊ��ֹ��Һ©������ѹ����������������ҡ���κ����Һ©���¿ڵIJ�����������B����ȷ��C����������ҡ���������轫��Һ©����������̨�Ͼ��á���Һ��ֲ㣬C�����D����Һ����ʱ����Һ©���е��²�Һ�����¿ڷų���Ȼ���ϲ�Һ����Ͽ��㵹������D�����ѡAB������װ��ͼ������A��������������ƿ���ڲ������м���CaCl2����������Ϊ��ˮ������ȥˮ��
��5�������Ҵ��������Ա���������������ɵı�����������![]() ~
~![]() ��n������������������=n�������ᣩ=
��n������������������=n�������ᣩ=![]() =0.1mol��m������������������=0.1mol
=0.1mol��m������������������=0.1mol![]() 150g/mol=15g����ʵ���Ʒ�IJ���=
150g/mol=15g����ʵ���Ʒ�IJ���=![]() 100%=90.02%��
100%=90.02%��
�����͡�ʵ����
��������
19
����Ŀ��������������Ԫ�صĵ�һ�����ĵ��������ݣ���λ��kJ/mol�����ش�������⣺
Ԫ�ش��� | I1 | I2 | I3 | I4 |
R | 500 | 4600 | 6900 | 9500 |
S | 740 | 1500 | 7700 | 10500 |
T | 580 | 1800 | 2700 | 11600 |
U | 420 | 3100 | 4400 | 5900 |
(1)�����ڱ��У�����ܴ���ͬһ�����___________
A��S��U B��S��T C��T��U D��R��T E��R��U
(2)T���Ȼ���Ļ�ѧʽΪ___________________
(3)���UԪ���Ƕ����ڵ�Ԫ�أ���������ĵ�2�ε����ܷ�Ծ���ݽ��ǵ�_____����
(4)���R��S��T��ͬ���ڵ���������Ԫ�أ������ǵ�ԭ��������С�����˳����_________������Ԫ��_______�ĵ�һ�����ܷ����ߵ�ԭ����_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������Һ����ij�Ȼ�þ���Ȼ����Ļ����Һ�У�������ͼ��仯������ȷ��( )
A. 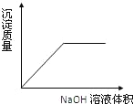 B.
B. 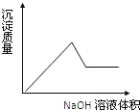
C. 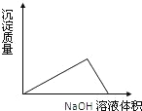 D.
D. 
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com