
【题目】A是化学实验室中最常见的有机物,它易溶于水并有特殊香味,能进行如图所示的多种反应。
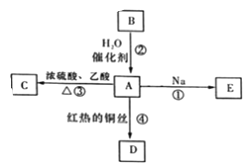
(1)A的官能团名称是____________,B的结构简式____________。
(2)反应②的反应类型为________________________________。
(3)发生反应①时钠在__________________________(填“液面上方”或“液体底部”)。
(4)写出反应③的化学方程式_______________________。
(5)写出反应④的化学方程式_______________________。
【答案】羟基 CH2=CH2 加成反应 液体底部 C2H5OH+CH3COOH![]() CH3COOC2H5+H2O 2C2H5OH+O2
CH3COOC2H5+H2O 2C2H5OH+O2![]() 2CH3CHO+2H2O
2CH3CHO+2H2O
【解析】
A是化学实验室中最常见的有机物,它易溶于水并有特殊香味,A能和Na、乙酸、红热的铜丝反应,B和水在催化剂条件下反应生成A,则B为CH2=CH2,A为CH3CH2OH,在浓硫酸作催化剂条件下,乙醇和乙酸发生酯化反应生成C,C为CH3COOCH2CH3,A在红热的Cu丝作催化剂条件下发生催化氧化反应生成D,D为CH3CHO,A和Na反应生成E,E为CH3CH2ONa,据此分析解答。
(1)A为乙醇,结构简式为CH3CH2OH,含有的官能团为羟基,B是乙烯,结构简式为CH2=CH2,故答案为:羟基;CH2=CH2;
(2)反应②为乙烯和水发生反应生成乙醇,为加成反应,故答案为:加成反应;
(3)钠的密度大于乙醇,所以将钠投入乙醇中,钠在液体底部,故答案为:液体底部;
(4)反应③为乙醇和乙酸发生的酯化反应,反应的化学方程式为CH3COOH+C2H5OH ![]() CH3COOC2H5+H2O,故答案为:CH3COOH+C2H5OH
CH3COOC2H5+H2O,故答案为:CH3COOH+C2H5OH ![]() CH3COOC2H5+H2O;
CH3COOC2H5+H2O;
(5)反应④是乙醇催化氧化生成乙醛,反应的化学方程式为:2CH3CH2OH+O2 ![]() 2CH3CHO+2H2O,故答案为:2CH3CH2OH+O2
2CH3CHO+2H2O,故答案为:2CH3CH2OH+O2 ![]() 2CH3CHO+2H2O。
2CH3CHO+2H2O。


 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:
【题目】汉黄芩素是传统中草药黄芩的有效成分之一,对肿瘤细胞的杀伤有独特作用。下列有关汉黄芩素的叙述正确的是( )

A. 汉黄芩素的分子式为C16H13O5
B. 与足量H2发生加成反应后,该分子中官能团的种类减少1种
C. 1 mol该物质与溴水反应,最多消耗1 mol Br2
D. 该物质遇FeCl3溶液显紫色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A.次氯酸钠溶液中通入少量的二氧化硫:SO2+3ClOˉ+H2O=SO42ˉ+Clˉ+2HClO
B.碳酸氢钠溶液与足量盐酸反应:CO32ˉ+2H+=CO2↑+H2O
C.稀硫酸和氢氧化钡溶液反应:Ba2++OHˉ+H++SO42ˉ= BaSO4↓+H2O
D.锌和浓硫酸反应:Zn+2H+=H2↑+Zn2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017年5月5日,中国首架按照国际标准研制,拥有自主知识产权的大型客机C-919在上海浦东机场首飞,科学家在实验室研究利用催化技术将飞机尾气中的NO和CO转变成CO2和N2,其反应为2NO(g)+2CO(g)![]() N2(g)+2CO2(g)。
N2(g)+2CO2(g)。
(1)上述反应的熵变ΔS__0(填“>”“<”或“=”,下同),该反应能够自发进行,则反应的ΔH__0。
(2)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是__(填字母代号,下同)
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
(3)一定温度下,将体积比为1∶2的NO、CO气体置于恒容密闭容器中发生上述反应,下列能说明反应达到平衡状态的是___。
A.体系压强保持不变
B.混合气体颜色保持不变
C.N2和CO2的物质的量之比保持不变
D.每生成1molN2的同时生成2molNO
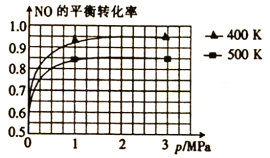
(4)已知上述反应中NO的平衡转化率与压强、温度的关系如图所示。工业上催化装置比较适合的温度和压强是__。
A.400K;3MPa B.400K;1.5MPa C.400K;1MPa D.500K;1MPa
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向25 mL 0.1 mol.L-1NaOH溶液中逐滴滴加0.2 mol.L-1的HN3(叠氮酸)溶液,pH的变化曲线如图所示(溶液混合时体积的变化忽略不计,叠氮酸的Ka=10-4.7)。下列说法正确的是

A. 水电离出的c(H+):A点小于B点
B. 在B点,离子浓度大小为c(OH-)>c(H+)>c (Na+)>c(N3-)
C. 在C点,滴加的V(HN3)=12.5 mL
D. 在D点,c(Na+)=2c(HN3)+2 c(N3-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将![]() 转变为
转变为![]() 的方法为( )
的方法为( )
A.溶液加热,通入足量的HCl
B.与足量的NaOH溶液共热后,再通入CO2
C.与稀H2SO4共热后,加入足量的Na2CO3
D.与稀H2SO4共热后,加入足量的NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
化合物M是合成香精的重要原料。实验室由A和芳香烃E制备M的一种合成路线如下:
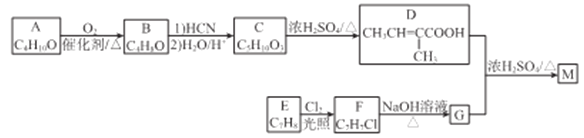
已知: (R1、R2表示烃基或H原子)
(R1、R2表示烃基或H原子)
请回答下列题:
(1)A的化学名称为_________,B的结构简式为________。
(2)C中官能团的名称为________。
(3)D分子中最多有___个原子共平面。
(4)E→F的反应类型为________。
(5)D+G→M的化学方程式为________。
(6)同时满足下列条件的D的同分异构体有___种(不考虑立体异构),其中核磁共振氢谱有3组峰的结构简式为________。
①能发生水解反应和银镜反应; ②不含环状结构
(7)参照上述合成路线和信息。以![]() 为原料(其他无机试剂任选),设计制备
为原料(其他无机试剂任选),设计制备 的合成路线_______________________。
的合成路线_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E、F六种元素,A是周期表中原子半径最小的元素,B是电负性最大的元素,C的2p轨道中有三个未成对的单电子,F原子核外电子数是B与C核外电子数之和,D是主族元素且与E同周期,E能形成红色(或砖红色)的E2O和黑色的EO两种氧化物,D与B可形成离子化合物,其晶胞结构如图所示.请回答下列问题.
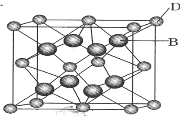
(1)E元素原子基态时的电子排布式为_________.
(2)A2F分子中F原子的杂化类型是_________
(3)CA3极易溶于水,其原因主要是_________,
(4)富勒烯衍生物由于具有良好的光电性能,在太阳能电池的应用上具有非常光明的前途.富勒烯(C60)的结构如图,分子中碳原子轨道的杂化类型为_________;1molC60分子中σ键的数目为_________.

(5)多元化合物薄膜太阳能电池材料为无机盐,其主要包括砷化镓、硫化镉、硫化锌及铜铟硒薄膜电池等.
①第一电离能:As_________Se(填“>”“<”或“=”).
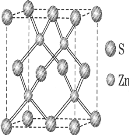
②硫化锌的晶胞中(结构如图所示),硫离子的配位数是_________与S距离最近且等距离的S之间的距离为_________(密度为ρg/cm3)
③二氧化硒分子的空间构型为_________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨和水都是常用的试剂。请回答下列问题:
(1)氮元素基态原子的核外电子中,未成对电子数成对电子数之比为_____。
(2)NH3分子可结合一个H+形成铵根离子(NH4+)。
①NH3分子中N原子的杂化类型是_____。
②NH3分子中与H+结合的过程中未发生改变的是_____(填序号)。
a 微粒的空间构型 b N原子的杂化类型 c H—N—H的键角
(3)将氨气通入CuSO4溶液中,产生蓝色沉淀,继续通过量氨气,沉淀溶解,得到蓝色透明溶液。该过程中微粒的变化是[Cu(H2O)6]2+→Cu(OH)2→[Cu(NH3)4]2+。 [Cu(H2O)6]2+和[Cu(NH3)4]2+中共同含有的化学键类型是_______。
(4)在冰晶体中,每个水分子与相邻的4个水分子形成氢键,则冰晶体中氢键的“键能”是_____ kJ·mol(已知冰的升华热是51 kJ·mol-1),水分子间范德华力的能量为11 kJ·mol-1);水变成冰晶体时,密度减小的主要原因是________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com