
【题目】用如图电解装置将雾霾中的SO2、NO转化为(NH4)2SO4,用其作为一种优良的氮肥。下列有关说法正确的是
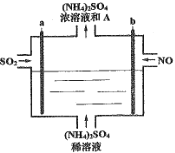
A.a与电源负极相连,发生还原反应
B.每处理lmolNO可以生成2molA
C.通电后阳极附近溶液的pH增大
D.理论上将SO2与NO以体积比2:5通入装置可彻底转化
【答案】B
【解析】
SO2、NO转化为(NH4)2SO4,二氧化硫中S的化合价由+4到+6价,化合价升高,失去电子,发生氧化反应,则a为阳极;NO的化合价降低,得到电子,发生还原反应,则b为阴极;结合电子守恒和元素守恒可知该电解过程的总反应为5SO2+2NO+8H2O (NH4)2SO4+4H2SO4。
(NH4)2SO4+4H2SO4。
A.电极a为阳极,与电源正极相连,发生氧化反应,故A错误;
B.电解池的总反应为5SO2+2NO+8H2O (NH4)2SO4+4H2SO4,产物中除有(NH4)2SO4外还有H2SO4,即A为硫酸,根据方程式,消耗1mol的NO生成2mol的硫酸,故B正确;
(NH4)2SO4+4H2SO4,产物中除有(NH4)2SO4外还有H2SO4,即A为硫酸,根据方程式,消耗1mol的NO生成2mol的硫酸,故B正确;
C.阳极的电极反应为2H2O+SO2-2e-=SO42-+4H+,溶液的pH应降低,故C错误;
D.根据电池总反应电解池的总反应为5SO2+2NO+8H2O (NH4)2SO4+4H2SO4,理论上将SO2与NO以体积比5:2通入装置可彻底转化,故D错误;
(NH4)2SO4+4H2SO4,理论上将SO2与NO以体积比5:2通入装置可彻底转化,故D错误;
故答案为B。


科目:高中化学 来源: 题型:
【题目】关于下列各装置图的叙述不正确的是( )


A.用图①装置实现铁上镀铜,a极为铜,电解质溶液可以是CuSO4溶液
B.图②装置盐桥中KCl的Cl-移向右烧杯
C.图③装置中钢闸门应与外接电源的负极相连获得保护
D.图④两个装置中通过导线的电子数相同时,消耗负极材料的物质的量不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可溶性钡盐有毒,医院中常用硫酸钡这种钡盐作为内服造影剂。医院抢救钡离子中毒患者时,除催吐外,还需要向中毒者胃中灌入硫酸钠溶液。已知:Ksp(BaCO3)=5.1×10-9 mol2·L-2;Ksp(BaSO4)=1.1×10-10 mol2·L-2。下列推断正确的是( )
A. 不用碳酸钡作为内服造影剂,是因为Ksp(BaCO3)>Ksp(BaSO4)
B. 抢救钡离子中毒患者时,若没有硫酸钠,可以用碳酸钠溶液代替
C. 若误饮[Ba2+]=1.0×10-5 mol·L-1的溶液时,会引起钡离子中毒
D. 可以用0.36 mol·L-1的Na2SO4溶液给钡离子中毒患者洗胃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究不同 pH 时 CuSO4 溶液对 H2O2 分解的催化作用。资料:a.Cu2O 为红色固体,难溶于水,能溶于硫酸,生成 Cu 和Cu2+。b.CuO2 为棕褐色固体,难溶于水,能溶于硫酸,生成 Cu2+和 H2O2。c.H2O2 有弱酸性:H2O2 ![]() H+ +HO2-,HO2-
H+ +HO2-,HO2- ![]() H+ +O22-。
H+ +O22-。
编号 | 实验 | 现象 |
Ⅰ | 向 1 mL pH=2 的 1 mol·L 1 CuSO4溶液中加入 0.5 mL 30% H2O2 溶液 | 出现少量气泡 |
Ⅱ | 向 1 mL pH=3 的 1 mol·L 1 CuSO4溶液中加入 0.5 mL 30% H2O2 溶液 | 立即产生少量棕黄色沉淀,出现较明显气泡 |
Ⅲ | 向 1 mL pH=5 的 1 mol·L 1CuSO4溶液中加入 0.5 mL 30% H2O2 溶液 | 立即产生大量棕褐色沉淀,产生大量气泡 |
(1) 经检验生成的气体均为 O2,Ⅰ中 CuSO4 催化分解 H2O2 的化学方程式是__。
(2)对Ⅲ中棕褐色沉淀的成分提出 2 种假设:ⅰ.CuO2,ⅱ.Cu2O 和CuO2 的混合物。为检验上述假设,进行实验Ⅳ:过滤Ⅲ中的沉淀,洗涤,加入过量硫酸,沉淀完全溶解,溶液呈蓝色,并产生少量气泡。
①若Ⅲ中生成的沉淀为 CuO2,其反应的离子方程式是__。
②依据Ⅳ中沉淀完全溶解,甲同学认为假设ⅱ不成立,乙同学不同意甲同学的观点,理由是__。
③为探究沉淀中是否存在 Cu2O,设计如下实验:
将Ⅲ中沉淀洗涤、干燥后,取 a g 固体溶于过量稀硫酸,充分加热。冷却后调节溶液 pH,以 PAN 为指示剂,向溶液中滴加 c mol·L 1EDTA 溶液至滴定终点,消耗 EDTA 溶液 V mL。V=__,可知沉淀中不含 Cu2O,假设ⅰ成立。(已知:Cu2++EDTA= EDTA-Cu2+,M(CuO2)=96 g·mol 1,M(Cu2O)=144 g·mol1)
(3)结合方程式,运用化学反应原理解释Ⅲ中生成的沉淀多于Ⅱ中的原因__ 。
(4)研究Ⅰ、Ⅱ、Ⅲ中不同 pH 时 H2O2 分解速率不同的原因。
实验Ⅴ:在试管中分别取 1 mL pHspan>=2、3、5 的 1 mol·L1 Na2SO4 溶液,向其中各加入 0.5 mL 30% H2O2 溶液,三支试管中均无明显现象。
实验Ⅵ:__(填实验操作和现象),说明 CuO2 能够催化 H2O2 分解。
(5)综合上述实验,Ⅰ、Ⅱ、Ⅲ中不同 pH 时 H2O2 的分解速率不同的原因是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴元素由于其良好的物理化学性质,被广泛应用于生产生活中。利用含钴废料(含CoO、Co2O3、金属Al、Li等)制取CoCl2·6H2O的流程图如图所示
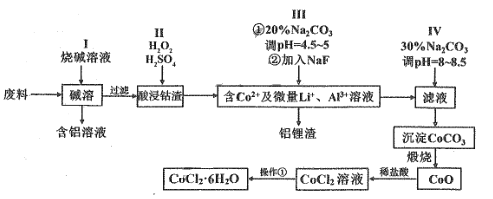
(1)写出步骤I中主要反应的化学方程式_______。
(2)步骤II中可用盐酸代替H2SO4与H2O2的混合液,但缺点是___________。
(3)步骤III①中Na2CO3溶液的作用是__________。
(4)若在实验室煅烧 CaCO3,所需硅酸盐材质的仪器除酒精灯和玻璃棒外,还有______(填仪器名称)。
(5)操作①的步骤是______、________、过滤、洗涤、干燥。洗涤过程中可以用乙醇和水的混合液代替水的优点是_______。
(6)CoCl26H2O晶体受热易分解,取119g该晶体加热至某一温度,得到CoCl2xH2O晶体83g,则x=_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】周期表前四周期的元素 A、B、C、D、E,原子序数依次增大。A的核外电子总数与其期序数相同,B和D位于同一周期且未成对电子数等于其周期序数,E为第四周期元素,最外层只有一个电子,次外层的所有轨道均充满电子。
(1)B、C、D三种元素第一电离能由大到小的顺序为___(填元素符号),E基态原子价层电子排布图为_____。
(2)写出由以上元素组成的BD2的等电子体的分子 _________。
(3)已知D可形成D3+离子,该离子中心原子杂化方式为___,立体构型为__。
(4)温度接近沸点时,D的简单氢化物的实测分子量明显高于用原子量和化学式计算出来的分子量,原因是 _______。
(5)无色的[E(CA3)2]+在空气中不稳定、立即被氧化成深蓝色的[E (CA3)4]2+,利用这个性质可除去气体中的氧气,该反应的离子方程为________。
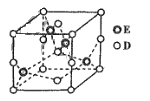
(6)已知E和D形成的一种晶体胞结构如图所示,已知晶胞边长为anm,阿伏加德罗常数为NA,则该晶体的密度为_________ g/cm3(列出计算表达式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示为800℃时A、B、C三种气体在密闭容器中反应时的浓度变化情况,则下列说法错误的是( )
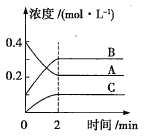
A.发生的反应可表示为2A(g)![]() 3B(g)+C(g)
3B(g)+C(g)
B.前2min,A的分解速率为0.1mol·L-1·min-1
C.2min后反应达到平衡状态
D.2min时,A、B、C的浓度之比为2:3:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是几种常见弱酸的电离平衡常数(25℃ )
化学式 | H2CO3 | CH3COOH | HClO |
电离平衡常数 | K1=4.3×10-7 K2=5.6×10-11 | 1.8×10-5 | 3.0×10-8 |
(1)根据分析表格中数据可知,H2CO3、CH3COOH、HClO三种酸的酸性从强到弱依次是_____________________________________。
(2)常温下,0.1molL﹣1 CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是_________(填字母)
A.c(H+)B.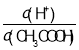 C.c(H+)c(OH﹣)D.
C.c(H+)c(OH﹣)D.![]() E.
E.![]()
(3)25℃时,等浓度的Na2CO3、CH3COONa和NaClO三种溶液的pH从小到大依次是_____________________________________。
(4)25℃时,将a molL﹣1的醋酸与b molL﹣1氢氧化钠等体积混合,反应后溶液恰好显中性,溶液中离子浓度大小关系:_________________
(5)下列反应不能发生的是______(填字母)。
a.![]() +2CH3COOH=2CH3COO-+CO2↑+H2O b.ClO-+CH3COOH=CH3COO-+HClO
+2CH3COOH=2CH3COO-+CO2↑+H2O b.ClO-+CH3COOH=CH3COO-+HClO
c.![]() +2HClO=CO2↑+H2O+2ClO- d.2ClO-+CO2+H2O=
+2HClO=CO2↑+H2O+2ClO- d.2ClO-+CO2+H2O=![]() +2HClO
+2HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是半导体光电化学电池光解水制氢的反应原理示意图。在光照下,电子由价带跃迁到导带后,然后流向对电极。下列说法正确的是

A.半导体电极的电极反应式4OH -4e-=2H2O+O2↑
B.电解一段时间后,溶液的pH减少
C.电解质溶液中的阴离子移向半导体电极
D.整个过程中实现了太阳能—化学能—电能
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com